Немного некромантии: как я оживляю человеческие глаза, чтобы искать новые лекарства
«Игорь… оно живое!»
Мери Шелли "Франкенштейн"
Предупреждение: в статье есть фотография лабораторного препарирования донорского человеческого глаза.
Хориоидальный эксплант формирует сосуды и соединительную ткань в структурном геле.Визуализация данных фазово-контрастной микроскопии с помощью искусственного интеллекта.
В моей лаборатории есть небольшая коллекция человеческих глаз. И это не метафора. Люди обычно улыбаются, но приглашение посмотреть её почему-то не принимают.
На самом деле за этой шуткой стоит довольно интересная научная идея. Мы привыкли думать о смерти как о моменте времени: сердце остановилось, человек умер. Но для клеток всё устроено иначе. Когда организм умирает, миллиарды клеток не выключаются мгновенно. Они ещё какое-то время продолжают существовать как автономные биологические системы. Намного дольше чем принято думать. Самый поздний срок, когда мне удавалось извлечь клетки, способные снова начать делиться в культуре, составлял больше двух недель после смерти.
Меня давно занимал вопрос: можно ли вернуть к жизни часть этой клеточной экосистемы и использовать её, чтобы лучше понять болезни? Могу ли я поймать болезнь в бутылку в чашку петри. Многие болезни глаз нельзя моделировать на животных, в первую очередь потому, что у грызунов нет макулы или трёхмерного зрения. Как же тогда моделировать возрастную макулярную дегенерацию? Сначала я думал создать мышей с глазами как у человека, но потом подумал, зачем всё так усложнять и внедрять сотни генов, когда вокруг нас столько людей в том числе с нужными мне болезнями.
Люди умирают, и их ткани могут помочь науке. Донорские глаза, посмертных доноров, могут помочь сохранить зрение другим людям. Эти ткани получены из донорских глаз, переданных для научных исследований после трансплантационных программ с письменного прижизненного согласия доноров. Все исследования проводятся с соответствующим одобрением комитета по научной этике.
Так появились наши экспланты. На первый взгляд это звучит почти как научная фантастика. Но на самом деле всё гораздо проще - и интереснее.
Процедура препарирования донорского глаза, до хориоидеи ещё нужно добраться через роговицу, хрусталик (у этого донора хрусталик был искусственный), стекловидное тело, сетчатку, чтобы получить заветный лист пигментного эпителия и хориоидеи.
В человеческих глазах много лютеина - каротиноида, который защищает сетчатку. Его же добавляют в витамины и некоторые энергетические напитки. Поэтому у человеческих глаз есть довольно узнаваемый запах. После нескольких лет работы с эксплантами я окончательно перестал любить энергетики. Человеческие глаза пахнут… примерно как Red Bull или Monster.
Мы берём небольшой фрагмент ткани человеческого глаза — пигментный эпителий сетчатки вместе с хориоидеей.
Этот фрагмент помещается в структурный гель и начинает жить как отдельная система.
Гель чуть чуть отличается от того, что используют в игре Soma, но тоже ничего. Даже спустя примерно сутки после смерти донора эти ткани можно «разбудить», дать им тепло, питательную среду, нужный pH, клетки начинают двигаться, взаимодействовать друг с другом, делиться, прорастать в гель, формируя живую систему вне тела.
И именно в такой системе можно наблюдать то, что почти невозможно увидеть иначе — как сосуды начинают растать, как реагируют клетки иммунной системы, как развиваются процессы, лежащие в основе возрастной макулярной дегенерации, диабета и других болезней.
Эти сосуды выросли из кусочка человеческого глаза через пять дней после начала культуры.
Ускоренная съёмка роста экспланта за 3 дня. После восстановления клеточной активности и получив питание и структурный гель, эксплант начинает строить сосудистую оболочку глаза и растить сосуды. Клетки пытаются воссоздать глаз. Легкое мерцание из-за неравномерности освещения.
И у вас может возникнуть вопрос зачем это всё нужно? Кто-то может найти мою работу даже отталкивающей. Но дело в том что я могу взять глаза здорового человек и больного например с возрастной дегенерацией сетчатки или диабетом и они будут вести себя так же как если бы это был человек целиком. Расти, развиваться и самое главное реагировать на лекарственные препараты.
Вот например тут очень хорошо видно, что экспланты с возрастной дегенерацией сетчатки растут намного больше сосудов, чем такой же эксплант от здорового донора. Этот процесс можно остановить если дать им препарат Авастин или его более современные аналоги. Точно так же как его колят в глаза пациентам. При этом на эксплантах хорошо работают самые разные методы исследования, их можно окрашивать антителами и химическими веществами, разбивать на отдельные клетки и проводить потоковую цитометрию, сиквенирования, список можно долго продолжать.
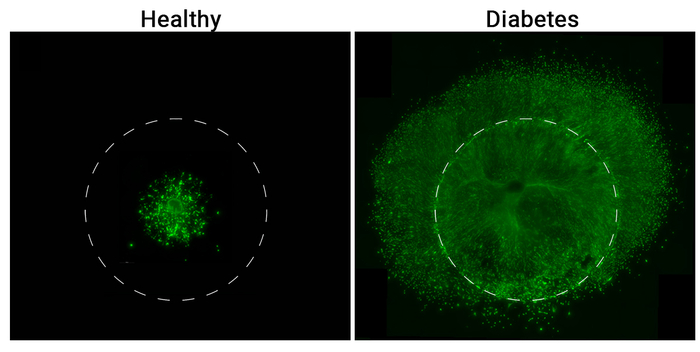
Слева здоровый донор (Healthy), справа человек умерший от осложнений диабета и высокой глюкозы (Diabetes). Круг обозначает границы структурного геля.
Если поместить в культуру экспланты здорового человека и пациента с диабетом, разница становится заметной очень быстро. На образцах диабетических доноров клетки буквально прорываются из структурного геля, обозначенного на изображении кругом. Они активно мигрируют и формируют плотную ткань, похожую на рубец. По сути, это фиброз — тот же процесс, который медленно разрушает ткани внутри глаза при диабете.
Когда смотришь на это под микроскопом, становится очень ясно: высокий уровень глюкозы это не просто цифра в анализе крови. Это сигнал для клеток перестраивать ткани, оставляя после себя что-то похожее на шрам.
Поэтому следите за своей глюкозой. Она влияет на тело гораздо сильнее, чем нам иногда кажется.
С помощью конфокального микроскопа я могу построить трёхмерную модель экспланта. В такой реконструкции хорошо видно, что сосуды прорастают вверх в структурный гель, а фиброзная ткань формируется на дне чашки Петри. Это позволяет разделить сосудистый и фибротический компоненты экспланта без использования антител и флуоресцентных красителей.
Как это всё ведёт к новым методам лечения глазных болезней. Дело в том что экспланты реагируют на лекарственные препараты, так же как это делают полноценные глаза. Более того каждый донорский глаз я могу превратить в 1500 эксплантов, то есть один донор может дать 3000 эксплантов для исследований. Теперь один донор с диабетом или дегенерацией сетчатки может превратиться в 3000 экспериментов с человеческой тканью.
Даже больше, я могу генномодифицировать экспланты создавая аналоги редких человеческих болезней. Когда на всю планету эта болезнь встречается может быть у тысячи человек, мне не нужно ждать когда кто-то из них умрёт и оказаться в течении суток рядом. Я могу болезнь воссоздать в культуре.
Один донор может дать больше научных данных, чем годы экспериментов на мышах.
А самое интересное — я разработал специальный раствор криопротектора, позволяющий погружать экспланты в жидкий азот и хранить их практически в «криосне». Почти как в моём фантастическом романе «Касаясь Пустоты: Чёрная Птица». Где я представляю каким может быть наш мир в 2283 году с развитием биотехнологий и кибернетики.
Это открывает по-настоящему большие возможности. Получив глаза нового донора, мы можем заморозить тысячи эксплантов и затем использовать их по мере необходимости — или отправлять на сухом льду в другие научные центры.
Криобиорепозиторий эксплантов. Температура хранения −196 °C. Почти как в сериале Fallout.
Иногда, уходя вечером из лаборатории, я мысленно говорю своим образцам: «Сладких снов. Берегитесь космических лучей и солнечных вспышек».
Это звучит как шутка, но в ней есть доля правды. Замороженные ткани не способны чинить повреждения ДНК. Космическое излучение и высокоэнергетические частицы со временем могут накапливать мутации в клетках, хранящихся в жидком азоте.
Поэтому криобиорепозитории стараются экранировать и размещать в защищённых помещениях. Даже в замороженном состоянии клетки остаются уязвимыми к радиации.
Иногда меня спрашивают, не странно ли работать с человеческими глазами после смерти человека. Возможно, немного странно. Но на самом деле в этом есть что-то удивительно человеческое. Ткань, которая больше не принадлежит живому человеку, всё ещё может помочь другим людям сохранить зрение.
Каждый донорский глаз можно разделить на тысячи маленьких эксплантов. Тысячи экспериментов. Тысячи попыток понять болезнь. Тысячи шансов найти лекарство или лучше понять болезнь.
Сейчас моя задача — как можно шире распространить эту технологию и сделать так, чтобы меньше экспериментов проводилось на животных.
Во-первых, их просто жалко, особенно если эксперимент оказался неудачным. Во-вторых, эксперименты на животных часто плохо воспроизводятся у человека. Более 90% результатов, которые прекрасно работают на мышах и других мелких позвоночных, в итоге не воспроизводятся у человека или работают совсем иначе. Парадоксально, но иногда лучший способ перестать использовать животных начать изучать человека.
Именно поэтому модели на человеческой ткани так важны. Экспланты позволяют изучать болезни прямо на человеческих клетках, не полагаясь на приближённые модели. Человеческие ткани — самый точный материал для изучения человеческих болезней, ведь мы пытаемся найти методы лечения для болезни человека, а не мышей и крыс. Возможно, это один из редких случаев, когда маленький кусочек ткани после смерти человека может одновременно помочь науке и избавить тысячи животных от экспериментов.
В каком-то смысле это и есть жизнь после смерти — не метафизическая, а вполне практическая, приносящая реальную пользу.
Правда, однажды я попытался объяснить всё это своим соседям, когда они очень опрометчиво спросили, чем же я на самом деле занимаюсь. Я очень люблю свою работу, поэтому рассказал всё подробно - страстно, с примерами и фотографиями. В конце я даже поделился своей заветной мечтой: чтобы после моей смерти мои собственные глаза тоже пополнили коллекцию и послужили науке.
После этого меня почему-то перестали приглашать на барбекю. Соседи начали как-то неловко обходить меня стороной. А через некоторое время и вовсе выставили дом на продажу и переехали в другой штат. Хочется думать, что просто совпадение.
Смерть организма — это конец человека.
Но не всегда конец биологии.
Иногда жизнь продолжается в нескольких миллиметрах ткани на дне лабораторной чашки.
Иногда в лабораторной чашке продолжается тихая жизнь клеток, которая может помочь нам понять болезнь и однажды спасти чьё-то зрение.
И, возможно, это один из самых странных и красивых способов, которыми наука пытается победить слепоту.
Мой небольшой подарок человечеству. Человечеству, которое, честно говоря, об этом подарке особенно не просило.