Новая платформа вакцин на основе мРНК и вычислительных белков обеспечивает мощную защиту от SARS-CoV-2 у мышей!
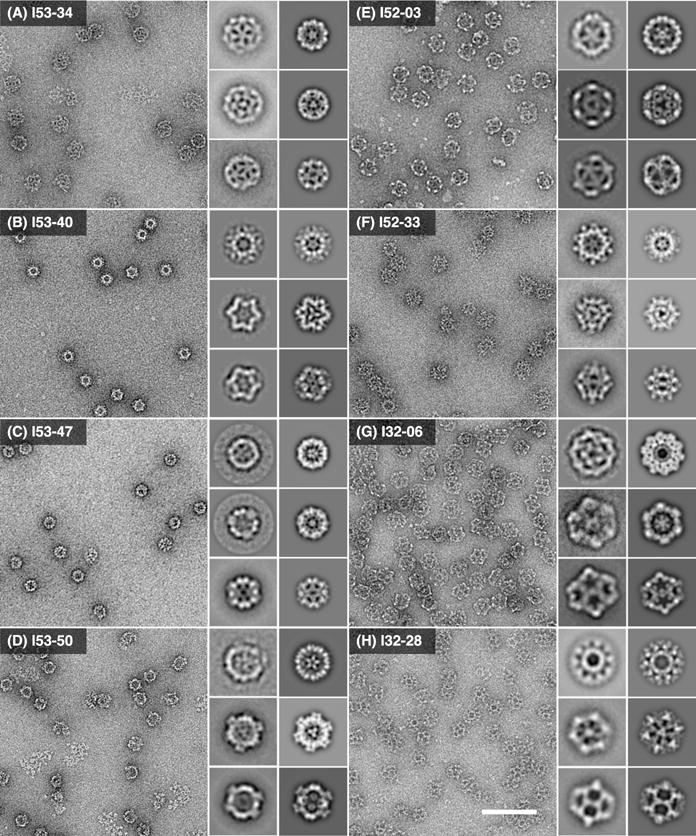
Пример изображения под электронным микроскопом наночастицы белка SARS-CoV-2, разработанной для обеспечения совместимости с мРНК вакцины.
Мультиинституциональная команда ученых из Вашингтонского университета разработала инновационную платформу для вакцин, объединяющую мРНК с вычислительно оптимизированными белковыми наночастицами. Это позволило создать у мышей сильную иммунную защиту от штаммов SARS-CoV-2 Wuhan-Hu-1 и Omicron BA.5.
мРНК-вакцины доказали свою эффективность во время пандемии COVID-19, но продолжаются поиски способов оптимизации. Белковые наночастицы, отображающие множественные копии антигена в упорядоченных массивах, усиливают антительный ответ через кластеризацию В-клеточных рецепторов. Сочетание этих подходов может вызвать как мощный антителообразующий, так и Т-клеточный иммунитет, сохраняя скорость и масштабируемость производства мРНК.
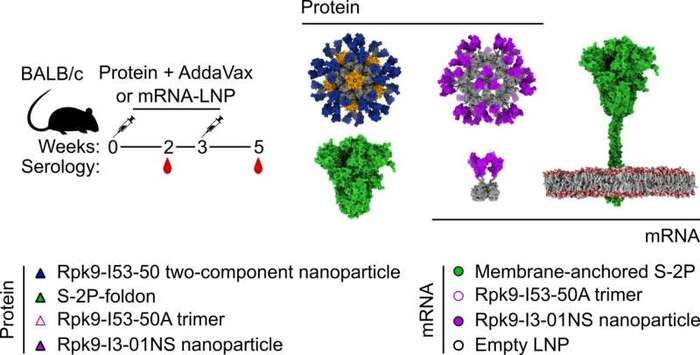
Обзор структуры исследования, показывающий, как новая вакцина Rpk9-I3-01NS тестировалась в различных формах - как традиционная вакцина на основе белка и как вакцина на основе мРНК - и сравнивалась с аналогами существующих вакцин против COVID-19.
В статье "Иммуногены белковых наночастиц, активируемые мРНК с помощью вычислений, вызывают защитные антитело- и Т-клеточные реакции у мышей", опубликованной в Science Translational Medicine, исследователи генетически связали стабилизированный вариант домена рецептор-связывающего домена SARS-CoV-2 (Rpk9) с оптимизированной наночастицей-каркасом из 60 субъединиц (I3-01NS).
Для оценки использовались мыши BALB/c (основная модель) и C57BL/6 (для Т-клеток). Группы по 10 животных тестировали иммуногенность с мРНК в липидных наночастицах или адъювантными белками; контрольные группы получали пустые наночастицы. Контрольные эксперименты включали группы по 4–6 мышей для штаммов Wuhan-Hu-1 MA10 и Omicron BA.5 MA10.
Наночастицы на основе мРНК превзошли стандартные мРНК-вакцины. При однократной дозе титры антител к Wuhan-Hu-1 были в 28 раз выше, чем у мРНК S-2P, и в 11 раз выше, чем у секретируемой мРНК RBD-тримера. Даже низкие дозы давали результаты, сопоставимые с высокими дозами стандартных вакцин. После бустерной дозы наблюдалась стойкая нейтрализация Wuhan-Hu-1 и перекрестная реактивность к Omicron BA.5.
У мышей C57BL/6, вакцинированных мРНК-наночастицами, выявлено значительное количество антиген-специфических CD8-Т-клеток в легких и селезенке — эффект, отсутствующий у получавших белки, что подтверждает вовлечение клеточного иммунитета.
Однократная вакцинация защищала от летального исхода при воздействии адаптированного к мышам Wuhan-Hu-1 SARS-CoV-2, предотвращая потерю веса и элиминируя вирус в легких. Две дозы против Omicron BA.5 предотвращали тяжелое заболевание, подавляя репликацию вируса и сохраняя массу тела.
Авторы представляют эту платформу как способ объединения мультивалентного отображения антигенов с быстрым производством нуклеиновых кислот. Результаты по I3-01NS демонстрируют концепцию: генетически реализуемый, вычислительно спроектированный каркас, пригодный для борьбы с патогенами с соответствующими антигенами.