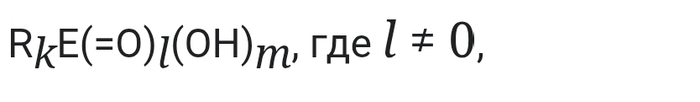Эфиры
Эфиры- совокупное название нескольких классов органических соединений.
Есть три класса эфиров.
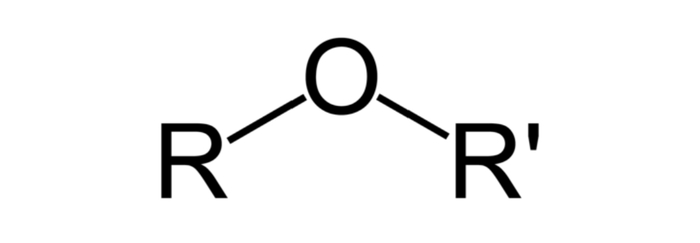
Этеры(простые эфиры)- органические вещества, имеющие формулу R-O-R', где R и R'- алкильные, арильные или другие заместители.
Представляют собой летучие жидкости с приятным запахом.
Простые эфиры используются как растворители для жиров, смол, красителей и лаков. Некоторые эфиры применяются для анестезии. Используются в парфюмерии и многих других сферах.
Получаются при нагревании первичных спиртов (например CH3CH2OH) с концентрированной серной кислотой до 130-140°С. Хотя есть и другие способы получения.
Эстеры(сложные эфиры)- производные кислородных кислот (карбоновых и неорганических) с общей формулой:
Одним из основных способов получения сложных эфиров является этерификация- взаимодействие кислот и спиртов в условиях кислотного катализа.
Сложные эфиры низших карбоновых кислот и простейших спиртов- летучие бесцветные жидкости с зачастую фруктовым запахом.
Сложные эфиры высших карбоновых кислот- бесцветные твёрдые вещества.
Сложные эфиры широко используются в качестве растворителей, пластификаторов, ароматизаторов.
...
Полиэфиры- полимеры, получаемые поликонденсацией многоосновных кислот или их ангидридов с многоатомными спиртами.
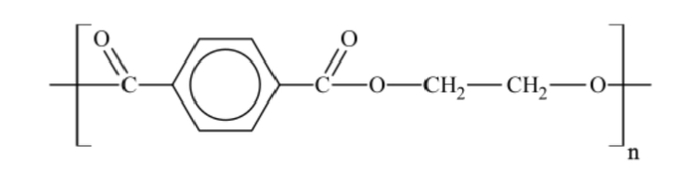
Например, полиэтилентерефталат:
Полиэфиры бывают как природными (янтарь, древесная смола, шеллак и др.), так и синтетическими (полиэстер и т.д.).
Из полиэтилентерефталата и его производных формируют полиэфирное волокно, которое применяется в производстве различных тканей, синтетического меха, канатов, утеплительного материала и прочего.