Карбонильные комплексы
Как испарить тугоплавкий металл без использования высокотемпературных печей?
Как очистить железо до особо чистого состояния?
Как можно соединить вольфрам с органикой?
Как из обычного никеля может получиться яд, токсичность которого в несколько раз выше паров ртути?
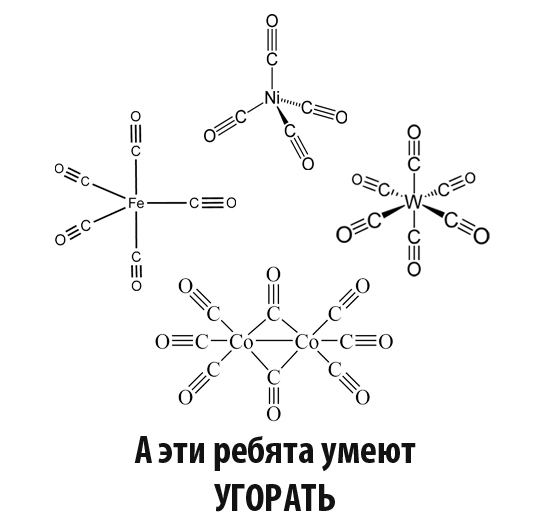
Ответ заключается в необычном соединении молекул угарного газа с атомами переходных металлов, под названием карбонильный комплекс.
В конце XIX века английскими химиками было установлено, что монооксид углерода кардинальным образом меняет свойства переходных металлов, связываясь с ними при высоком давлении в комплексное соединение - карбонил.
В данном случае, металл не окисляется, как происходит при образовании солей, а остаётся нейтральным атомом, который образует с молекулой CO (лигандом) координационную связь по механизму обратного донирования (т. е. сначала атом металла приобретает эффективный положительный заряд, а затем происходит обратный перенос электронной плотности с лиганда на металл).
Благодаря этому карбонилы металлов обладают совершенно уникальными свойствами, которые не характерны ни для чистых металлов, ни для их солей. При нормальных условиях карбонилы переходных металлов объединяет свойство с лёгкостью улетучиваться.
Это могут быть и жидкости (пентакарбонил железа) и твёрдые кристаллы, склонные к сублимации (гексакарбонил хрома). Карбонилы металлов, как правило плохо растворяются в воде и хорошо растворимы в органических растворителях, таких как диэтиловый эфир, ацетон и бензол). На данный момент из всех переходных металлов чистыми карбонилами не обладают лишь титан, цирконий, гафний, ниобий и тантал, а карбонилы палладия, платины, меди, серебра и золота могут существовать лишь в низкотемпературной инертной среде.
Среди всех карбонилов наиболее мягкие условия для синтеза присущи тетракарбонилу никеля: соединение можно получить при атмосферном давлении, пропуская угарный газ в среде без доступа воздуха через мелкодисперсный никель при температуре 80°С. Карбонилы других металлов требуют более жёстких условий или сложных химических реакций.
Хранят карбонилы также в закупоренном виде; во-первых, даже при комнатной температуре на воздухе многие соединения разлагаются, а во-вторых, карбонилы металлов являются сильнейшими токсинами неорганического происхождения. Из-за своей летучести и хорошей растворимости в жирах карбонилы способны попадать в организм даже через кожу, поэтому при работе с ними требуется соблюдать предельную осторожность. Опасность для организма представляет как образующиеся частицы тяжёлых металлов, так и высвобождаемый угарный газ, который при попадании в кровь карбонилирует гемоглобин в карбоксигемоглобин, неспособный связывать кислород, что приводит к патологическим изменениям в легких и повреждению других органов.
Для сравнения, предельно допустимая концентрация паров тетракарбонила никеля в рабочей зоне составляет 0,0005 мг/м³, что в 10 раз меньше концентрации паров ртути и в 20 раз меньше концентрации паров таллия в аналогичных условиях.
Но несмотря на такую опасность карбонилы не имеют себе аналогов во многих отраслях.
Так, выделение металла при разложении карбонила это способ получить сверхчистый нанопродукт, который в дальнейшем может быть использован в других химических реакциях, при катализе или в качестве тонкого металлического покрытия. Нередко в качестве катализаторов используют и сами карбонилы (например при синтезе карбоновых кислот). Высвобождаемый угарный газ также может быть использован в карбонилировании органических соединений.
Из-за неустойчивости связи M-CO, карбонилы могут вступать в реакции замещения лигандов, что открывает безграничные возможности в области металлоорганических соединений. Однако замещать CO могут не только лиганды, но и неорганические анионы, что позволяет получать уже комплексные соли. Следует ещё добавить, что карбонилы весьма чувствительны к свету и под действием фотолиза способный образовывать новые структуры.
Иными словами, эти соединения являются исходным реагентом во многих областях химии и могут быть использованы в самых разных технологиях. Подробнее о карбонилах каждого металла и их применении будет рассказано в следующих постах...
Все материалы также публикуются на странице ВК: vk.com/mircenall










Лига Химиков
1.9K постов12.9K подписчика
Правила сообщества
Старайтесь выбирать качественный контент и не ставьте теги моё на копипасты
Посты с просьбой решения домашнего задания переносятся в общую ленту
Также нельзя:
1. Оскорблять пользователей.
2. Постить материал далеко не по теме и непотребный контент (в остальном грамотно используйте теги)
3. Рекламировать сомнительные сайты и услуги коммерческого характера