Наши внутренние войска: есть ли жизнь после тимуса?
В прошлом посте я рассказал, как получаются Т-лимфоциты и какой серьезный отбор они проходят. Что же происходит с этими клетками дальше?
Несколько Т-киллеров атакуют раковую клетку и образуют с ней разрушительный контакт, который поэтично называют “поцелуй смерти”. Киллеры выделяют цитотоксические вещества для уничтожения врага.
Жизнь вне тимуса
Итак, тимус покидают зрелые Т-лимфоциты: киллеры и хелперы. Однако эти солдаты ещё не нюхали пороху, они не знают, что такое настоящий антиген (тимоциты контактировали только с антигенами своих тканей). Поэтому их называют наивными лимфоцитами. С током крови эти наивные юнцы поступают во все периферические органы иммунной системы (о которых был отдельный пост).
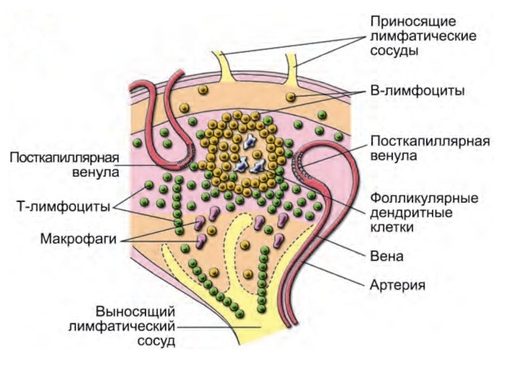
Строение лимфатического узла.
Наши лимфоцитарные бойцы распределяются по разным военным частям. Одна из таких частей представлена лимфатическими узлами. Эти небольшие скопления лимфоидной ткани раскиданы по всему организму. Сюда поступают зрелые, но наивные Т- и В-лимфоциты. Именно здесь, в лимфоузле, они готовятся исполнить свое предназначение. Через лимфоузел проходит лимфа, которая омывает ближайшие ткани и захватывает всё подозрительное, что там есть. Основные регионы скопления лимфатических узлов представлены на картинке ниже.
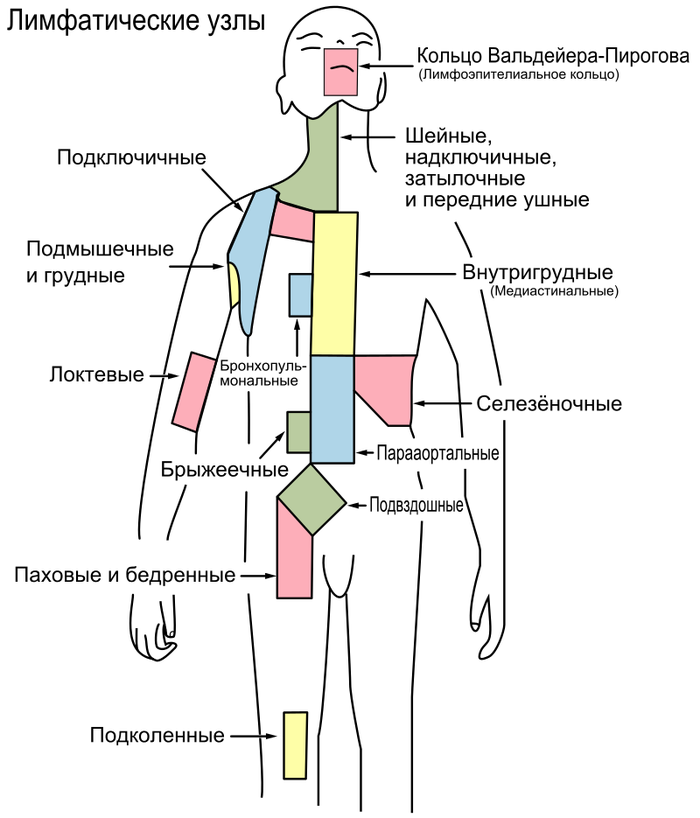
Группы лимфатических узлов (ресурс).
В лимфатических узлах также присутствуют макрофаги и дендритные клетки, которые приносят антигены наивным лимфоцитам. Здесь лимфа очищается от антигенов и всего чужого, что она принесла с собой. И здесь же происходит дальнейшее созревание лимфоцитов. Как только новоиспеченный киллер или хелпер столкнулся со своим единственным антигеном, он активируется и начинает делиться. Активированные лимфоциты называются эффекторными клетками (потому что они производят некоторый эффект). Из лимфоузла активированные лейкоциты перемещаются к воспалительному очагу и реализуют там свои биологические функции.
Т-хелперы
Т-киллеры - это только половина из Т-лимфоцитов, покинувших свою свою альма-матер. Вторую половину составляют Т-хелперы. Если быть точнее, хелперов чуть больше половины, а киллеров - немного меньше.
Но зачем нужны хелперы? Возможно у вас уже мелькнула догадка: хм, help - означает “помогать”, следовательно, эти лимфоциты в чем-то кому-то помогают. И ваша догадка верна, Шерлок! Т-хелперы, несущие на своей поверхности маркер (белок) CD4, поддерживают и регулируют иммунитет, воздействуя на его разные звенья. Сами хелперы не участвуют в уничтожении своих клеток или микробов, но помогают это делать другим. Они эдакие политруки, мотиваторы и вдохновители иммунных клеток. Хелперы выполняют свои функции, выделяя различные сигнальные молекулы. Как только началась война за жизнь и здоровье нашего организма, отовсюду слышится крик Т-хелперов:
Вперед, за родину! Отступать некуда! Ты, макрофаг, ну-ка съел вон ту бактерию, а ты, нейтрофил, ему помоги! Эй, Т-киллер, во имя всего святого, пойди уничтожь эту подозрительную клетку, внутри неё какие-то неправильные белки! Аллё, эозинофил, чего заснул? Гляди, там глист прополз - атакуй его! B-лимфоциты, ну-ка, навели на цель орудия и выпустили антитела!.. Всё-всё, ребята, тише, пора заканчивать обстрел, враг уничтожен! Время зализывать раны.
Изначально CD4-клетки делили на два вида (субпопуляции): Т-хелперы 1 и Т-хелперы 2. Однако вскоре этот репертуар значительно расширился. Для краткости их стали обозначать Th1, Th2, Th3, Th9 и так далее. Вначале нумерация шла просто по порядку, но в дальнейшем число стало обозначать, какое вещество выделяет тот или иной хелпер.
Если вы помните, я периодически упоминал цитокины - вещества белковой природы, которые клетки выделяют для общения друг с другом. Эдакие биологические смс-ки. Цитокины, которые выделяют лейкоциты, называют интерлейкинами. К примеру, хелпер Th17 выделяет интерлейкин-17 и ряд других веществ, которые активируют нейтрофилы для защиты эпителиальных барьеров (эпителий - это ткань, контактирующая с внешней средой). Разбирать каждый вид хелперов мы не будем (ибо вы проклянете меня), но несколько основных типов рассмотрим. А для наглядности ниже приведу таблицу.
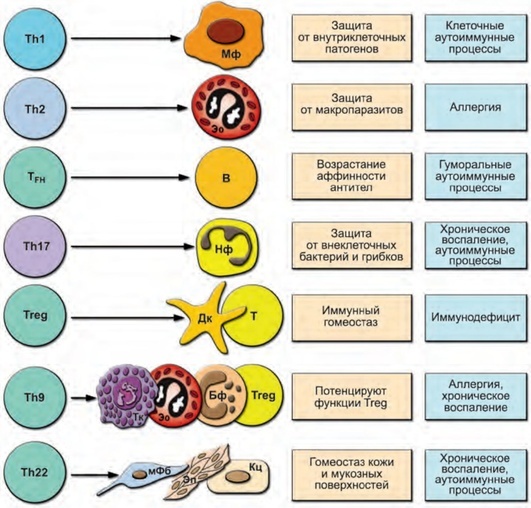
Таблица “На что какой хелпер влияет”. Справа от стрелки показаны клетки, на которые влияет хелпер. В оранжевой табличке - физиологические эффекты хелпера. Рядом в синем квадратике указан основной патологический процесс, развивающийся вследствие дисфункции данного класса хелперов.
Расшифровка: Мф - макрофаг; Эо - эозинофил; Нф - нейтрофил; Дк - дендритная клетка; Т - Т-лимфоциты; Тк - тучная клетка; Бф - базофил; Кц - кератиноцит (клетка кожи); мФб - миофибробласт (заживляет и стягивает края раны); Эп - эпителий (клетки слизистых оболочек).
Th1 лимфоциты обеспечивают клеточный иммунитет. Они выделяют ряд интерлейкинов, которые стимулируют различные клетки. Выделяя фактор некроза опухоли (ФНО-b), Th1 активируют воспалительные макрофаги. Кроме того, хелперы выделяют цитокины, необходимые для эффективной работы Т-киллеров. Дело в том, что недостаточно только показать антиген Т-киллерам. Этим прихотливым клеткам нужны ещё и дополнительные стимулы, которые может послать или дендритная клетка, или хелперы. Поэтому Th1 выделяют костимулирующие факторы, необходимые для максимальной экспансии киллеров.
Например, интерлейкин-2 стимулирует созревание клонов лимфоцитов, а также активирует работу нейтрофилов и моноцитов. Интерлейкин-2 необходим для полноценной активации Т-киллеров. Настолько этот стимулятор хорош, что существует его лекарственный аналог, который применяется для лечения иммунодефицитных состояний.
Также Th1 выделяют интерферон-гамма, который, как и другие интерфероны, тормозит размножение вирусов и предотвращает заражение здоровых клеток. А ещё эти хелперы стимулируют B-лимфоциты к продукции антител, а именно - IgG (иммуноглобулин G).
Т-киллеры, связавшиеся с дендритной клеткой, активируются после помощи Т-хелперов.
Th2 лимфоциты выделяют несколько разных интерлейкинов (ИЛ-4, ИЛ-5, ИЛ-6, ИЛ-10 и ИЛ-13). Этот тип лейкоцитов активирует B-лимфоциты и способствует выработке антител разных классов, особенно IgE (да-да, антитела тоже бывают разные). Также хелперы этого класса активируют эозинофилы и базофилы. Тандем IgE и эозинофилов играет важную роль в противоглистном иммунитете. IgE и базофилы виноваты в различных аллергических реакциях, таких как аллергические астма и ринит, пищевая аллергия и другие. Основная активность этих хелперов происходит вблизи эпителиальных барьеров ЖКТ и легких.
И ещё один тип CD4-клеток, о котором нужно бы упомянуть - Т-регуляторы (Th-reg). Это тоже подвид хелперов, который раньше выделяли в отдельный вид и называли супрессорами. Задача этого класса - регулировать иммунный ответ, не позволяя военной ярости погубить весь организм. Они выделяют интерлейкин-10, который снижает активность киллеров и макрофагов, а также подавляет высвобождение разных воспалительных веществ (интерфероны, фактор некроза опухоли и другие интерлейкины). С другой стороны, ИЛ-10 увеличивает выживаемость B-лимфоцитов и стимулирует продукцию антител, а также созревание новых тимоцитов. Другое вещество, трансформирующий фактор роста b (ТФРb), также подавляет иммунные реакции. К сожалению, некоторые злокачественные опухоли тоже “научились” вырабатывать этот фактор.
Но почему природе понадобилось “придумывать” такой сложный механизм защиты в виде посредников-хелперов. Хорошо, мы ещё можем понять, зачем нужны регуляторы - чтобы прекратить иммунный ответ. Но Th1 и Th2? Наличие хелперов помогает более тонко настроить иммунный ответ. Слишком агрессивный иммунитет будет успешно бороться с большинством инфекций, но и с большой долей вероятности атакует свои же клетки. Слабый же иммунитет не тронет своего хозяина, но и пропустит какой-то микроб. Кроме того, хелперы могут прицельно переключать иммунитет на какой-то конкретный тип возбудителя (например, на вирусный или бактериальный).
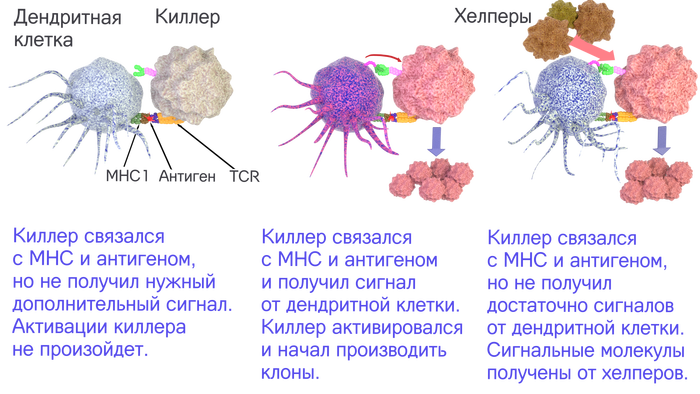
Сначала чужеродное вещество должна распознать, например, дендритная клетка. Затем она покажет это вещество Т-киллеру и Т-хелперу. Даже если киллеры не активировались в силу каких-то причин, то активированные хелперы простимулируют наивных киллеров, и те с большей долей вероятности распознают чужеродный антиген. Поэтому для эффективного иммунного ответа нам очень нужны хелперы, они способствуют активации клеточного (киллеры, макрофаги) и гуморального (антитела) иммунитетов.
Варианты взаимодействия хелперов и киллеров.
Иммунорегуляторный индекс и ВИЧ
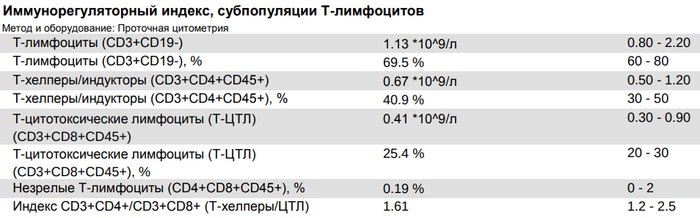
В норме в крови человека содержится 30-50 % CD4 клеток (хелперов) и 20-25 % CD8 клеток (киллеров). Как видите, хелперов больше, но и репертуар их значительно разнообразнее (Th1, Th2, Th17 ...). Соотношение CD4 к CD8 всегда больше единицы и в норме составляет 1,2 - 2,5. Например, если хелперов - 50%, а киллеров - 25%, то соотношение будет 2 (50/25). Эту пропорцию называют индексом регуляции или иммунорегуляторным индексом (CD4/CD8 ratio). Данный показатель увеличивается в начале и в разгаре болезни, так как возрастает количество хелперов. В период выздоровления индекс уменьшается за счет возрастания Т-киллеров. Появилось много киллеров - значит, иммунная система распознала антиген и наплодила CD8 лимфоциты, которые атакуют инфицированные клетки. Но даже во время инфекционного процесса этот индекс не бывает значительно ниже единицы. Снижение соотношения означает состояние иммунодефицита - организму не хватает хелперов для обеспечения эффективной защиты.
Пример иммунограммы с просторов инета. Здесь всё в порядке.
И несколько слов о ВИЧ инфекции. Конечно, эта болезнь требует написания отдельного поста, но в рамках данной темы все же рискну написать ещё один абзац :) Для проникновения вируса в клетку ему необходим специфический рецептор, связавшись с которым, подлый микроб проникает внутрь клетки (более подробно написал здесь). Для вируса иммунодефицита таким рецептором является CD4 белок. Смекаете, в чем дело? Вирус поражает клетки, на поверхности которых находится CD4 рецептор, а это как раз и есть наши хелперы. Знает, куда метить, проклятый враг! В результате вирус-специфичных иммунных механизмов происходит массовая гибель Т-хелперов, и организм утрачивает способность эффективно бороться с инфекциями и опухолями. Когда уровень CD4 падает настолько, что любая “простая” инфекция вызывает тяжелое заболевание, наступает фаза СПИД-а - синдром приобретенного иммунодефицита. Иммунорегуляторный индекс при этом ниже единицы. Кстати, CD4 рецепторы присутствуют и на моноцитах и макрофагах - эти клетки также инфицируются вирусом, но живут гораздо дольше хелперов.
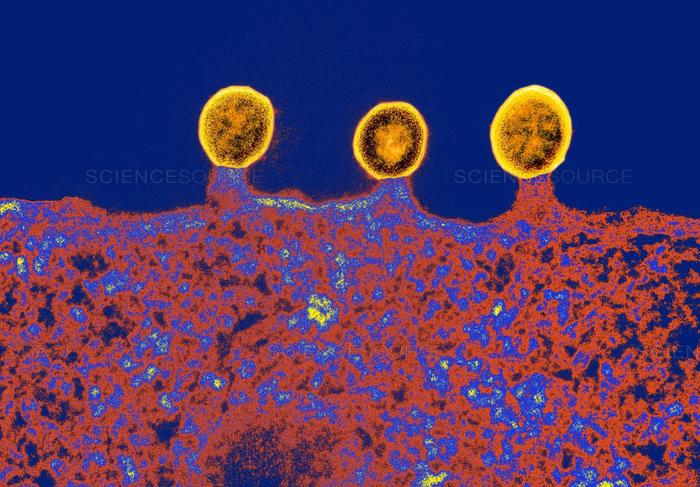
Вирусы иммунодефицита человека (желтые) на поверхности хелпера.
Итак, Т-лимфоциты бывают разных типов: киллеры и хелперы. Хелперы нужны для более тонкой настройки иммунитета и регуляции его интенсивности. После созревания в тимусе Т-лимфоциты с током крови попадают во вторичные иммунные органы (лимфоузлы, селезенку и другие). Во вторичных органах происходит встреча лимфоцитов с чужеродными антигенами. Th1 обеспечивают иммунитет для борьбы с внутриклеточными паразитами, Th2 - внеклеточными. Чрезмерные “старания” Th1 приводят к воспалительному поражению клеток, а Th2 - к аллергическим реакциям. Th1 и Th2 антагонистически влияют друг на друга, то есть активация первых подавляет вторые и наоборот.
В следующем посте я расскажу о других иммунных клетках, которые помогают нам в борьбе за выживание. Всем отличного настроения и нормального CD4/CD8 ratio!