«Зомби-клетки» внутри нас
В вашем теле живут клетки-зомби. Они не совсем мёртвые. Такие клетки скорее живые, но они больше не делятся и могут свою «зомби-сущность» передавать соседям. И соседние клетки тоже превращаются в зомби! Зомби-клетки повышают риск рака и разных других заболеваний — например, артеросклероза. Сейчас учёные активно думают о том, как от таких клеток избавиться. Однако есть нюанс: наши внутренние «зомби» выполняют и полезные функции.
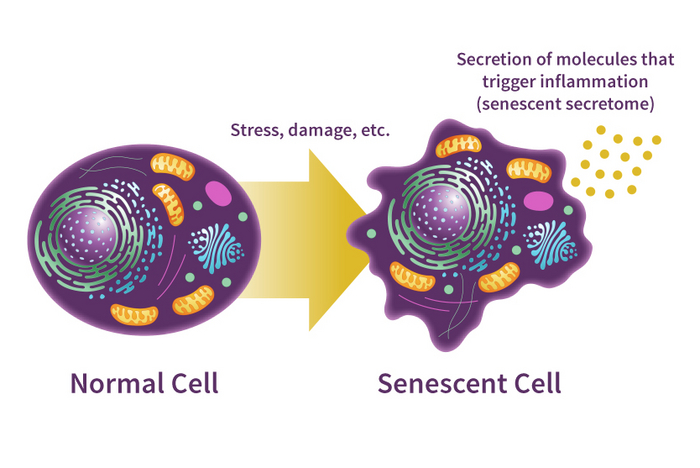
Учёные называют «зомби» сенесцентными клетками. И накопление этого типа клеток в нашем организме — очень важный элемент человеческого старения. Говоря простым языком, сенесцентные клетки — это клетки, которые ранее обладали способностью делиться, но из-за накопления разных повреждений делиться больше не могут. Обычно количество «зомби» с возрастом увеличивается. Из-за этого появляются разные старческие заболевания, возникает боль в суставах, нарушения когнитивных функций, системные воспаления и так далее.
Откуда в нашем теле берутся сенесцентные клетки? Это точно не старые клетки — некоторые «зомби» образуются ещё на стадии эмбрионального развития. Чаще всего сенесцентные клетки, вызывающие заболевания, появляются из-за ошибок, мутаций в ДНК и иных повреждений. Клетка, в которой накопилось много повреждений, выходит из клеточного цикла и как бы говорит: «Всё, я дальше делиться не буду». А ещё «зомби» сигнализируют о своём состоянии иммунной системе, выбрасывая провоспалительные факторы. На эти факторы «приходит» иммунная система и некоторые сенесцентные клетки утилизирует.
Ещё «зомби» могут образовываться из-за повышенной активности отдельных генов. Например, когда клетка подозревает, что может стать раковой, она превращается в сенесцентную. И это хорошо! А сейчас приведу пример, который всем понятен — родинки. Наверняка мои читатели слышали про меланому — рак кожи. Родинки — это не меланома, но в родинках клетки начинают очень активно делиться. Затем в них включается механизм сенесценции — и они делиться перестают. И родинка оказывается «зафиксированной» в своём размере и не превращается в раковую опухоль.
Важно сказать, что сенесцентные клетки могут быть очень разными как по происхождению, так и по свойствам. Поэтому некоторые учёные очень скептично относятся к термину «сенесцентные клетки» — ведь не всегда понятно, какие именно клетки имеются в виду. Интуитивно может показаться, что, раз клетка перестала делиться, значит, в ней что-то сломалось. Но на самом деле «зомби» — это клетки, в которых сработал специальный и целенаправленный механизм, который ограничивает клеточное деление. Так задумано — это не случайная поломка. Это, скорее всего, специальная «поломка» ради предотвращения онкологического заболевания.
Когда клетка сильно повреждается и не может эти повреждения исправить, у неё есть две опции. Первая — запрограммированная клеточная смерть, самоубийство клетки или апоптоз. Вторая — превращение в «зомби». Во втором случае клетка выживает, но перестаёт делиться.
Перед тем как выбрать одну из двух опций клетка пытается себя починить. Когда в клетке повреждается ДНК, включается огромное количество механизмов «репарации». Активируются разные белки, которые пытаются это дело исправить. Однако, если ошибку устранить не получается, клетке приходится выбирать одну из двух упомянутых опций.
Существует по меньшей мере четыре вида сенесценции:
Репликативное старение. У большинства клеток есть встроенный ограничитель делений — предел Хейфлика. При каждом делении кончики хромосом — теломеры — укорачиваются. И через 40-60 делений клетка перестаёт делиться — это и есть репликативное старение. Это старение особенно распространено у крупных видов животных — в частности, у человека;
Сенестенция, вызванная стрессом. Здесь речь идёт не о депрессии, а о том, что клетка может повреждаться из-за ультрафиолетового излучения, ионизирующей радиации, активных форм кислорода и так далее. В результате клетка перестаёт делиться;
Сенесценция, вызванная онкогенами. Онкогены — это гены, чья повышенная активность увеличивает риск рака. Если клетка «замечает» онкогены, то перестаёт делиться;
Сенесценция эмбрионального развития. У человека есть разные эмбриональные структуры, которые не должны чересчур разрастись в утробе. А некоторые структуры даже должны исчезнуть совсем — например, плавники и хвостик у зародыша. Благодаря сенесцентному механизму младенцы появляются на свет без хвоста!
В общем, сенесценция — это довольно нужно и важно. И всё же есть учёные, которые называют сенесцентные клетки «зомби» и считают, что от некоторых из них нужно избавляться — чтобы победить старение.
Итак, у сенесценции есть плюсы и минусы. Сначала расскажу о плюсах. Благодаря «зомби» организм предотвращает появление некоторых онкологических заболеваний. Учёные создавали ГМ-животных с отключенным геном p16. p16 — один из ключевых генов, запускающих сенесцентность. В результате подопытные массово страдали от рака. То есть полностью сенесценцию отключать нельзя! Кроме того, учёные выяснили, что «зомби» иногда помогают регенерировать ткани кожи и мышц. А сенесценция клеток поджелудочной железы может увеличивать выработку инсулина. Сенесценция же клеток печени предотвращает цирроз. В общем, «зомби» делают массу всего полезного. Кстати, такие «зомби» встречаются даже у сверхдолгожителей — голых землекопов.
При этом сенесцентные клетки обладают и рядом «недостатков». Так, с возрастом в нашем теле накапливается очень много «зомби». Особенно опасны клетки, ставшие «зомби» из-за повреждений в ДНК. Они начинают производить молекулы, которые могут вызывать хронические воспаления в тканях вокруг. Так, есть очень важная провоспалительная молекула — интерлейкин-6. Она нужна для коммуникации клеток между собой. Интерлейкин-6 активирует высокую температуру при заболеваниях, влияет на исход некоторых видов рака... Когда клетки перестают делиться из-за сенесценции, порой они начинают производить в 40 раз больше интерлейкина-6. От этого могут повреждаться соседние клетки — и у них тоже включается сенесценция. Происходит цепная реакция.
И ещё один момент: в нашем теле есть «спящие» эндогенные вирусы, которые изначально встроены в наш геном. Они попали туда в ходе эволюции и зашифрованы прямо в нашей ДНК. Так вот, в норме особые клеточные механизмы подавляют вирусы и не дают им сделать ничего плохого. Однако, как показало недавнее исследование, «зомби» не подавляют такие эндогенные вирусы. И в итоге клетка собирает из своего же генома вирусные частицы и заражает ими здоровые клетки. Заражённые клетки, в свою очередь, тоже становятся сенесцентными. Но всё не так плохо: авторы упомянутого исследования создали антитела против вирусных частиц — и остановили заражение.
Но всё же сенесцентные клетки опасны в первую очередь из-за хронического воспаления, которое они вызывают. Инфекции в организме нет, а воспаление есть. И иммунитет борется, по сути, с самим организмом. В итоге из-за хронического системного воспаления возникают артрит, атеросклероз и прочие неприятные «старческие» заболевания. Иногда из-за воспаления возникает рак, деменция, болезнь почек, депрессия. А ещё выраженность системного хронического воспаления очень неплохо предсказывает вероятности смерти человека.
Откуда мы знаем, что сенесцентные клетки существуют и работают? Надо признать: есть учёные, которые скептически относятся к концепции сенесцентных клеток. Как минимум потому, что «зомби» трудно дать точное определение — уж очень разными они бывают. Но одна команда исследователей провела эксперимент, показавший «работоспособность» сенесцентных клеток. Итак, учёные взяли клетки эпителия в предраковом состоянии — в них уже «назрели» мутации, вызывающие рак. Потом эти предраковые клетки исследователи смешали либо с сенесцентными клетками, либо с обычными, несенесцентными, которые могут делиться. А дальше ввели и первую, и вторую смесь подопытным грызунам. Оказалось, что при введении смеси из предраковых и сенесцентных клеток повышается и риск появления рака, и скорость роста опухоли. А при введении другой смеси — с нормальными клетками — таких страшных последствий не наблюдалось.
Считается, что рак — это результат мутаций в клетках. Но на самом деле на успешность и активность раковой клетки влияют ещё и соседние клетки. И если рядом с потенциально мутантной раковой клеткой находятся сенесцентные клетки, шанс развития рака повышается.
Другая команда учёных поставила ещё один опыт — взяла свиные клетки и превратила часть из них с помощью радиации в сенесцентные. Затем и нормальные клетки, и «зомби» исследователи перенесли в почки молодых мышей. Выяснилось, что из-за сенесцентных клеток у грызунов начали возникать фиброзы, воспаления и различные повреждения почек. Похожий опыт провела ещё одна группа учёных: они брали из жировой ткани мышек как сенесцентные, так и нормальные клетки, которые способны делиться. Далее специалисты понемногу пересаживали клетки другим грызунам. Выяснилось, что мышки, которым подсаживали «зомби-клетки», начали проявлять признаки старения — они хуже бегали, становились слабее. Чем больше грызун получал сенесцентных клеток, тем дряхлее он становился. В ходе эксперимента учёные выяснили, что 1 сенесцентная клетка на 10 000 нормальных примерно в 5 раз увеличивает риск смерти.
Что же делать — избавляться от «зомби» или нет? Видимо, надо оставить механизм сенесценции в покое — но при этом можно устранять уже получившиеся «зомби» по мере их накопления. Как это сделать? Наши гены должны активироваться в определённых условиях. Поэтому у каждого гена есть регуляторный участок, который «говорит», где именно и в каких условиях ген будет работать (пример такого участка — промотор, который находится перед началом гена и показывает, с какого места его «считывать»). Так мы можем «подсмотреть», какие гены активируются в сенесцентных клетках. В общем, учёные выяснили, что у существенной части сенесцентных клеток их сенесцентность запускалась уже упомянутым геном p16. У p16, как и у любого другого гена, есть промотор — вот его-то и можно «приделать» к другому гену. Тогда при «запуске» p16 параллельно запустится и тот второй ген. А теперь фокус: приклеиваем промотор p16 к гену, который запускает запрограммированную смерть клетки! Тогда в момент, когда клетка по какой-то причине «решит» стать сенесцентной, она тут же себя и убьёт.
А можно пойти ещё более хитрым путём. Например, сделать так, чтобы наш дополнительный ген, к которому мы приклеили промотор от p16, срабатывал бы только при наличии синтетического вещества, которого не бывает в организме человека. То есть, когда мышке или человеку вводят это секретное вещество, все клетки, где активен p16, убьются. Так исчезнут клетки с повреждённой ДНК, которые больше не делятся. Но будет ли такая «зачистка» полезна для здоровья?
Учёные выяснили, что да, «зачистка» скорее полезна. Исследователи в ходе своего эксперимента удаляли сенесцентные клетки у ГМ-мышей — и продолжительность жизни грызунов немного выросла! При этом животные выглядели моложе сверстников и были более активными, любознательными и бодрыми. Это круто — получается, удаление сенесцентных клеток поможет в борьбе со старением.
Но, увы, такая генная терапия должна происходить до рождения — а мы с вами взрослые люди, нас в эмбриональное состояние уже не вернуть. Что же нам делать? Как избавиться от вредных клеток? Хорошие новости: уже разработаны препараты — сенолитики — которые могут уничтожить некоторые типы сенесцентных клеток. По крайней мере, так показали опыты на животных. Так вот, самая известная комбинация сенолитиков — это дазатиниб и кверцетин. Дазатиниб — это вообще лекарство от рака и опухолей. А кверцетин — это природное вещество, которое достаточно часто встречается в продуктах питания. Исследования показали, что кверцетин усиливает действие дазатиниба.
Я уже описывал эксперимент, авторы которого пересаживали мышам сенесцентные клетки из жировой ткани. Так вот, в той работе учёные брали клетки у ГМ-доноров со светящимися клетками. Клетки доноров отличались от клеток реципиентов, их можно было легко увидеть под микроскопом. В ходе опыта реципиентам давали дазатиниб и кверцетин — и выяснилось, что сенолитики устраняли светящихся «зомби», но не устраняли нормальные светящиеся клетки. А ещё учёные поставили дополнительный эксперимент на старых мышах, чей возраст примерно эквивалентентен возрасту 80-летних стариков. Им давали те же дазатиниб и кверцетин. «С момента лечения продолжительность жизни мышей увеличилась на 36%», — резюмировали авторы статьи. Но на самом деле старые мышки просто чуть-чуть дольше протянули.
Другие учёные показали, что дазатиниб и кверцетин замедляют старение лёгких у мышей. А ещё одни исследователи поставили эксперимент на людях — правда, людей было всего 9, то есть выборка оказалась ничтожно мала. Тем не менее, учёные заявили, что сенолитики снизили число «зомби» в тканях. А вот как препараты повлияли на продолжительность жизни, непонятно — люди, в отличие от мышей, слишком долго живут, на них такие эксперименты ставить сложно.
Кроме микса из дазатиниба и кверцетина, существуют и другие сенолитики. Например, популярен экспериментальный препарат навитоклакс — тоже средство против рака. Вы, наверное, спросите: как противоопухолевое лекарство от рака помогает против сенесцентных клеток? Ведь раковые клетки суперактивно делятся, а «зомби» не делятся вовсе. Но у этих двух типов клеток есть нечто общее — у них постоянно включены «сигналы об ошибке», о повреждениях. Правда, «зомби» в ответ на сигнал перестают делиться, а раковые клетки сигнал игнорируют и очень активно делятся.
В одной работе учёные исследовали сенесцентные клетки в сердцах грызунов. Да-да, в сердце тоже могут появляться «зомби» — это приводит к фиброзу и гипертрофии сердца, что увеличивает риск внезапной смерти. В общем, учёные вызывали инфаркт у мышей. И выяснили, что старые 23-месячные грызуны, которым ранее давали навитоклакс, выздоравливали после инфаркта как 3-месячные мышки. Это как если бы 70-летний старик отошёл от инфаркта как подросток.
К сожалению, у сенолитиков есть побочные эффекты — в частности, малоприятный кашель с кровью. А теперь — к хорошим новостям:
Для борьбы с «зомби» нужны не такие высокие дозировки, как для борьбы с раком;
Сенолитики можно принимать не постоянно, а курсами: попил, а потом дальше живёшь и «копишь» своих «зомби» лет 10-20;
Есть такой сенолитик — квертицин — который идёт в комбо с дазатинибом и почти не имеет побочек. Сам по себе это флавоноид, которого много в разных фруктах и овощах, особенно в каперсах. Правда, есть овощи ради кверцитина бесполезно: чтобы получить нужное количество вещества, придётся есть по полкило каперсов в день. Что делает кверцитин? Он подавляет белок, который не даёт клетке убить себя, говорит ей «Живи!» Грубо говоря, этот белок как психотерапевт. А кверцитин приходит и убивает психотерапевта, а клетка такая: «Всё, не хочу больше жить».
Сейчас много хайпа вокруг ещё одного сенолитика — физетина. Он тоже встречается в разных фруктах и овощах — в яблоках, огурцах, луке, винограде. Биохакеры очень любят кушать физетин! Но есть нюанс. Существует научная программа тестирования интервенций — Interventions Testing Program. Она беспристрастно испытывает всякие средства против старения — три разных лаборатории в США независимо тестируют предлагаемые способы на мышах, самцах и самках. В общем, согласно Interventions Testing Program, физетин жизнь не продлевает.
Но вообще, даже если физетин или другой сенолитик работает на мышах, это не значит, что он будет работать и на нас с вами. Из 100 препаратов, которые работают на грызунах, лишь 10 оказываются эффективными на людях. Так что ждём исследований сенолитиков на людях — чтобы понять, какие из них работают — и работают без серьёзных побочных эффектов.
У нас есть часть тела, где клетки вообще не делятся — это наш мозг. Да-да, нейроны делиться не умеют, а ещё они с годами могут ухудшаться и дряхлеть. У дряхлых нейронов может, например, уменьшаться объём митохондрий. А ещё стареющие нейроны могут выделять интерлейкин-6. А значит, вызывать старческое хроническое воспаление в мозге. То же самое может происходить и с клетками, которые питают и берегут нейроны — например, с астроцитами. И даже у стволовых клеток может случаться сентенция!
В общем, кажется, дела плохи: в нашем мозге, скорее всего, с возрастом настанет старческое хроническое воспаление. Кстати, были опыты, в ходе которых в мозг мышам вводили интерлейкин-6 — и это приводило к ухудшению когнитивных функций грызунов. А ещё учёные знают, что у пациентов с Паркинсоном и Альцгеймером в спинномозговой жидкости находится много противовоспалительных маркёров.
Учёные исследовали влияние сенолитиков на мозг мышей. Оказалось, что сенолитики могут избирательно устранять «сенесцентноподобные» нейроны — повреждённые нейроны, которые вызывают воспаления. И в итоге у грызунов после устранения «проблемных» нейронов улучшились когнитивные способности. Вывод тут простой: лучше потерять немного повреждённых нейронов сегодня, но предотвратить воспаление и сохранить гораздо большее количество здоровых нейронов завтра.
Но всё же пока учёные не знают точно, стоит ли избавляться от «зомби» с помощью лекарств, предназначенных для лечения рака. А ещё устранение сенесцентных клеток — не панацея от старости, ведь «зомби» — лишь один из симптомов этого неприятного процесса. У старения больше дюжины причин!
Тем не менее, обращать внимание на сенесцентные клетки важно, потому что они приводят к системным воспалениям, а такие воспаления — сильный предсказатель смертности у людей. Недаром есть исследование: у людей, которые прожили больше 110 лет, гораздо ниже уровни маркеров воспаления — таких как интерлейкин-6. И это не совпадение. Так что продолжаем изучать сенолитики!
Напоследок расскажу про недавние эксперименты на мушках-дрозофилах. Авторы работы решили объединить два метода продления жизни:
Они удаляли «зомби»;
А ещё омолаживали другие клетки организма с помощью факторов Яманаки, превращая их в стволовые — чтобы они активнее делились и восполняли удалённые дряхлые клетки.
Учёные пришли к выводу, что вместе эти два способа дали результат лучше, чем использование лишь одного метода. Это в очередной раз говорит о том, что старение — это множество разных процессов. И чтобы его победить, нужно использовать одновременно разные методы — чинить митохондрии, увеличивать число стволовых клеток и уменьшать число «зомби», удлинять теломеразу и устранять мутации. Думаю, в будущем возникнет комбинированная терапия против старения — и люди будут жить значительно дольше, чем сейчас.
Метастазам мутации не нужны
Злокачественные опухоли расселяются по телу не столько из-за особых метастазных мутаций, сколько из-за ослабления иммунитета.
Злокачественные опухоли возникают благодаря мутациям, из-за которых клетки начинают бесконтрольно делиться. Потом в них появляются другие мутации, обеспечивающие устойчивость к лекарствам. Таких дефектов в ДНК может быть не один, и не два, и не десять: недавно мы писали о том, как исследователи из Медицинского центра Чикагского университета и Геномного института в Пекине насчитали около 100 000 мутаций в опухоли размером 3,5 см в диаметре.
С другой стороны, не все генетические изменения, происходящие в раковых клетках, одинаково важны; некоторые из них ничего не дают опухоли, но зато могут пригодиться потом, когда условия изменятся (например, если одна терапевтическая схема придёт на смену другой).
Одна из самых известных и самых неприятных особенностей рака – это его способность к метастазированию: некоторые злокачественные клетки покидают первичную опухоль и отправляются блуждать по организму, чтобы сформировать где-нибудь вторичный очаг болезни. Поведение метастазных клеток – одна из самых «горячих точек» в современной биологии и медицине, мы едва ли не каждый день узнаём что-то новое, например, о том, как рак выбирает место для вторичной опухоли, как его клетки путешествуют по другим тканям и т. д.
Однако о том, что именно заставляет рак рассылать своих агентов на соседние «территории», до сих пор известно было мало. Логично было бы предположить, что и способность к метастазированию у опухолевых клеток появляется в результате каких-то специальных мутаций.
Жером Галон (Jerome Galon) и его коллеги из института INSERM и других европейских научно-исследовательских центров проанализировали генетическую активность в опухолевых образцах, взятых у 800 пациентов с колоректальным раком. Цель была в том, чтобы найти особые молекулярно-генетические факторы, которые способствовали бы метастатическому распространению злокачественных опухолей.
Среди больных, чьи клетки были взяты для анализа, были как те, у кого рак вёл себя более-менее смирно, так и те, у кого начали появляться вторичные очаги – однако, как пишут авторы работы в Science Translational Medicine, никаких мутаций, которые можно было бы однозначно связать с метастазной активностью, обнаружить не удалось.
Зато отличия были в активности некоторых генов, в частности, тех, что регулируют синтез белка, эндоцитоз и некоторые другие клеточные и иммунные процессы. (На всякий случай заметим, что изменения в активности генов могут происходить без мутационных поправок в ДНК, а просто под действием молекулярных, биохимических, физиологических механизмов – в конце концов, наши гены безо всяких мутаций умеют по-разному работать утром и вечером, в молодости и в старости, и т. д.)
Также удалось заметить, что в метастатических опухолевых образцах было сравнительно мало иммунных цитотоксических Т-лимфоцитов, чья задача – уничтожать раковые клетки. Таких Т-лимфоцитов также было мало у тех больных, у которых вторичных опухолей ещё не было, но блуждающие злокачественные клетки в крови уже появились. Связь между распространением опухоли и активностью Т-клеток удалось показать в опытах на животных: у мышей с пониженным уровнем иммунных «убийц» рак расселялся по организму быстрее.
В целом вывод можно сделать такой: у опухоли изначально есть молекулярно-генетические инструменты, которые позволяют ей колонизировать новые территории, но до поры до времени она не может себе такого позволить – из-за противораковой иммунной защиты. Однако, как только иммунитет ослабеет, злокачественные клетки отправляются в странствие.
С практической точки зрения это означает, что для предотвращения метастазов нужно не искать новые лекарства, которые работали бы против особых метастазных мутаций (таких особых мутаций, как выясняется, просто нет), а стимулировать иммунную систему, в частности, цитотоксические Т-киллеры. Считается, что иммунотерапия в онкологии в принципе может быть намного эффективнее, нежели другие методы лечения, однако у самих опухолей есть целый ряд трюков, которые позволяет им скрыться от внимания иммунной системы, и задача тех, кто занимается онкологическими проблемами, состоит как раз в том, чтобы помочь иммунитету увидеть внутреннего врага.
Автор: Кирилл Стасевич
Поиграем в бизнесменов?
Одна вакансия, два кандидата. Сможете выбрать лучшего? И так пять раз.
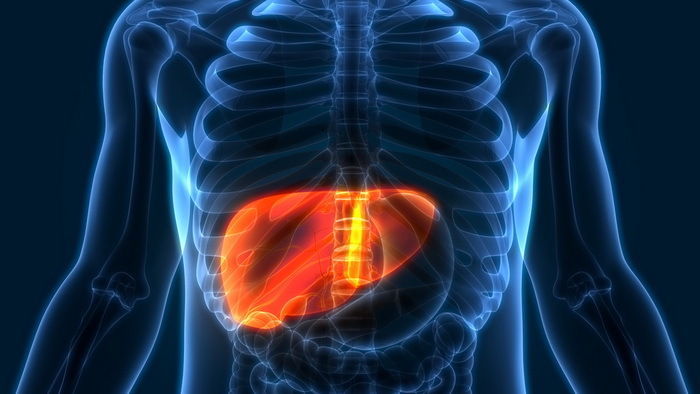
Рак портит печень на расстоянии
Молекулярные посылки, которые злокачественные клетки рассылают по телу, меняют биохимию печени, заставляя её накапливать много жира.
Злокачественную опухоль чувствует не только тот орган, в котором она выросла, её чувствует весь организм. Причина этого в разных молекулах, которые выделяют раковые клетки и которые портят жизнь другим тканям и органам. Сотрудники Корнеллского университета уже много лет изучают опухолевые молекулярные посылки и те системные эффекты, которые из-за них возникают. Посылки выглядят как крохотные мембранные пузырьки, содержащие те или иные молекулы — такие пузырьки называются экзосомы, и это обычный способ общения друг с другом самых разных клеток, не только злокачественных. В 2015 году исследователи опубликовали статью, в которой говорили, что раковые экзосомы готовят место для метастазных клеток. Молекулярная посылка адресуется конкретному органу, в который должны попасть блуждающие раковые клетки и в котором после такой посылки им проще укорениться.
В новой статье в Nature речь идёт о том, что раковые молекулярные посылки могут повредить органу без всяких метастазов. Исследователи экспериментировали с мышами, у которых был рак костей, или кожи, или молочной железы. У мышей с опухолями в какой-то момент возникали аномалии в работе печени. Однако метастазов в печени не было, она просто накапливала много жира. У мышей начиналось нечто похожее на стеатоз, или жировой гепатоз, который случается у людей с ожирением. Избыток жира провоцирует воспаление, а за воспалением начинается нарастание соединительной ткани, или фиброз. Уже сам по себе фиброз может доставить много неприятностей, потому что из-за соединительнотканных участков в печени нарушается кровообращение — соответственно, печень не может в должной мере выполнять свою работу. (А работы у неё, как известно, очень много, от обезвреживания токсинов до управления обменом веществ на уровне всего организма.) Но если фиброз будет усиливаться дальше, в конце концов всё дойдёт до цирроза.
У подопытных мышей в печени действительно сильно повышался уровень одного из белков, который указывает на воспаление, и одновременно становилось мало белка цитохрома P450, который помогает расщеплять различные токсины. Причина же была в пузырьках, которые рассылали раковые клетки и которые содержали в себе жирные кислоты, и особенно много пальмитиновой кислоты. Пальмитиновая кислота действовала на печёночные иммунные клетки макрофаги, сидящие в кровеносных сосудах, которые называются клетками Купфера. Почувствовав пальмитиновую кислоту, клетки Купфера начинали синтезировать много того самого воспалительного белка, о котором упоминалось выше, и в печени разгоралось воспаление.
При жировой болезни — то есть при жировом гепатозе — печень не только накапливает в себе жир, поступающий извне, но и сама синтезирует множество разных липидов. Возможно, раковым клеткам нравятся синтезированные печенью жиры, потому они и направляют её обмен веществ в эту сторону. Ну а то, что такая печень начинает хуже расщеплять токсины, объясняет повышенную чувствительность многих онкобольных к химиотерапии, ведь лекарства — это те же токсины, и их нужно вовремя обезвреживать. (Хотя для раковых клеток было бы выгоднее, наоборот, подстёгивать антитоксические свойства печени.)
Похожие аномалии с печенью исследователи наблюдали не только у подопытных мышей, но и у больных с опухолями, у которых в печени никаких метастазов не было. Очевидно, что полученные результаты вполне можно распространить на людей, хотя, скорее всего, у людей всё же будут какие-нибудь особенности. У мышей удалось предотвратить раковую порчу печени, заблокировав выделение молекулярных посылок из опухолевых клеток, или подавив упаковку пальмитиновой кислоты в эти посылки, или подавив синтез воспалительного белка, или же вообще убрав иммунные купферовы клетки из печени. Вопрос весь в том, какой способ подойдёт для того, чтобы использовать его в повседневной онкологической практике.
Автор: Кирилл Стасевич
РНК лекарства. Синтез нужных белков внедрением матричного РНК
Синтез белка начинается с этапа Транскрипции, когда идёт считывание информации ДНК и построение комплеменнарной ей цепочки матричной или как её называют информационной РНК. Ну а дальше идёт Трансляция- когда рибосома считывает эту информацию с цепочки матричной РНК и преообразует в цепочку аминокислот: пептидов или белков.. . Это вкратце..
Суть идеи внедрения мРНК :
Представим если организм даёт сбои, какие то процессы нарушены, синтез нужного белка идет плохо, или в недостаточном количестве, или же речь идёт в нарушении цепочки ДНК. В этом случае возможно будет внедрять в клетки созданные, нужные цепочки матричного РНК, с которых и будут считывать рибосомы информацию для синтеза нужного белка.
Белковую природу имеют многие структуры организма, ферменты, гормоны, транспортные, структурные, сигнальный... Большинство процессов в организме осуществляются белками. Поэтому нельзя переоценить пользу данного метода.
Скорее это проще чем вырезать и встраивать новые гены в ДНК. Как бы действуя в обход ДНК и стадии Транскрипции.
Возможно таким образом можно будет и усовершенствовать организм, например отправляя в клетку мРНК которая улучшит состояние тканей, придаст им нужную фическую функцию ( прочность, эластичность, устойчивость к каким либо неблагоприятных условиям). Или например применить этот метод для улучшения иммунитета когда это нужно.
Возможно таким образом можно будет омолаживать клетки организма когда, с возрастом, функции синтеза нужныхбелков, каких-либо групп клеток будут нарушены....
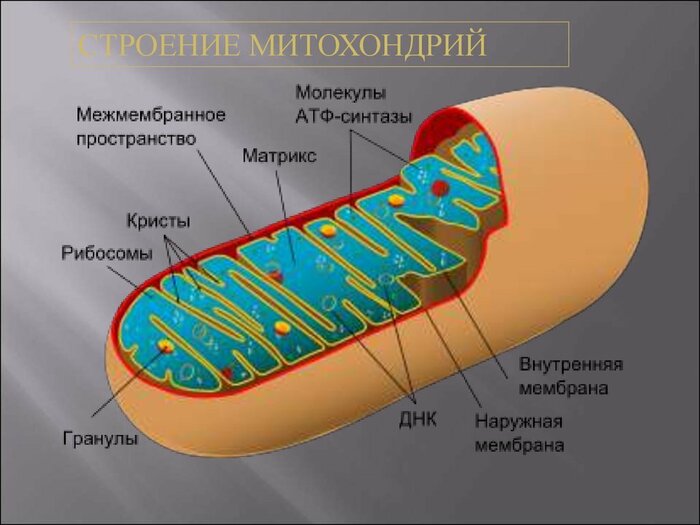
Иные Митохондрии
Этот пост про создание возможности дыхания организма, кроме кислорода и другими газами.
Митохондрии наше всё.
Бактерия в далёкие времена поселившаяся в животной клетке стала её симбионтом и обеспечила выживание животных организмом в кислородный среде. Вероятно без них и не была бы возможна жизнь многоклеточных животных организмов.
Что делает митохондрия:
Вкратце митохондрии производят АТФ используя в виде топливных молекул кислород забирая у молекул кислорода электронны.
Представьте себе если учёные выведут бактерии которые, наподобие митохондрии, могут использовать в виде топливных молекул иные молекулы вместо кислорода. Возможно не только простых молекул но и сложных.
И внедрят их в клетки организма в которых они будут сосуществовать вместе с митохондриями и начинать выполнять функцию выработки АТФ при попадании организма в чужеродную среду.
Почему это представляется возможным? : так это потому, что митохондрии от кислорода нужен только электрон, который она умеет у него забирать. А если создать органеллу которая способна брать электрон у других веществ.
Представьте себе что будут созданы такие органелы для различных сред, и будут переключаться при попадания в неблагоприятные (иные) условия.
Представьте себе в таком случае организм бы мог обходится и без скафандра в чужеродной атмосфере. И яды бы были не почем...
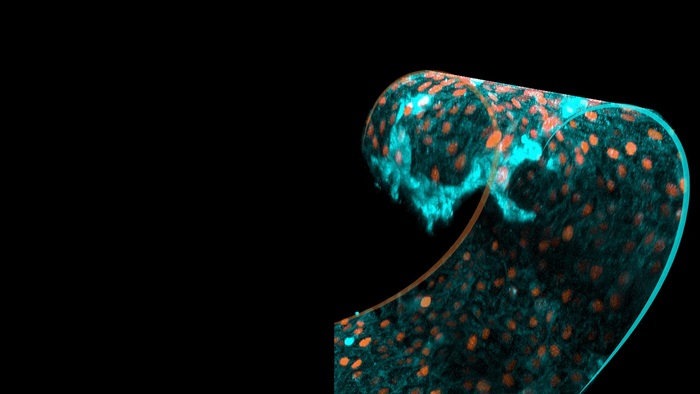
Лучшие научные снимки мая 1) Клетки, которые набухают
Молекулярные биологи обнаружили, что когда плоский лист клеток изгибается в кривую — как на этом изображении под микроскопом — клетки набухают и приобретают куполообразную форму . Исследователи говорят, что понимание того, как клетки реагируют на изгиб, может помочь в развитии органоидов — выращенных в лаборатории многоклеточных структур, которые предназначены для имитации микроанатомии органа.
Сможете найти на картинке цифру среди букв?
Справились? Тогда попробуйте пройти нашу новую игру на внимательность. Приз — награда в профиль на Пикабу: https://pikabu.ru/link/-oD8sjtmAi
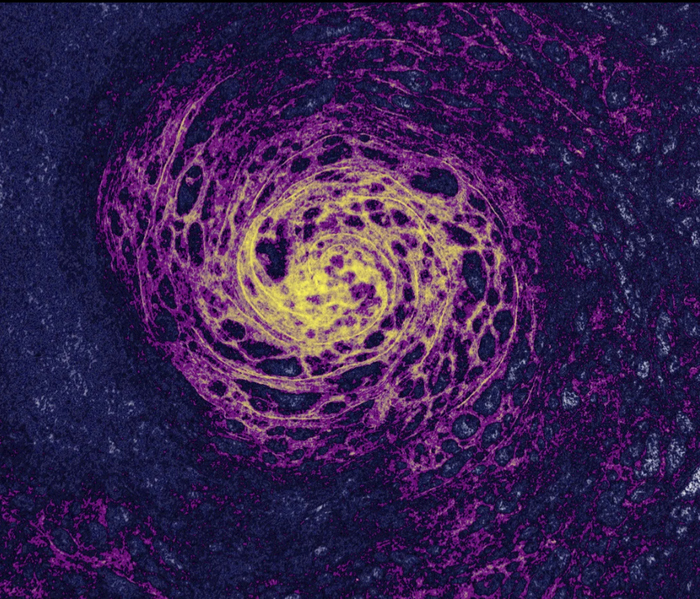
Лучшие научные снимки марта. Спиральные клетки
Это изображение клеток носа человека, полученное Кэти-Мари Кейс из Института детского здоровья Университетского колледжа Лондона на Грейт-Ормонд-стрит.
Клетки покрыты ресничками — крошечными волосками, которые улавливают и удаляют из носа инородные тела. Изучая, почему COVID-19 влияет на определенные возрастные группы больше, чем на другие, Кейс заметил, что эти галактические спирали клеток носа присутствовали только у пожилых пациентов.