Продолжение поста «Хром»5
Тут в комментариях спросили.
Дело в том, что у меня все химикаты включая оксид хрома самодельные. Поэтому данный вопрос был задан весьма уместно. Оксид хрома я получал растворяя руду с концентратом оксида хрома. Раствор кислот после растворения породы, гасил гидроксидом натрия (средство для чистки сантехнических труб). Раствор фильтровал и полученный фильтрат подкислял самодельной соляной кислотой. Соляная кислота готовилась из аккумуляторной продажной путем кипячения и добавления туда пищевой соли(хлорид натрия) до насыщения. Следствием этого в соляной кислоте присутствуют хлорид натрия (так как в серная кислота содержит воду), и сульфат натрия. Подкисленный раствор оксида хрома подвергался электролизу. В качестве электродов применял пластины из нержавейки. Соответственно при электролизе в раствор переходили ионы железа и никеля. Так же при нейтральной РН раствора( делал электролиз и при РН6-7) выпадали соли меди и гидроксида железа.
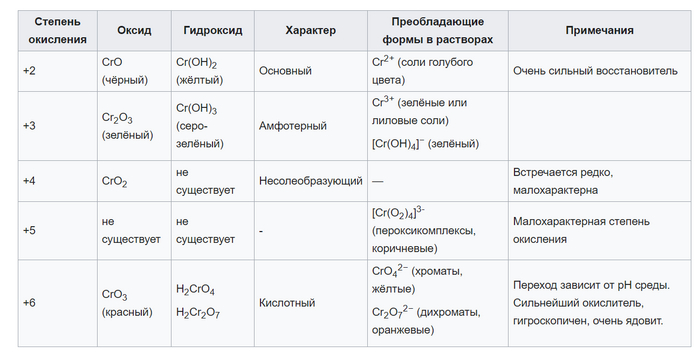
В процессе электролиза подкисленного раствора оксида хрома выделяющийся хром частично выпадал в раствор в виде осадка хрома(VI), а часть растворяясь возвращалась в раствор в виде хрома(III). Вот этот раствор с пере-растворившимся оксидом хрома(III) я и использовал для получения оксида хрома (IV). Раствор после электролиза был профильтрован от осадка хрома(VI). Полученный раствор подогрел до закипания и добавил туда сульфат железа (II). Сульфат железа(II) был получен растворением железа в аккумуляторной продажной кислоте(H2SO4) и представлял из себя зеленоватые полупрозрачные кристаллы. Выпал желтого вида осадок, возможно оксида хрома(IV). Заподозрив что выпавший осадок это возможно реакция с моей соляной кислотой и ее содержимым, я взял немного отфильтрованного осадка после электролиза оксида хрома (VI) и растворив его в своей кислоте добавил туда при кипении раствора сульфат железа(II). Но ничего не произошло, кипячение раствора никак не повлияло на раствор и никакого осадка не выпало, возможно причина в повышенной кислотности раствора, как то не подумал и не перепроверил это..
Тогда я взял отфильтрованный раствор, после электролиза, с растворенным в нем оксидом хрома(III) и повторил выделения из него оксида хрома(IV) и осадок выпал, желтого цвета как я думаю оксида хрома(IV).
Возможно, что на получения осадка в виде желтой соли, предположительно оксида хрома(IV), повлияли ионы никеля. Но данный опыт можно повторить имея доступ к Х,Ч, реактивам. Сама процедура не займет и получаса вместе с мытьем посуды. У меня нет доступа к реактивам да я и не хочу тратится и так эта химия мне в копеечку влетает, а зарплата у меня одна и не резиновая.
А так все логично получается. Оксид хрома(III) + сульфат железа(II) + кипячение= оксид хрома(IV) + сульфат железа(I) = Оксид хрома(IV) + сульфат железа(I) + прокаливание до красна газовой горелкой = оксид хрома(V) + сульфат железа(0) = Оксид хрома(V) + соляная кислота + кипячение = .........= раствор с оксидом (хлоридом - сульфатом) хрома + гидроксид натрия = оксид хрома(VI).
Вот как то так.