Химия мозга. Дубынин Вячеслав
Медиаторы. Глицин, кофеин, наркотики.
Это повтор. Но думаю, что многие не видели и будет интересно. Залипательно и познавательно.
Группа вк: https://vk.com/club74058720
Сыворотка правды. Расскажете, что угодно!
Действительно, что угодно. То есть - что пожелаете. То есть - не работают никакие "сыворотки" никакой правды. Давайте пару слов про эту магию, что ли...
Человек умеет врать (говорить неправду), это - общеизвестный факт. Да чего уж там человек, даже братья наши меньшие умеют (есть масса интересных экспериментов с обезьянками). И разумеется, у многих есть большой соблазн "принудить" человека к правде. В первую очередь это касается всевозможных спецслужб. В книжках разного уровня художественности то и дело попадаются эпизоды, как в застенках КГБ/ФСБ/ЦРУ/МИ6/Моссада человеку на допросе вводят сыворотку правды (чаще всего звучат названия "скополамин" или "пентотал"). И человек, конечно, не может теперь не соврать. Или - конечно же, это ещё надёжнее! - магия, как у Джоан Роулинг или Даниэля Дессана. В воображении волшебствующих авторов это выглядит примерно так (смотреть с 1:50, не нашла идеально вырезанного фрагмента):
В реальности - ничего подобного. Нет. Ноу. Найн. Даже не надейтесь, коварные спецслужбы, хитрые маги и проч. Вот вам правда. "Сыворотки правды" могут воздействовать на процессы торможения, и при этом человеку несколько труднее запускать сложное мышление (а придумывание лжи - это очень сложный в физиологическом смысле акт). Но сыворотки не отнимают у человека этой способности в принципе. А самое главное - они просто дают некоторое ощущение расслабленности и комфорта. Иными словами, если вы хотели наврать всем и каждому, что вчера видели прилёт летающей тарелки с марсианами, то после применения "сыворотки правды" вы получите лишь больше удовольствия от такой фантазии правдивой истории и будете охотнее ею делиться. Хотя она, возможно, станет несколько беднее на подробности, но это уже детали.
Пентотал (а точнее - пентотал натрия, а ещё точнее это вещество называется тиопентал натрия) - препарат, работающий с системой гамма-аминомасляной кислоты. ГАМК - главный тормозный нейромедиатор, так вот тиопентал просто стимулирует это действие. Он активирует ГАМК-рецепторы, замедляет закрытие ГАМК-зависимых каналов, которые имеются у нейронов, словом - вовсю помогает этой кислоте "жать на тормоз".
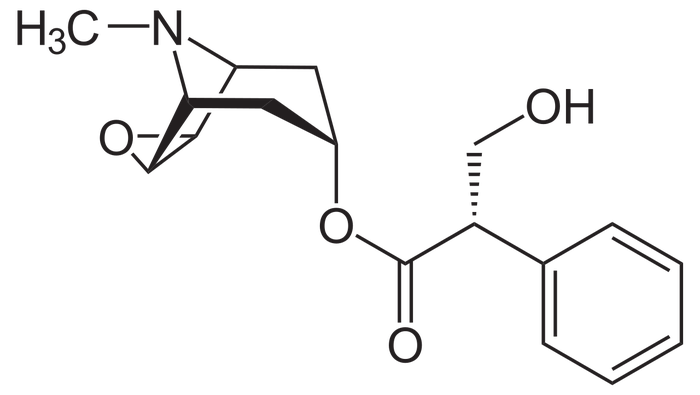
Скополамин - алкалоид (т.е. производится природой, а мы у неё это подсмотрели). Он работает с системой ацетилхолина (холинолитик, т.е. противодействует этому нейромедиатору). Для ацетилхолина есть два вида рецепторов: типа Н, никотиновые, и типа М, мускариновые. У них есть свои подтипы, вот у мускариновых рецепторов их 4 штуки. И все 4 блокируются скополамином, если тот оказывается в организме. Результат - седативное и снотворное действие, возможные кратковременные потери памяти и т.п., но ничего, связанного с желанием говорить правду, только правду и ничего, кроме правды. От укачивания ещё помогает...
Скополамин, или точнее - (1R,2R,4S,7S,9S)-9-метил-3-окса-9-аза-трицикло... а, ну его, это название по номенклатуре ИЮПАК. :)) Скополамин.
Все остальные препараты из богатого арсенала спецслужб фантазий писателей действуют примерно так же. Заторможенность - да, правдивые ответы - ну, как повезёт. Так что, способы заставить говорить правду, конечно, есть, но они не имеют никакого отношения к биохимии, нейрохимии и фармакологии. По крайней мере, пока. ;-) Такое вот резюме... многообещающее.
Источник: наш однозначно правдивый канал "Биохимикум" на Яндекс.Дзен. Статья моя, а эликсиры правды - из ближайшего супермаркета, между солью и маслом стояли где-то...
Антибиотики: часть 2. Борьба с борьбой
Всем привет! В первой серии мы немножко обсудили основную идею работы антибиотиков и немножко истории их открытия. Тот пост закончился не очень-то радостной для человечества идеей о том, что бактерии умеют с антибиотиками бороться. Новость (хотя не, это уже неновость) такая себе, как ни крути.
Вот умное и хитрое человечество придумало пенициллины. Молодцы мы, да? Гордость эволюции и всё такое. Но ответ этому изобретению бактерии нашли всего через пару десятилетий. По меркам микромира, пожалуй, очень долго искали. За год у бактерий проходит смена 50 тысяч поколений (цифра, конечно, дана для красоты. Разные бактерии размножаются в разных условиях с разной скоростью. Есть такие, которые удваивают свою популяцию каждые 10 минут). Но по человеческим меркам - совсем быстро у них это получилось... Устойчивость к антибиотикам - это серьёзная проблема.
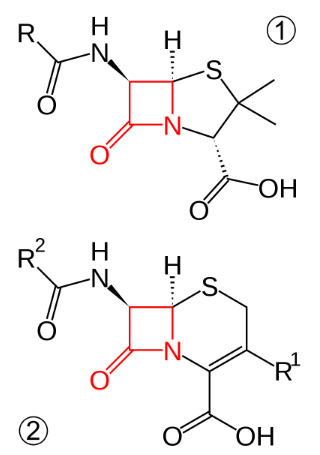
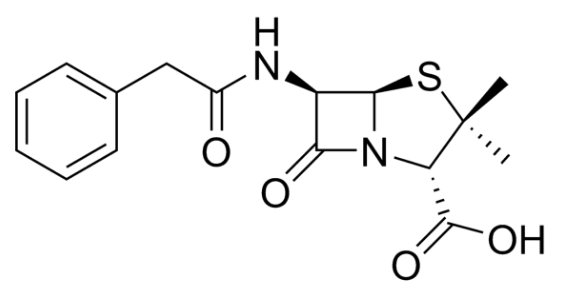
Что эти мелкие гады надумали: разрушать пенициллины специальными ферментами, которые зовутся β -лактамазы. В устройстве пенициллинов есть один фрагмент, который даже сам по себе не очень прочный. Четырёхчленный β -лактамный цикл (на рисунке выделен красным). В такой структуре всегда есть "внутреннее напряжение" (по сравнению с пяти- и шестичленниками, атомы расположены слишком близко друг к другу и хотят разойтись). А уж если им помочь...
Красным выделен тот самый цикл - уязвимое место у пенициллинов (1) и цефалоспоринов (2), это - ещё один класс антибиотиков, придуман позднее, и обещался быть весьма перспективным.
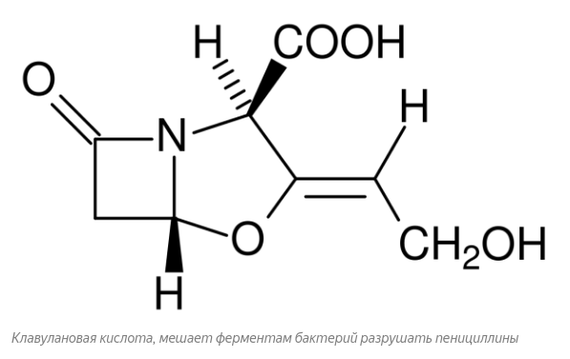
β -лактамазы атакуют связь между углеродом карбонильной группы и азотом. Связь рвётся, структура антибиотика меняется, и он перестаёт работать. Прознав о таком повороте дела, учёные сообразили: надо добавлять в препарат не только сам антибиотик, но и вещества, мешающие ферментам бактерий бороться с антибиотиком. Вышло забавно: такие вещества, как оказалось, и сами обладают антибактериальной активностью (правда, уступающей по силе настоящим антибиотикам). Получилось, что бактерии в попытках разрушить антибиотики сами себе подложили свинью! *злорадно потирает ручки* Мало того, что люди разгадали этот манёвр, так ещё и нашли такие добавки, что бактериям совсем не по вкусу. В первую очередь, это - клавулановая кислота и похожие на неё соединения. Победа?
Победа - разве что в одном сражении, но не в войне. В предыдущей серии мы рассказали, как работает пенициллин. Связывается с веществами, которые обычно работают на стройке бактериальной стенки-защиты, мешает тем работать, а в результате стенка получается никудышная. "Ага, - смекнули бактерии ещё в 60х годах XX века. - Так значит надо производить вещества, которые буду связываться с пенициллином лучше и прочнее, чем эти наши строители. Пенициллин будет связан, и строителям помешать уже не сможет". И преуспели в этом :-( Такие группы бактерий (их называют "метициллинрезистентными") начали причинять массу проблем. На них не действовали пенициллины и почти не действовали цефалоспорины.
Человечество ответило взрывным ростом открытий и производства новых антибиотиков, уже не похожих на пенициллины. Макролиды, фторхинолоны и мн. др. - у бактерий оказалась куча "мишеней", куча слабых мест. Блин, это ж всего лишь слабые глупые бактерии! Сможет ли венец эволюции (это который хомо сапиенс) надрать им задницу, наконец?! Но слабые-глупые научились бороться с пенициллинами, учатся противостоять и новым антибиотикам. К сожалению, скорость открытия новых антибиотиков сильно замедлилась. И бактериальные инфекции, вызванные антибиотикоустойчивыми бактериями, могут представлять немалую сложность для медицины. С начала XXI века (20 лет) было открыто меньше двадцати новых антибиотиков, и некоторые из них всё ещё под вопросом - идут испытания эффективности и безопасности. Для сравнения: в 80-е годы XX века (10 лет) найдено порядка 50 антибиотиков.
Ципрофлоксацин - ещё одна "глобальная надежда" на превосходство человека над бактериями. Поначалу был очень хорош, говорят. Но...
Но свой вклад в борьбу "человек VS бактерии" внесли и продолжают вносить обычные люди, не учёные и не врачи. Часто они выступают на стороне... бактерий, да. Бесконтрольный и неграмотный приём антибиотиков приводит к выведению устойчивых к этому препарату штаммов. В частности, к этому ведут уменьшение рекомендуемых дозировок ("ну зачем я буду травить себя антибиотиками, производители ведь наверняка завысили цифры дозировок, чтобы раскупали побольше") или сокращение срока приёма ("в инструкции написано, принимать десять дней, но мне уже через два дня лучше - перестану пить таблетки").
Принимать антибиотик нужно так, как прописал врач. Если в инструкции производителя приводится явно другая схема применения, есть смысл проконсультироваться с другим врачом. Мы не призываем слепо верить любому "человеку в белом халате", но следует понимать: у этих людей гораздо больше знаний и опыта в вопросе лечения антибиотиками, чем у рядового обывателя. Конечно, бывают врачи, которые назначают гомеопатию (линк на мой пост на Пикабу про Г.). Но относиться к этому надо всего лишь как к табличке "Ищите другого врача" на кабинете такого гомеопата. Обойтись без консультации врача и пить антибиотики самостоятельно - это не лучшее решение. Даже если "соседу помогло". Даже если "всегда эти таблетки пил(а)". Тем более, сейчас, когда дистанционные консультации - крайне простая штука. Неграмотное самолечение, в частности, уменьшение дозировки или сокращение сроков лечения антибиотиком могут привести к очень простой штуке: часть болезнетворных бактерий останется в живых.
Бактериальная клетка - она ведь что? Она пытается сработать на нейтрализацию антибиотика. Делает она это бессознательно, разумеется, но ведь делает! Стоит дать ей шанс научиться производить контрантибиотик - и этот синтез она запомнит, пропишет в ДНК/РНК, передаст по наследству (цена вопроса - полчаса времени, помним, да?). Ну и всё, для колонии бактерий, произошедших от успешной паразитки, что нашла способ борьбы, требуется уже новый антибиотик. Прежний уже не подействует. Или подействует слабее - и уж к следующему разу точно подготовит устойчивую колонию.
Даже при соблюдении всех рекомендаций врача, антибиотик - вовсе не конфетка для организма. Список побочных действий у каждого из них внушительный, и самое общее из них - нарушение работы ЖКТ. Всё дело в том, что антибиотик не умеет решать, которая тут бактерия плохая, а которая организму нужна. А нужных много! Они участвуют в пищеварении, и они же не позволяют размножаться в ЖКТ неполезным бактериям. "Место занято, ищите себе другой организм!"
Хорошие добрые бактерии-милашки смотрят на тебя, как на друга.
Антибиотик уничтожает бактерии без разбора, без разделения на хороших/плохих. Получается удобно для разных новых бактерий: курс антибиотика завершён, "поляна зачищена", никто не мешает поселиться. Не встретив сопротивления от постоянных "жителей" (полезных бактерий, которые перебиты антибиотиком), те начинают размножаться в ЖКТ. Результат - пищевые расстройства, диарея и т.п. Это, конечно, восстанавливается. Приём антибиотика заканчивается, полезные бактерии снова начинают размножаться и, наконец, побеждают неполезных. Иногда, чтобы им помочь, после антибиотиков врачи назначают т.н. "пробиотики" - капсулы, содержащие те самые полезные бактерии (или просто молочнокислое питание, в простоквашах-йогуртах-кефирах такие бактерии есть). Замечу, что про эффективность "пробиотиков" идут споры, хотя они таки содержат споры. Споры полезных бактерий. Как вам тавтология? (Что-то подобное я в своё время слышала на лекциях и размышляла ещё - не будет ли некрасиво с моей стороны не смеяться сомнительным остротам преподавателей). Ближе к теме. Побочка у антибиотиков - ещё один повод подходить к лечению антибиотиками вдумчиво и разумно, короче.
В третьей серии я сначала думала описать несколько антибиотиков и их работу. В частности, планировалось рассказать, почему самая страшная болезнь средних веков, бубонная чума, с изобретением антибиотиков перестала вообще быть чем-то серьёзным (при своевременном лечении, конечно). Но в итоге сочла этот план неразумным. Руководствуясь таким текстом, кто-нибудь займётся самоназначением препаратов, а мы как раз от этого предостерегаем. Поэтому заканчиваю на этом. Резюме:
1) Антибиотики - одно из величайших изобретений человечества.
2) Использовать антибиотики надо по назначению врача, соблюдая предписанные дозировки и режим.
3) Помним: антибиотики лечат бактериальные инфекции и не лечат вирусные.
Источник: наш антибактериальный канал "Биохимикум" на Яндекс.Дзен. Статья моя, картинки из сети.
Дисклеймер: многое в мире устроено сложнее, чем описывается в наших статьях. Мы в курсе. Но задача текстов - простым языком рассказывать об этом тем, у кого другая специальность. Не надо открывать нам глаза, помогите лучше Зулейхе с этим. За указание на опечатки, пропущенные по недосмотру слова и т.п - вот за это спасибо! :-)
Антибиотики. Когда хочется убивать
Речь об убийстве бактерий, разумеется. Плохих, вредных бактерий. Они вызывают различные инфекционные заболевания, и их-то, без сомнений, хочется убивать. Для этого и используются антибиотики. К сожалению, те не особо отличают плохих от хороших, и бьют всех подряд. Впрочем, обо всём по порядку...
Антибиотики - классные и, в умелых руках, крайне полезные вещества. Спасшие миллионы человеческих жизней. Антибиотики были придуманы для лечения бактериальных инфекций. И сразу уточнение: микромир одними бактериями не ограничивается. Там есть ещё и вирусы, и много кто/что ещё. Несмотря на некоторые данные (противоречивые!), что некоторые антибиотики действуют на некоторые вирусы, общее правило по-прежнему такое: бактериальную инфекцию антибиотиками лечат, вирусную - нет.
Всё дело в том, что бактерия - это вполне самостоятельная живая клетка. У неё есть какой-никакой метаболизм, который как раз и можно испортить антибиотиком, испортить с концами. А вирус - это не вполне живой объект, это как раз скорее случай "что", а не "кто". Без клетки, в которую он коварно пролезает, он не может в общем-то ничего. Сам по себе, вирус лишён обмена веществ, поскольку он есть лишь нуклеиновая кислота (РНК или ДНК), окружённая простеньким слоем из белков и липидов. Без биохимических конвейеров внутри. Соответственно, антибиотику некуда влезать и нечего портить. Тем не менее, антибиотики иногда назначаются при вирусных заболеваниях. Не против вирусов, а чтобы не дать каким-нибудь бактериям воспользоваться благоприятным моментом ослабленности организма.
Микромир при увеличении весьма красив...
Антибиотики по своей сути - очень натуральные, самые что ни на есть "природные" вещества. Ведь бактерии и прочие микроорганизмы - вовсе не в добрососедских отношениях. Говоря честно, каждая колония из микроорганизмов просто-таки мечтает уничтожить всех "соседей" и господствовать над миром самостоятельно. Или хотя бы замедлить соседское размножение, что в конечном итоге одно и то же. И для этой цели они вырабатывают разнообразные вещества, губительные для других микроорганизмов. То есть, антибиотики. Они бывают "бактерицидами" (убийцами) и "бактериостатиками" (замедляющими размножение). При применении последних человеком, задача по окончательному убийству инфекционного агента ложится на иммунную систему. Но ей всё равно сильно легче, раз эти агенты уже не множатся в геометрической прогрессии...
Так вот, антибиотики распространены в природе. Но не все эти вещества непременно безопасны для человека. У микроорганизмов, пытающихся отравить соседей, в конце концов, не было такой задачи - "подобрать для убийства такое вещество, чтобы ещё и для людей безопасно было". Тем не менее, некоторые природные антибиотики оказались вполне безопасными. И в первую очередь, это - пенициллин.
О том, что некоторые виды плесени оказывают благотворное действие на гнойные раны, знали давно, ещё в древнем Египте. Но умным египтянам, конечно, до целенаправленного производства первого антибиотика было очень и очень далеко. Плесень в контексте "а что ж в ней такого, что она так действует на раны и воспаления" не исследовали всерьёз аж до начала XX века. Что интересно, к этому времени уже были работы русских врачей (Манасеин и Полотебнов, 1873), итальянского биолога Гозио (1896), французского врача Дюшена (1897), из которых явнейшим образом следовало, что в плесени сокрыт ключ к борьбе с инфекцией. Но... научное сообщество отнеслось к этим работам равнодушно.
Кстати, поначалу не особо впечатлили это самое сообщество и работы Александра Флеминга (а ведь он выделил пенициллин!), первая из которых по этой теме была опубликована в 1928 году. И только когда в 1938-м Флори и Чейн получили устойчивое соединение пенициллина, дело сдвинулось. Массовое производство было налажено к 1943 году (как нельзя кстати! Ведь шла война), а в 1945 году все трое получили "нобелевку". В СССР, впрочем, тоже не дремали: в 1942 году Зинаида Ермольева и Тамара Балезина получили из плесени вещество "крустозин" - это тот же пенициллин. В том же году антибиотик начали производить.
Бензилпенициллин.
"Лирическое отступление": иногда в интернете проскальзывает информация, что штаммы пенициллинпродуцирующей плесени были украдены на западе советским разведчиком. Мы, разумеется, не в теме политики и работы разведок, но вскользь заметим: пенициллин Флемминга и крустозин были получены из разных штаммов плесени. Чтобы ещё больше засомневаться в версии с кражей штаммов, рекомендуем прочитать научную биографию Ермольевой - потрясающего учёного, выпускницы Ростовского-на-Дону госуниверситета (в то время он назывался "Донской"), которая отметилась в истории науки не только с пенициллином. Достаточно сказать, что, исследуя заболевание холерой, она намеренно себя заразила, чтобы на себе исследовать способы борьбы с возбудителем. Хочется как-нибудь написать о ней большую статью, хоть история - совершенно не наш профиль...
Зинаида Виссарионовна Ермольева.
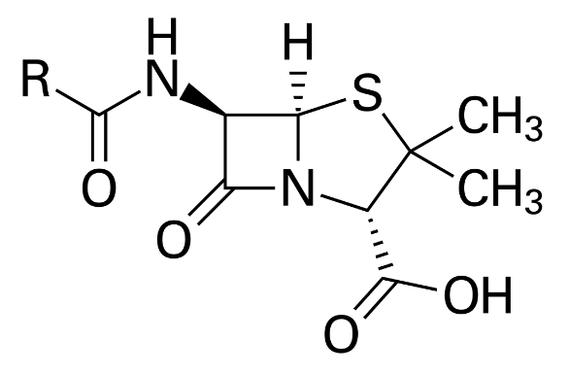
Так вот, пенициллин. Строго говоря, это - не одно вещество, а несколько разных (их так и называют, пенициллинЫ). Отличаются они друг от друга только радикалом (R), а 6-аминопенициллановая кислота для всех пенициллинов является одинаковым фрагментом.
Вот R - различающаяся часть, а всё остальное - одинаковое.
Все они мешают бактериям нормально жить. Как? А вот: многие бактерии отгораживаются от всего надёжной прочной стеной (клеточной стенкой на основе пептидогликана). Пенициллины мешают бактерии выстроить эту защиту. Как промышленные вредители-диверсанты они берут и рушат "производственные процессы" на стенкостроительном заводе. В отличие от диверсантов, не особо и скрываясь. Бедная беззащитная бактерия в результате этого погибает (а так ей и надо!) В первоисточнике имеется анимация сего занимательного процесса - очень интересно. Для узкого круга лиц))
Пенициллины становятся знаменитыми, не только из-за своей бактерицидной способности, но и как указатели на совершенно потрясающую идею: оказывается, можно находить или синтезировать вещества, которые портят бактериям жизнь изнутри, в прямом смысле этого слова! Пролезают в бактерию и бьют им по чувствительным местам. Уж наверное пенициллины - далеко не единственные подобные вещества, логично? Так началась эра антибиотиков.
Генштаб противника, конечно, не дремал. Бактерии нашли, что противопоставить пенициллинам... В следующей серии расскажем, как бактерии борются с антибиотиками, а человеческая наука борется с этой борьбой. "И вновь продолжается бой..."
Источник: наш антибактериальный канал "Биохимикум" на Янлекс.Дзене
Текст статьи мой (анимация там есть, она не моя), пенициллин аптечный, плесень и прочие фотки - общественные, то есть из интернетов.
PS: дисклеймер для биологов и прочих причастных: я в курсе, что описанное здесь устроено несколько сложнее. Здесь - упрощения, для небиологов в первую очередь.
PPS: для политиков-антисоветчиков-конспирологов: если наши пенициллин таки украли, то и ладно. Молодцы наши! А меня этическая сторона работы нашей разведки не заботит, я - биохимик.
PPPS: знаю, что давненько новых статей не было. Работы много пока, времени не хватает. Скоро будут!
Гомеопатия: работает или нет? Взгляд биохимика
Нет. На этом всё, расходимся. :-D Дата, подпись, д.х.н. и всё такое. Но для такого вывода не надо быть ни доктором, ни кандидатом, ни даже аспирантом-троечником. Надо просто включать логику и разум. Тем удивительнее новости с полей - то диссертацию по гомеопатии (!) кто-то успешно (!!!) занёс кому надо защитил, то ещё какой-нибудь трэш... Собственно, в сети есть куча реплик типа "а мне помогло". Ну, не могут же они все быть покупными?
Давайте более серьёзно, в подробностях. Современная гомеопатия - это такая лженаука, использующая сомнительные термины типа "памяти воды" и прочую антинаучную ересь. Из-за обилия такой "терминологии", отсылок к каким-то "учёным" с "мировой известностью" и прочих нечестных приёмов гомеопатия может выглядеть, как что-то, внушающее доверие. Но любой, даже далёкий от биохимии человек, понимает: не может работать гомеопатический препарат, просто потому, что там отсутствует какое-либо действующее вещество.
Идея у гомеопатических "препаратов" (да, тут много слов в кавычках будет) состоит в сильном разбавлении "действующих" веществ. Проблема в том, что на определённом этапе такого разбавления количество вещества становится ничтожно малым. Буквально. Смотрите: если взять 1 моль вещества и развести его по принятой в гомеопатии схеме 12C (это 1 к 10 в 24-й степени), то от вещества может не остаться ни единой молекулы. Ведь число Авогадро (количество молекул в 1 моль вещества) меньше: 6,02*10^23. Помните химию 8 класса?
Да, молекула-другая может и остаться (статистика и теория вероятностей это допускают), но это всё равно крайне мало. Своё действие пара молекул не окажет, по той же причине: статистика. Химическая реакция в масштабе одной молекулы - ничтожное событие. Молекул должно быть очень-очень много. Ну для примера, столовая ложка воды (18 грамм, для удобства счёта) содержит примерно 600000000000000000000000 молекул (надеемся, не опечатались с нулями). Что такое одна штука молекула в масштабах хотя бы этой ложки воды? Капля в море. А гомеопаты утверждают, что она отчего-то вдруг сработает.
Ну ладно, а что насчёт памяти воды?
У воды нет никакой памяти. Это - ещё одна глупость, тиражируемая гомеопатами. Каждое вещество специфично по своему строению и свойствам - поэтому наш мир настолько прекрасен и разнообразен. Если бы вода "запоминала" что-то о других веществах, случайно или неслучайно попавших в неё, было бы презабавно. Одна крупинка сахара делала бы сладкой цистерну чая, а капля спирта превращала бы в водку весь мировой океан.
Но ведь троюродному брату мужа соседки гомеопатия помогла!
Вот, мы дошли до объяснения феномена "а вот помогло же". Здесь - несколько возможных вариантов. Первый (наиболее вероятный) - улучшения наступили по независящим от приёма "чудо-таблеток" причинам. Часто так бывает при простудных заболеваниях. Фишка в том, что иммунитету, если он встретился с незнакомым возбудителем инфекции, всегда нужно какое-то время, чтобы научиться производить нужные антитела. Потом закономерно наступает улучшение (это - очень упрощённая схема, но для примера вполне подходящая). Смотрите-ка: троюродный брат мужа соседки ведь наверняка не сразу начал пить гомеопатические "препараты". Сначала он подождал несколько дней - авось само пройдёт? Не прошло, и он принялся лопать таблетки с мелом и сахаром (гомеопатические средства зачастую сделаны именно из этих веществ). НО: несколько дней уже ведь миновало, и иммунитет троюродного брата это время даром не терял, он учился. Выучился - и начал действовать. Наступило улучшение, а затем и выздоровление. Благодаря действию иммунитета. Не благодаря действию "гомеопатических препаратов".
Антитела изображают именно так, похоже на букву Y. Хотите узнать, почему? Ну, вы поняли, где можно узнать... ;-)
Второй вариант: эффект плацебо. Слышали о таком? Сейчас есть много высказываний, что такого эффекта не существует, с разным уровнем аргументации. Но как минимум в ряде случаев, по нашему мнению, этого эффекта не может не быть. Принятие таблетки из мела и сахара (но только если верить, что это - чудодейственное средство) таки запустит ряд биохимических событий. Связанных не с содержанием таблетки, а с самим фактом её принятия. Не будем сейчас утомлять в деталях, как оно бывает. "Я же выпил(а) крутейшее гомеопатическое лекарство за 100500 денег, оно обязательно сработает!" Подъём настроения, дофамин, серотонин и т.п. В свою очередь это влияет на тот же иммунитет: он начинает действовать чуть активнее. Не повлиять не может, ведь иммунная система и гормональная система тесно связаны. Но куда лучше принимать настоящие медицинские препараты, они ведь тоже запустят этот механизм. Но при этом, ещё и реально действуют, реальным действующим веществом.
Резюме: гомеопатические средства в современном их понимании (доведение содержания действующего вещества до абсурдной одной молекулы на таблетку, в лучшем случае) не работают.
Два замечания под конец текста. Первое: не следует путать гомеопатию с фитотерапией (лечением лекарственными растениями). Фитотерапия работает, т.к. в растениях содержатся настоящие лекарственные вещества, в значимых количествах. Но сразу же скажем: фитотерапия работает не всегда. Этих веществ в растении может оказаться меньше, чем нужно. По разным причинам. Например, вещество должно образовываться в растении на втором году его жизни, а сборщики собрали слишком молодое растение. Или оно образуется только, если растение получает достаточно воды и света, а сбор был произведён в засушливой тенистой местности. Причин масса, поэтому фитотерапевтические методы применять можно, но учитывая все подобные нюансы.
Второе: не следует путать гомеопатические препараты с препаратами с недоказанной/слабодоказанной эффективностью. Первые не работают, вторые - могут работать (не равно "обязательно сработают"). Но, по крайней мере, действующие вещества в них есть, опять-таки, в значимых количествах. Никакой "памяти воды" и миллиардных разведений. Но подробнее о них - как-нибудь в другой раз. Спасибо за внимание!
Первоисточник: наш уютненький канал "Биохимикум" на Дзене. Ссылка на саму статью: вот.
Путь лекарства
Противоопухолевый препарат, над которым мы работали 4 года, который показывал прекрасные результаты на клетках и животных... был признан неэффективным уже в первой фазе клинических исследований. И, конечно, отрицательный результат в науке - это тоже результат, но слишком грустно. Это провал. На который были выделены миллионы.
Вы задумывались когда-нибудь, какой путь проходит сертифицированный препарат прежде, чем окажется на полке аптеки? И почему те же противоопухолевые столько стоят?
📚 Всё начинается с кучи статей. Первое задание, которое мы даём всем студентам, пришедшим в лабораторию - найти, прочитать и понять пару научных статей по теме. Этим же занимаются научные сотрудники, за этим ездят на конференции. За информацией. Что уже сделано, какие есть идеи, мысли, гипотезы, каков механизм работы рецепторов и белков, втянутых в биохимию патологического процесса... Важно досконально понять всё, до чего до тебя додумался научный мир.
💡И на этой базе возникает мысль: «а что если попробовать вот так? Сделать соединение поменьше, ввести другой заместитель погидрофильнее и упаковать в невирусную систему доставки?»
И это точка невозврата. Теперь все силы твоей лаборатории и дружественных ей будут направлены на реализацию этой странной идеи.
🧪 Химики начинают синтез. Но у вещества есть куча стерических затруднений, да ещё и оно оптически активно, а потому задача не из простых. Через полгода упорной работы химиков-синтетиков всей лабораторией вы задумчиво смотрите на коричневый склизкий комок будущего препарата-спасителя, который сейчас размазан по колбе. Хммми...
🛁 Квест продолжается. Это вещество ещё прилично грязное, с примесями снятых защитных групп, с кусками других побочных продуктов. Его нужно очистить.
Химик благословляет хроматограф и своё детище на работу, и начинает очистку. Первая, вторая серия, трудоемкое расщепление рацематов. Ох уж эта оптическая активность... Проверяем на всякий случай на математической модели, ну конечно, изомер не обладает нужной нам активностью. Специалист ругается в голос, подбирает растворители и выдаёт-таки чистоту 98%, допустимую для доклинических испытаний.
Уже на этих стадиях идее может прийти конец. Химики не смогут синтезировать и очистить задуманное вещество так, как это необходимо. Увы.
✔️ Теперь нам нужно подтвердить, а то ли вещество мы вообще выделили 🙈. Были случаи ))). Поэтому идём к аналитикам, приносим жертву масс-спектрометру и, счастье, это наше вещество, масса совпала. Потом мы ещё несколько раз перепроверим другими методами, но пока подойдёт и такое подтверждение.
🐀 Дальше мы либо начинаем работать с клетками, либо сразу выходим на стадию работы с животными - заказываем партию особых nude-мышей (иммунодепрессивных, чтобы их иммунная система не мешала работе препарата). Смотрим, как реагируют на препарат, на какие дозы, какие побочные реакции есть, делаем матмодели процессов, совместно с коллегами из других лабораторий пробуем разные варианты систем доставки. Из 10.000 потенциально интересных соединений, которые берут в работу фармкомпании, примерно 250 пройдут на стадию доклиники. Всё остальное будет просто отрицательным результатом.
🐁 Самый частый вопрос, который задают мне люди, когда узнают о том, что мы работаем с животными: «и вам не жалко?! Почему нельзя испытывать на заключённых?!»
Не в жалости дело. Это высокая миссия мышек, их дело жизни и их работа. Они пришли в этот мир для того, чтобы помочь. Без них мы не справимся.
А испытывать на заключённых нельзя как минимум из-за этических вопросов, а как максимум - математика запрещает. Для исследования важна 100% статистическая однородность выборки. Совсем одинаковые мыши. Одного пола, возраста, содержащиеся в одинаковых условиях, одинаково здоровые, с одинаковыми нокаутными генам (если нужно). Тогда мы можем быть уверены, что 8 летальных исходов из 10 - это проблема препарата. А если мы возьмём 10 разных людей? Один с туберкулёзом в активной форме, другой с аутоиммунным заболеванием, третьему 59 лет, четвёртый в клинической депрессии, пятый с гастритом мается, шестой с мигренями, седьмой ни разу за 40 лет не был у врачей и его анамнез вообще невозможно собрать, у восьмого митральный клапан помирает, девятый аллергик лютый, а десятая - женщина в период менструаций. Классный набор. И как понять, от чего умрут 8? От того, что добитая изониазидом печень отказала раньше, чем успела метаболизировать новый препарат? Статистика не прощает такую выборку. И никакой информации мы всё равно не получим.
📈 А математические модели... к сожалению, они ещё не могут описать действие вещества на живой организм настолько качественно, чтобы мы могли сразу перейти к проверке на пациентах.
На животных проводятся различные испытания: изучают безопасность (общую и специфическую токсичность препарата), эффективность препарата в отношении конкретного заболевания на моделях, подбирают нужные дозы и режимы введения в фармакокинетических исследованиях. По испытаниям разрабатывают протоколы по международным нормам, делают математическую обработку результатов и пишут итоговый отчёт. На его основании принимается решение о том, переводится ли препарат дальше, в клинические исследования или нет.
Из тех 250 препаратов, что вышли на доклинику, хорошо если 5 пойдут дальше. И только 1... вдумайтесь. 1 из 10.000 соединений возможно станет современным препаратом.
💰Разработка одного препарата с нуля занимает 10-12 лет. Каждый год работы исследователей, разумеется, оплачивается. Оплачивается, чтобы раз за разом получать тот самый «отрицательный результат», с которым столкнулись мы.
Эх.
Взято у https://www.facebook.com/yanapollly/posts/2471566789622635
(С) Яна Полянских
В поисках гена-мишени
Не так давно в ФИЦ «Институт цитологии и генетики СО РАН» был представлен цикл презентаций «Как создаются современные лекарства». Поводом для выбора темы стали новые возможности, которые дало объединение «под крышей» одного Федерального исследовательского центра ведущего института СО РАН, занимающегося фундаментальными генетическими исследованиями, и двух НИИ медицинского профиля. Теперь в рамках одной организации стало возможным осуществление полного цикла создания лекарственного препарата, от компьютерных моделей до клинических испытаний и выпуска пробных партий готового препарата. О чем собственно и рассказали собравшимся (журналистам и студентам вузов Новосибирска) сотрудники ФИЦ ИЦиГ.
Сегодня путь на рынок для любого нового лекарства занимает много лет, а начинается он в научных лабораториях, где часто вместе работают молекулярные генетики и специалисты по биоинформатике.
Об этом этапе рассказала сотрудник лаборатории компьютерной протеомики Института цитологии и генетики Олька Сайк. А точнее – про поиск потенциальных генов-мишеней, перспективных для разработки новых лекарств с помощью анализа генных сетей.
В настоящее время медицине известно более 10 тысяч различных заболеваний и синдромов, от которых может страдать человек. В Госреестре зарегистрировано почти 40 тысяч лекарственных препаратов. И, тем не менее, для многих заболеваний существует только симптоматическое лечение (не устраняющее саму болезнь, а лишь ослабляющее ее воздействие), а уровень смертности населения остается высоким.
Не упрощают жизнь медикам и другие факторы: с годами многие бактерии и вирусы становятся устойчивыми к существующим лекарствам, сильнодействующие препараты имеют неприятные побочные свойства, а одновременный прием разных лекарств (при одновременном лечении разных болезней) может вести к новым осложнениям.
В этой ситуации требуются новые лекарства, более эффективные и в то же время безопасные, а еще лучше – персонализированные, учитывающие генетические особенности пациента. Ключевым этапом при их создании является правильный выбор фармакологической мишени, выбор белка, на который необходимо оказать химическое воздействие для предотвращения развития заболевания.
Сделать этот поиск более быстрым, эффективным и менее затратным позволяют методы биоинформатики, опирающиеся на анализ генных сетей.
– В начале прошлого века генетика исходила из парадигмы, что один ген определяет один фенотипический признак, - напомнила Ольга Сайк. – Но позднее ученые пришли к выводу, что отдельный признак обеспечивается функционированием группы взаимодействующих генов. К примеру, цвет глаз определяется группой из 5-10 генов. Так и возникла концепция генных сетей, каждая из которых определяет тот или иной признак организма. А сам ген при этом может быть включен в разные сети.
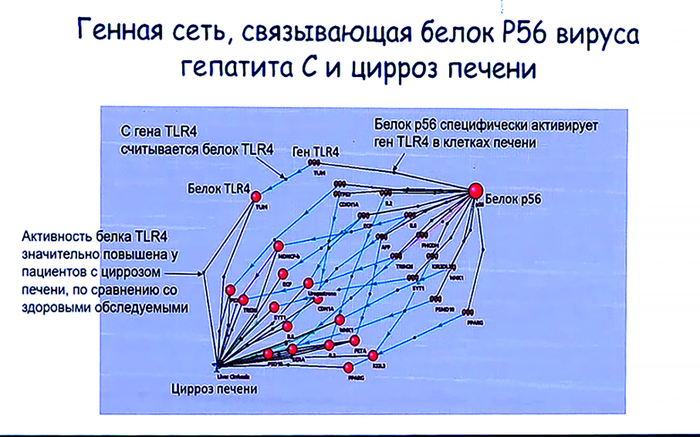
Анализ генных сетей, в частности, позволяет понять, каким образом воздействие вируса или мутации самого гена может приводить к развитию определенного заболевания. В качестве примера Ольга Сайк привела модель воздействия вируса гепатита С, ведущего к развитию цирроза печени. Известно, что белок вируса р56 может специфически активировать белок TLR4 в клетках печени человека. Также известно, что у людей, болеющих циррозом, уровень данного белка в печени значительно повышен. Далее, выстроив модель генной сети, в которой задействован пораженный вирусом ген, можно выделить гены-мишени, воздействие на которые позволит нейтрализовать негативный фактор.
Один из подходов предполагает выделение внутри сети отдельных кластеров, ответственных за те или иные процессы, затем выбирают те из них, что наиболее вовлечены в процесс развития заболевания (апоптоз клеток или наоборот – иммунный ответ и т.п.), после чего работают, в первую очередь, с ними. Затем внутри кластера ищут хабы (центральные вершины) – гены, через которые проходит больше всего связей внутри генной сети. Обычно это белки – регуляторные молекулы. Именно они и являются приоритетными генами-мишенями.
Дальнейший анализ позволяет также оценить риски развития у пациента побочного эффекта в результате воздействия на мишень лекарством. Ведь ген, выбранный мишенью, может участвовать во многих других процессах, в том числе, не связанных напрямую с заболеванием. И надо оценить, как это воздействие повлияет на другие процессы, в которые вовлечен ген. Исходя из этого, приоритет получают гены, которые имею меньше связей с иными биологическими процессами.
Звучит довольно просто, но на самом деле решение этой задачи занимает массу времени и сил. Ведь многие сети включают сотни генов и еще больше – регуляторных взаимодействий между ними. Для проведения всего этого объемного анализа разработан специальный математически аппарат. Изучая воздействие того же вируса гепатита С, сотрудники ИЦиГ выявили 900 белков человека, вовлеченных в этот процесс. А затем, проанализировав их работу в генных сетях, определили несколько потенциальных кандидатов в гены-мишени, причем, не только для лечения собственно гепатита С. Так, белок человека енолаза 1 (ENO1) может быть также мишенью для лекарств против воспаления легких, неходжкинской лимфомы и глиомы. И все же – это только первый (и не самый трудоемкий) этап на пути к новому лекарственному препарату.
Следующий шаг – компьютерное моделирование потенциальных ингибиторов: сначала строится модель белка-мишени, а затем подбирается химическое соединение, которое блокировало бы его работу. Более подробно об этой работе рассказал еще один сотрудник лаборатории компьютерной протеомики Никита Иванисенко.
– Если вы проанализируете, что вам выписывает терапевт, то вы увидите, что большинство лекарств – это низкомолекулярные соединения, - сказал он. – Фактически, задача молекулы лекарства – ингибировать конкретный белок (затормаживать или останавливать его работу), который ответственен за возникновение и развитие заболевания.
К примеру, установлено, что если удастся проингибировать (нарушить работу) белка протеаза ВИЧ-1, то сам вирус иммунодефицита человека также прекращает размножаться и поражать организм. Собственно, сегодня множество исследований по созданию лекарства против ВИЧ работают именно в этом направлении.
В описании такого рода исследований, ученые часто используют аналогию «ключ-замок». В ней белку отводится роль «ящика», который надо «открыть». «Замочной скважиной» в данном случае является некий сайт (место, через которое к нему может прикрепиться молекула лекарственного препарата).
И задачей ученых на данном этапе является смоделировать химическое соединение, которое смогло бы связаться с этим сайтом, создать «ключ» для этого уникального природного «замка».
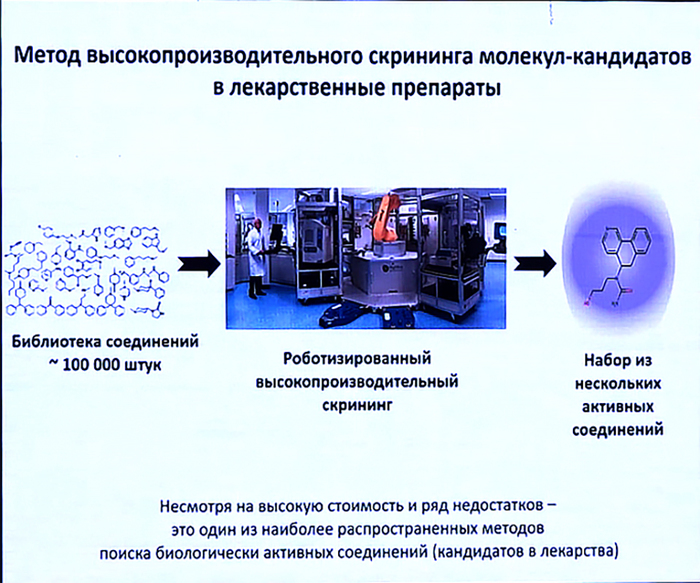
Существует много способов подбора таких соединений, которые в фармацевтике классифицируют по двум подтипам. Это методы полного перебора (когда проверяются все возможные комбинации, а речь может идти о миллионах вариантов) и методы рационального подхода (когда сначала изучается устройство «замка», и на основе этого подбираются подобия «ключей»). Оба подхода сегодня широко используются в фармацевтике. Первый подход более понятен и методы поиска в его рамках хорошо отработаны, зато второй часто помогает значительно сэкономить ресурсы и время.
Каким же образом ученые изучают «замки» белков. Большой популярностью пользуется, в частности, метод рентгеноструктурного анализа. Для начала надо вырастить кристалл, который будет состоять из белка-мишени (что само по себе очень непростая задача). Затем проводится анализ дифракции рентгеновских лучей. И на его основе строится компьютерная модель белка-мишени, которая и предоставляет информацию об устройстве его «замка». Правда, в этой модели нет информации о том, какие части молекулы белка подвижны, а какие – нет. На этом этапе и начинается рациональный поиск «отмычки», с использованием компьютерных вычислений, таких как машинное обучение.
Как видно из описания, несмотря на то, что такой подход заметно сокращает число кандидатов на роль «отмычки», сам по себе он подразумевает решение сложных задач и привлечение для этого весьма компетентных специалистов. Поэтому, несмотря на очевидные «слабые места», методы полного перебора по-прежнему пользуются высокой популярностью у фармацевтических компаний.
Впрочем, формирование некоего списка кандидатов на роль нового лекарства – это лишь первый шаг. Далее в работу включаются исследователи другого профиля, о которых мы подробнее расскажем в следующих частях нашего мини-цикла.
Наталья Тимакова, https://academcity.org/content/v-poiskah-gena-misheni