Коллаген, передовой даже по мировым меркам, создан в России. Большое исследование, которое легло в основу создания.Часть 1
Дорогие читатели, исследования описанные в данной статье легли в основу создания первого в России коллагена, обладающим повышенной усвояемостью среди всех прочих. Это все благодаря извлечению коллагена из рыб. Компания Bio Farm Eco стала пионером в данной области и благодаря внедрению технологии в своё производство уже выпускает продукт под названием: Гендерный коллаген для женщин и Гендерный коллаген для мужчин
Я очень благодарен данной компании за возможность внести свой вклад в мировую фармацевтику!
1. Введение
Использование морского коллагена быстро растет благодаря его уникальным свойствам по сравнению с коллагеном млекопитающих, таким как отсутствие риска передачи заболеваний, отсутствие религиозных ограничений, экономичный процесс, низкая молекулярная масса, биосовместимость и его легкое усвоение организмом человека. В этой статье представлен обзор недавних исследований, проведенных с 2014 по 2022 год по извлечению коллагена из материалов морского происхождения, в частности рыбных субпродуктов. Представлены структура рыбьего коллагена, методы экстракции, характеристика и биомедицинское применение. Более конкретно, описаны и сравнены методы экстракции морского коллагена уксусной кислотой и глубоким эвтектическим растворителем (DES) для выделения морского коллагена. Кроме того, исследуется влияние параметров экстракции (температура, концентрация кислоты, время экстракции, соотношение твердого вещества к жидкому) на выход коллагена. Кроме того, были обобщены вопросы разработки биоматериалов и терапевтического применения морского коллагена.
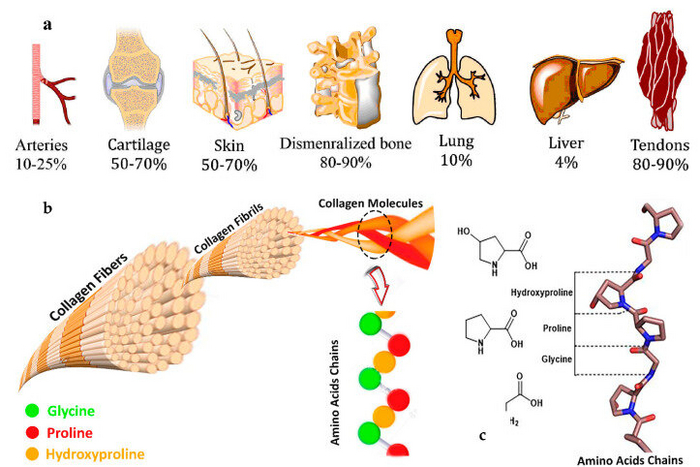
Коллаген является наиболее распространенным структурным белком во внеклеточном матриксе различных соединительных тканей организма (т.е. Кожи, костей, связок, сухожилий и хрящей) (Рисунок 1а). Основное биомедицинское применение коллагена находилось в биоматериалах, особенно в качестве носителей лекарств и генов, тканевой инженерии, рассасывающихся хирургических швах, остеогенных материалах и костных пломбировочных материалах, гемостатических средствах, иммобилизации терапевтических ферментов и повязках для покрытия ожогов / ран. Коллаген является важнейшим компонентом процесса заживления ран; он действует как естественный структурный каркас или субстрат для роста новых тканей и играет важную роль на всех этапах заживления ран, включая гемостаз, воспаление, пролиферацию и ремоделирование . Коллаген, вырабатываемый организмами, определяется как эндогенный, который состоит из трех длинных аминокислотных цепей геликоидальной формы. Цепи полипептида, образованные повторяющейся последовательностью (Gly-X-Y), n образуют коллагены, где X и Y могут быть заняты любой аминокислотой, хотя эти позиции обычно занимают пролин и 4-гидроксипролин (Hyp, рисунок 1(b). Коллаген разрушается из-за старения, воздействия ультрафиолетового излучения и употребления табака. Разрушение коллагена приводит к появлению морщин, дряблости кожи, ригидности суставов и сухости кожи, и поэтому важно выявить новые ресурсы коллагена для регенерации тканей.
Рисунок 1
(a) Приблизительное содержание коллагена в различных тканях;(b) Структура коллагеновых волокон, фибрилл, тройных спиралей альфа-цепей и аминокислотных остатков, 4-гидроксипролина (Hyp), глицина (Gly) и пролина. Структура аминокислотных цепей коллагена (c).
Экзогенный коллаген в основном используется в пищевых продуктах, биоматериалах и фармацевтике. В связи с широким спектром применения коллагена были исследованы альтернативные источники, такие как коллаген млекопитающих крупного рогатого скота и свиней. Тем не менее, вспышка таких заболеваний, как губчатая энцефалопатия крупного рогатого скота (BSE), и религиозные ограничения ограничили применение коллагена на основе млекопитающих.
С другой стороны, в последние годы понятие “устойчивое развитие” стало одним из основных оплотов в рамках программ "зеленой экономики". В глобальном масштабе настоятельная необходимость перехода к экологически чистым альтернативам эксплуатации природных ресурсов была продиктована необходимостью решения растущих экологических и экономических проблем. В соответствии с этим экологическим подходом Европейская комиссия одобрила “Голубой рост”, долгосрочную стратегию, направленную на поддержку устойчивого роста в морском секторе. Согласно Карузо и др., было подсчитано, что более 50% тканей рыбы, включая плавники, головы, кожу и внутренности, выбрасываются как “отходы”, что превышает 20 миллионов тонн побочных продуктов в год. Однако использование субпродуктов из морепродуктов представляет собой растущую проблему. Более того, одной из наиболее привлекательных особенностей, характеризующих отрасль производства морепродуктов, от которой отказались, является высокое содержание ценного белка (10-25%) и соединений, богатых липидами (17-35%).
Таким образом, использование морских субпродуктов в качестве нового источника коллагена привлекает все большее внимание из-за их легкой экстракции, высокого содержания коллагена, усвояемости организмом человека с учетом его низкой молекулярной массы, биосовместимости, отсутствия рисков заболеваний животных и патогенов, экологичности, незначительного содержания биологических загрязняющих веществ и токсинов, менее значительных религиозных и этических ограничений и незначительных проблем с регулированием и контролем качества. Следовательно, многие исследования сосредоточили свои усилия на извлечении и характеристике коллагена из кожи различных рыб, таких как мелкопятнистая кошачья акула (Scyliorhinus canicula), рыба-кролик (Chimaera monstruosa), акула-фонарь (Etmopterus spp.), кошачья акула (Galeus spp.), скат-кукушка (Leucoraja naevus), обыкновенный атлантический гренадер ( Nezumia aequalis), треска (Gadus morhua), а также чешуя и плавники Catla catla и Cirrhinus mrigala.
Коллаген из кожи, костей и плавников рыб имеет низкую температуру денатурации (25-30 ° C для большинства видов рыб) по сравнению с коллагеном млекопитающих (39-40 °C) и переменный состав, что ограничивает его использование в биомедицине. Низкое содержание аминокислот (пролина и Hyp) в морском коллагене обуславливает низкую температуру денатурации, что затрудняет обращение с рыбьим коллагеном, поскольку он денатурирует при температуре тела человека. В настоящее время изучается коллаген морских беспозвоночных организмов, включая медуз и морских губок.
Основные функции коллагеновых волокон в тканях позвоночных заключаются в предотвращении преждевременного механического сбоя и содействии накоплению, рассеиванию и передаче энергии от опорно-двигательного аппарата или внешних воздействий. Коллагеновые волокна обеспечивают структурную поддержку всем органам тела и обеспечивают упругость, эластичность и прочность, необходимые для эффективного передвижения, регенерации тканей и восстановления посредством процессов механохимической трансдукции. Коллаген участвует в построении волокнистой сети клеток, называемых фибробластами, которые образуют основу для роста новых клеток. В таких областях, как дерма, коллаген играет активную роль в защите кожи, препятствуя поглощению и распространению патогенных веществ, токсинов окружающей среды, микроорганизмов и раковых клеток.
Существует несколько обзоров ресурсов коллагена для разработки биоматериалов, гидролизованного коллагена, а также источников и применений морского коллагена. Цель этой обзорной статьи - представить обновленный обзор состояния выделения коллагена из рыбных субпродуктов с особым акцентом на параметры, необходимые для выделения коллагена из рыбных субпродуктов, с использованием статей, опубликованных с января 2014 по июнь 2020 года.
2. Образование коллагена, стабильность и молекулярная структура
У позвоночных, таких как млекопитающие, рыбы и птицы, можно обнаружить 28 различных типов коллагена, которые кодируются по меньшей мере 45 различными генами. Коллаген является основным структурным белком, содержащимся во внеклеточном матриксе (ECM), на его долю приходится от 25% до 35% общего содержания белка в организме. Существует по меньшей мере 28 типов коллагена в зависимости от доменной структуры и их надструктурной организации, но 80-90% коллагена в организме состоит из типов I, II и III. Наиболее распространенный тип коллагена в организме, тип I, содержится в костях, коже, сухожилиях и органах. Тип II можно обнаружить в хрящевой ткани, а тип III - в ретикулярных волокнах, крови и коже. Коллаген III типа содержится в коже, стенках сосудов и ретикулярных волокнах легких, печени и селезенки (рисунок 1). Типы IX, XIV и XIX (FACIT: коллагены, связанные с фибриллами, с прерывистыми тройными спиралями) в небольших количествах связаны с фибриллообразующими типами, а типы IV, XIX и XVIII обнаружены в базальных мембранах клеточных мембран. Коллагены типов I-IV являются наиболее распространенными у беспозвоночных.
Одиночная молекула коллагена имеет длину около 300 нм и диаметр 1,5–2 нм, а многоколлагеновые молекулы образуют более крупные коллагеновые агрегаты, такие как фибриллы. Коллаген характеризуется структурой α-доменов с тройной спиралью, названной “тропоколлаген”, поскольку он состоит из трех различных α-цепей. Это три параллельные полипептидные нити, каждая из которых имеет конформацию левосторонней спирали, намотанной друг на друга подобно канату, образуя правостороннюю тройную спираль, или “суперспираль”, которая представляет собой общую плотно упакованную трехспиральную форму молекулы, стабилизированную множеством водородных связей. Для намотки трех левосторонних спиралей в правостороннюю тройную спираль требуется, чтобы каждая третья аминокислота представляла собой остаток глицина (Gly), в то время как многие из оставшихся позиций в цепи заполнены пролином и Hyp. Gly требуется на третьей позиции, потому что в переполненном центре трехцепочечной спирали нет места для более крупной боковой группы, чем один Н-атом Gly. Последовательность представляет собой повторяющийся паттерн X-Y-Gly, где X и Y могут быть отнесены к любым другим аминокислотным остаткам. Однако позиции X и Y часто занимают пролин и Hyp соответственно. Форма Pro–Hyp–Gly является наиболее распространенным трипептидом (10,5%) в коллагене.
Благодаря уникальной аминокислотной последовательности плотная тройная спираль коллагена особенно стабильна, и считается, что наличие Hyp в положении X способствует стабильности спирали. Гидроксильная группа Hyp играет существенную роль в стабилизации тройной спирали благодаря связыванию с пирролидиновым кольцом. Она повышает температуру денатурации и энтальпию денатурации коллагена. Более того, тройные спирали окружены сетью молекул воды, обеспечивающей термостабильность тройных спиралей благодаря высокой энтальпии денатурации, которая напрямую отражает количество водородных связей, а также функционирует как чувствительный параметр степени тройной спиральной структуры. Напротив, температура денатурации отражает энтропийный вклад в стабильность тройной спирали коллагена. Межцепочечные водородные связи стабилизируют три α-цепи в спирали и делают молекулу умеренно устойчивой к атаке других молекул. Эти водородные связи, которые возникают, когда аминогруппа (NH) остатка Gly образует пептидную связь с карбоксильными группами в соседнем полипептиде, помогают удерживать три цепи вместе.
2.1. Морской коллаген
Морские коллагены, такие как кожа рыбы, кости, хрящи и чешуя, включая источники как из морских позвоночных, так и из беспозвоночных, более биодоступны по сравнению с бычьим или свиным коллагеном и обладают более высокой способностью к всасыванию (до 1,5 раза эффективнее в организме) и более быстрой циркуляцией в кровотоке из-за их низкой молекулярной массы и малого размера частиц. Кроме того, коллагены на морской основе схожи с обычным бычьим и свиным коллагеном с точки зрения аминокислотного состава и биосовместимости. Рыбий коллаген может быть получен из различных рыбных побочных продуктов, таких как рыбные кости, чешуя и шкуры (рисунок 2а), которые ежедневно потребляются в разных частях мира и приводят к образованию большого количества отходов - от 50% до 70% исходного сырья, которое образуется в рыбных цехах и на перерабатывающих фабриках.
Рисунок 2
(a) Рыбьи кости, чешуя и кожа как источники коллагена. (b). Процедура извлечения коллагена из рыбных субпродуктов.
2.1.1. Рыбья кожа
Кожа рыбы обычно содержит коллаген I типа с высокой степенью чистоты (около 70%) в зависимости от возраста вида и сезона года. Коллаген из рыбьей кожи демонстрирует превосходную способность удерживать воду (около 6% от его веса при воздействии 63% влажности в течение 24 часов) и не оказывает раздражающего действия, поэтому подходит для нанесения на кожу. Исследование Бланко и др. коллагена из кожи двух видов костистых и двух видов хрящевых показало температуру денатурации коллагена в диапазоне от 23 до 33 ° C, в то время как коллаген, выделенный из кожи трески, денатурировался при температуре около 16 ° C, что, возможно, могло быть связано со средой обитания вида. Однако коллаген из кожи тилапии, сома, помфрета и макрели требует низкой температуры экстракции (чуть ниже 13,26 °C), длительного времени экстракции (74 ч) и дает выход 2,27% (в пересчете на содержание сухой массы). В другой работе Виджая и др. исследовали аллергенные свойства коллагена из кожи рыбы Паранг-Паранг. Выделение коллагена проводили с использованием 0,1 М NaOH в течение 12 ч, а перед экспериментом его гидролизовали с использованием 0,5 М уксусной кислоты (AcOH). Содержание неколлагенового белка составило 0,2163 мг/мл при выходе 1,915%. Говиндхарадж и др. исследовали использование коллагена, полученного из кожи угря (тип I), для приложений 3D-печати. Конечный выход коллагена составил около 4,2%. Сообщалось о аналогичном результате, при котором выход коллагена, извлеченного из рыбы-угря, составил 4,7% . Ахмед и др. исследовали использование бактериальных коллагенолитических протеаз (CP) для извлечения коллагена из кожи рыб в качестве альтернативного метода. Для производства CP они использовали две бактерии, Bacillus cereus FORC005 и Bacillus cereus FRCY9-2. Общий выход коллагена при обработке бактериями и в сочетании с кислоторастворимым коллагеном составил 188 и 177 г/ кг соответственно, что было больше, чем выход только при кислотной экстракции (134,5 г/ кг). Другим подходом к извлечению коллагена из кожи рыбы является использование воды, подкисленной CO2, которая использовалась для выделения коллагена из атлантической трески (Gadus morhua). Общее содержание пролиноподобных аминокислот в коллагене, экстрагированном подкисленной водой, составило 151/1000 остатков, с выходом экстракции 13,8% (по массе).
2.1.2. Рыбья чешуя Рыбья чешуя составляет значительное количество отходов рыбоперерабатывающей промышленности. Недавние исследования показали, что коллаген, полученный из рыбьей чешуи, обладает свойствами, типичными для коллагена I типа, состоящего из двух α1-цепей и одной α2-цепи. Исследование коллагена из чешуи тилапии (Oreochromis sp.) показало высокую температуру денатурации (57,9–79,0 ° C), что, возможно, связано с его высоким содержанием аминокислот и более высокими внутри– / межцепочечными связями (водородные связи, диполь-дипольные связи, ионные связи и ван-дер-ваальсовы взаимодействия). Напротив, коллаген, выделенный из чешуи свежего карпа (Cyprinus carpio), показал низкую температуру денатурации (32 °C). Коллаген из чешуи тилапии, сома, помфрета и макрели требует более высокой температуры экстракции (диапазон 16,6–19,03 °C) и более длительного времени экстракции (77,51 ч) с более низким выходом экстракции (0,13%) по сравнению с кожей рыбы (4,3%). Коллаген из рыбьей чешуи также обладает надлежащими свойствами водопоглощения (13,3%) и удерживания (15%), что делает его пригодным для медицинского и терапевтического применения. Раневая повязка на основе коллагена (паста и лист) из чешуи тилапии и серой кефали продемонстрировала отличную антимикробную активность против золотистого стафилококка и кишечной палочки методом дисковой диффузии. Более того, раневая повязка обладала высокой способностью закрывать раны (до 99,63%), что указывает на роль коллагена рыбьей чешуи в ускорении реэпителизации. Однако из-за высокого содержания кальция (16-59% от массы минерала) в рыбьей чешуе декальцинацию необходимо проводить с помощью этилендиаминтетрауксусной кислоты (ЭДТА).
2.1.3. Рыбьи кости Коллаген из рыбьей кости обладает свойствами коллагена I типа, состоящего из двух цепей α1 и одной цепи α2. Исследование коллагена из костей тилапии (Oreochromis mossambicus) показало температуру денатурации 32,5 °C. Коллаген из рыбьих костей тилапии, сома, помфрета и скумбрии требует высокой температуры экстракции (16,6–19,03 ° C) и меньшей продолжительности экстракции (73,16 ч) по сравнению с рыбьей чешуей и кожей, а также имеет более низкий выход экстракции (0,64%) по сравнению с рыбьей кожей . Рамли и др. сообщили, что коллаген из кости Lutjanus sp. с выходом 4,535% (при концентрации белка 8,815 мг / мл) может быть использован в качестве природного противоопухолевого средства. Высокоинтенсивные импульсные электрические поля (PEF) являются одним из основных подходов к извлечению коллагена из рыбьей кости. В исследовании, проведенном Им и его коллегами, для выделения кальция, хондроитина и коллагена из отходов рыбьих костей применялся комбинированный метод полубионной экстракции (SBE) и PEF-обработок. В методе SBE процесс переваривания и всасывания в желудочно-кишечном тракте человека моделируется посредством повторяющейся кислотной и щелочной экстракции в различных диапазонах рН. Используя PEF 22,79 кВ/см, авторы извлекли 3,87 мг / мл коллагена, а комбинированный метод PEF и SBE был признан эффективным для выделения коллагена, кальция и хондроитина из рыбьей кости.
Та же группа в недавнем исследовании достигла максимального выхода коллагена в 16,13 мг / мл из рыбьих костей с использованием 1% пепсина при прочности PEF 20 кВ / см. Обессоливание также предлагается в качестве важного процесса при извлечении костного коллагена из-за высокого содержания в нем гидроксиапатита и кальция, которые удаляются EDTA или HCl во время предварительной обработки; однако использование HCl может привести к разрушению коллагена.
2.1.4. Рыбий хрящ Коллаген из рыбьего хряща состоит преимущественно из коллагена II типа и некоторых других типов коллагена в незначительных количествах, таких как тип IX и тип XI, обнаруженных в носовом хряще хоки (Macruronus novaezelandiae). Коллаген I типа содержится в хрящах Sphyrna lewini, Dasyatis akjei и Raja porosa. В хрящевой ткани амурского осетра (Acipenser schrenckii) коллаген I типа был обнаружен в солюбилизированном кислотой и солями коллагене, а тип II с другими второстепенными типами был обнаружен в солюбилизированном пепсином коллагене. Сообщалось, что коллагены, полученные из хряща Хоки, имеют сходный набор α-цепей, аминокислотный состав и структуру с коллагенами в хряще млекопитающих; и они могут иметь потенциал в качестве биоматериалов для лечения заболеваний, связанных с хрящом. Физико-химические и антиоксидантные свойства коллагена, выделенного из серебристой акулы (Carcharhinus albimarginatus), были оценены Jeevithan et al. Из этого хряща были извлечены кислоторастворимый коллаген II типа (ASC), солюбилизированный пепсином коллаген (PSC) и желатин II типа. Температура денатурации желатина II типа составила 32,5 °C, что выше, чем у двух других коллагенов (PSC и желатина II типа). Однако антиоксидантная активность в отношении 1,1-дифенил-2-пикрилгидразильных радикалов и восстанавливающая способность PSC были выше, чем у ASC II типа и желатина II типа. Коллагены, выделенные из серебристой акулы, могут быть подходящим кандидатом для биомедицинского применения благодаря их более высокой антиоксидантной активности. В другом исследовании Luo и соавт. [61] получили ASC и PSC из хрящей сибирского осетра (Acipenser baerii) с выходом 27,13 ± 1,15% и 14,69 ± 0,85% соответственно. Согласно результатам, коллагены из этого хряща могут быть подходящей альтернативой коллагенам млекопитающих II типа.
Коллаген рыбьего хряща имеет более низкую температуру денатурации, чем бычий коллаген, в диапазоне от 26,3 ° C до 35,9 ° C, что связано со средой обитания вида; например, низкая температура денатурации коллагена hoki collagen соответствует среде обитания в холодной воде. Альтернативно, коллаген кеты (Oncorhynchus keta) денатурируется при 19 °C, в то время как коллаген акулы денатурируется при температуре около 30 °C. Такая температурная нестабильность ограничивает применение некоторых биоматериалов, полученных из коллагена, в медицине человека. Поэтому необходимы дальнейшие исследования, чтобы найти столь же устойчивую альтернативу рыбьему коллагену с более высокой температурой денатурации, которая более удобна для биомедицинских применений и могла бы гарантировать лучшие характеристики с точки зрения термической и механической стабильности. Помимо термической стабильности, состав / структура коллагена должна быть максимально схожа с коллагенами млекопитающих, особенно для биомедицинских применений.
3. Методы извлечения коллагена
На основе морских источников могут быть использованы различные методы извлечения. Однако общая процедура выделения коллагена включает подготовку, экстракцию и извлечение (рисунок 2 b).
Приготовление в основном состоит из промывания, очистки, отделения частей животного происхождения и уменьшения размера путем разрезания или измельчения образцов для облегчения последующей предварительной обработки образцов. После получения препарата проводится мягкая химическая предварительная обработка для повышения эффективности экстракции и удаления неколлагенистых веществ. Как правило, в зависимости от сырья и метода экстракции могут проводиться различные предварительные обработки (щелочная или кислотная). Предварительная обработка используется разбавленной кислотой или основанием для разрушения сшитого коллагена перед экстракцией из-за наличия сшитого коллагена в соединительной ткани животных. Действительно, происходит частичный гидролиз, который сохраняет цепи коллагена неповрежденными.
При кислотной форме предварительной обработки сырье погружают в раствор кислоты. Проникающий раствор в структуру коллагена позволяет ему набухать в два или три раза по сравнению с первоначальным объемом, что приводит к разрыву нековалентных межмолекулярных и внутримолекулярных связей. Предварительная щелочная обработка в основном выполняется с использованием гидроксида натрия (NaOH) и гидроксида кальция (Ca(OH)₂) в течение периода, который может занять от нескольких дней до нескольких недель. Однако использование NaOH более удобно из-за более высокой способности к набуханию, что облегчает извлечение коллагена за счет увеличения скорости переноса массы в тканевой матрикс.
Более того, перед этапом экстракции требуется деминерализация сырья для повышения эффективности извлечения коллагена из частей тела с высоким содержанием минералов, таких как кости, хрящи и чешуя. Обычно деминерализацию можно выполнить с использованием либо EDTA, либо HCl.
Коллагеновые волокна представляют собой тройную спираль со стабильными межмолекулярными и внутримолекулярными водородными связями, которые делают коллагеновые волокна нерастворимыми в воде. Следовательно, для экстракции требуется использование специальных методов экстракции, чтобы увеличить солюбилизацию коллагеновых белков и завершить их выделение. Экстракция солюбилизированного кислотой коллагена (ASC), экстракция солюбилизированного пепсином коллагена (PSC), экстракция глубоким эвтектическим растворителем (DES) и экстракция сверхкритической жидкостью (SF) являются основными методами, описанными в литературе для выделения коллагена из рыбных субпродуктов.
3.1. Процедура кислотной экстракции
ASC известен тем, что коллаген извлекается только кислотой. Кислоты (такие как HCl и AcOH) гидролизуют тройную спираль коллагена и солюбилизируют его отдельные цепи в растворе, где происходит деполимеризация тяжелых белков в более короткие пептиды (0,3–8 кДа). Взаимодействие кислоты с молекулами коллагена разрушает поперечные связи, присутствующие в коллагеновой спирали, и повышает эффективность извлечения. Поэтому представляет большой интерес исследовать эффективность экстракции с использованием различных кислот для максимального повышения чистоты и выхода экстрагируемого коллагена. Расщепление тройной спирали, осуществляемое кислотами, схематично показано на рисунке 4.
AcOH является одним из наиболее распространенных соединений, с помощью которых осуществляется извлечение коллагена из животных и морских источников. Диапазон концентраций кислотного экстракционного раствора составляет от 0,5 до 1 Мкл, что позволяет расщеплять внутри- и межмолекулярные поперечные связи, не влияя на структуру коллагеновых цепей. Хотя в большинстве исследований исследователи используют 0,1 или 0,5 М AcOH для извлечения коллагена из кожи рыб, Тан и соавт. исследовали эффект использования различных кислот (AcOH, соляная кислота, лимонная кислота и молочная кислота, W: V = 1: 50), соотношений жидкости и твердого вещества и различного pH (1.8, 2.1, 2.4, 2.7 и 3.0) об извлечении коллагена из кожи сома различными методами (кислотными, с использованием гомогенизации и пепсиновых методов экстракции). Метод с использованием пепсина и гомогенизации (PHSC) показал самое высокое извлечение белка (64,19% при рН 2,4 в пересчете на HCl). Что касается метода кислотной экстракции, то скорость извлечения белка, выделенного из кожи с помощью HCl при рН 2,4, составила 42,36% (самый высокий показатель), за которым следует экстракция с рН 2,7 AcOH (39,45%). Это исследование противоречило другим исследованиям, в которых сообщалось о более низком выходе экстракции коллагена HCl по сравнению с AcOH. Причина может быть в различных концентрациях используемой кислоты, а также в том, что рН смеси не поддерживался на начальном уровне, который имел тенденцию меняться со временем экстракции.
Влияние AcOH в диапазоне 0,2–1,0 Мкм на извлечение коллагена из кожи подошвы рыбы было определено Arumugam et al., в то время как остальные переменные были постоянными. Выход коллагена постепенно увеличивался с увеличением концентрации AcOH, так что максимальный выход составил 15,968 мг/ г при 0,6 М AcOH. Однако при превышении 0,6 М выход коллагена снижался.
Янг и др. изучали взаимодействие между молекулами коллагена и раствором AcOH. Агрегированное состояние молекул коллагена и концентрация AcOH были связаны друг с другом таким образом, что критическая концентрация агрегации коллагена увеличилась с 0,518 до 1,581 мг/ мл при изменении концентрации AcOH с 0,1 до 2,0 Мг/мл. Было исследовано реологическое поведение раствора коллагена в зависимости от концентрации AcOH, чтобы понять взаимодействие между молекулами коллагена и кислотным растворителем. Все образцы показали поведение при истончении при постоянном сдвиге, которые могут быть использованы в качестве биоинъекций для 3D-печати. С увеличением концентрации AcOH повышалась способность коллагена к текучести, что могло быть связано с уменьшением вязкости. В дополнение к AcOH для извлечения коллагена использовались лимонная и молочная кислоты.
3.2. Процедура извлечения AcOH с помощью пепсина
Экстракция AcOH пепсином является вторым основным методом извлечения коллагена, который позволяет расщеплять телопептидные участки тройной спирали, облегчая выщелачивание коллагеновых пептидов в растворе и увеличивая выход экстракции. PSC - это известный пепсин, который добавляют в процесс экстракции (рисунок 3). Поэтому во многих исследованиях использовалась предварительная ферментативная обработка с использованием пепсина для расщепления телопептидных концов коллагеновых цепей, чтобы облегчить удаление белков из оставшегося матрикса. Несколько факторов играют решающую роль в эффективности методов экстракции AcOH с использованием пепсина, таких как концентрация пепсина, время гидролиза и соотношение твердое/ жидкое (S / L) в коллагене, солюбилизированном пепсином, которые необходимо оптимизировать для получения более ценных результатов. Влияние концентрации пепсина на выход экстракции растворимого в пепсине коллагена исследовали при неизменных других параметрах экстракции. Увеличение концентрации пепсина (с 800 до 1200 Ед/г) привело к впечатляющему увеличению выхода выделения (с 66,35% до 79,93).
Рисунок 3
Разница между методами извлечения кислоторастворимого коллагена (ASC) и пепсинорастворимого коллагена (PSC).
Более того, Джунианто и соавт. исследовали влияние концентрации как AcOH, так и фермента пепсина при выделении коллагена из кожи рыбы нилем. Для этой цели они использовали три различные концентрации AcOH и фермента пепсина. Результаты показали, что максимальный выход экстракции коллагена (6,18%) был получен при комбинированной обработке концентрации 0,7 М раствора AcOH ферментом пепсином в 1,0%.






![Голодные игры [-1 неделя] Похудение, Диета](https://cs14.pikabu.ru/post_img/2024/02/26/4/1708924391137442724.jpg)
![Голодные игры [-1 неделя] Похудение, Диета](https://cs13.pikabu.ru/post_img/2024/02/26/4/1708923642115583608.jpg)
