Первый опыт работы с химическим никелированием
Приветствую вас, друзья! Хочу рассказать про свой первый опыт никелирования. Он не совсем удачный, но интересный и показательный.
Что такое никелирование?
Никелирова́ние — обработка поверхности изделий путём нанесения на них никелевого покрытия. Толщина наносимого покрытия обычно составляет от 1 до 50 мкм.
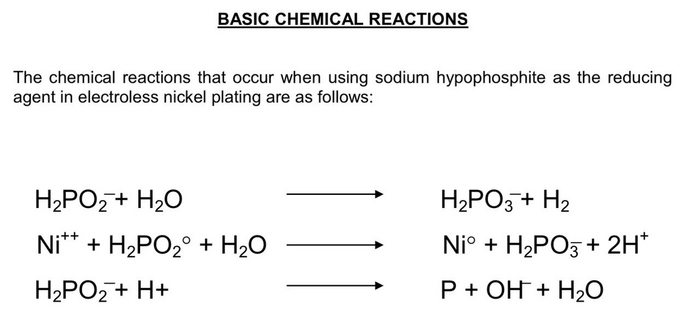
Процесс происходит по следующей реакции:
Для опыта мы использовали специализированные растворы для никелирования. Пока состав оглашать не буду, речь пойдет об этом тогда, когда всё выйдет.
Смешение и разведение раствора:



После разведения раствора нам необходимо его подогреть. И тут у нас были проблемы, так как не было плиты. Мы решили всё это чудо нагреть феном :) И сделать водяную баню, чтобы сохранить тепло. Нормальная рабочая температура для раствора 82-91 градус, оптимальная - 88.


В прогретый раствор до 82-91 градусов необходимо опустить предварительно обезжиренный кусок металла. Как правило, никелированием обрабатывают металлические изделия, изготовленные из стали либо других металлов и сплавов, в частности меди, цинка, алюминия, реже марганца, титана, вольфрама или молибдена. Мы работали со сталью СТ3. Вот так выглядела заготовка "до"
Опустили заготовку в раствор.
Изначально мы поддерживать температуру старались при помощи водяной бани, но температура всё равно упала. Пришлось направить фен на колбу с раствором.
И у нас был косяк, в проволоке находился цинк. Он вступил в реакцию с раствором и стал образовать осадок.
После 30 минут никелирования получилось вот такое покрытие.
Такой результат уважения недостоин. Нет глянцевого и блестящего покрытия из-за опустившейся температуры и присутствия цинка в проволоке. Кстати, вот что случилось с проволокой после эксперимента:
Никель искренне пытался хорошенько лечь на поверхность, но в итоге сдался и не смог.
Спасибо за прочтение! В планах устранить все недостатки и показать действительно стоящий результат!
Думаете, что бы такое посмотреть вечером? Есть ответ
Типичная ситуация: надо выбрать фильм на вечер, вы крутите один трейлер за другим, потом все это надоедает, вы бросаете это дело и идете листать ленту. То есть смотрите короткие видео, но в них чего-то не хватает.
Сокращайте ненужные усилия и получайте больше радости: листайте ленту с короткими видео, в которых всего достаточно. Такие водятся на NUUM — свежей платформе для видео, стримов и трансляций. Смотрим, снимаем и зарабатываем!
Реклама ООО «Джумс Проекты», ИНН: 7709484636
Чистая правда о Fe(OH)2, которую решили не упоминать
Многие из нас в школе наблюдали получение гидроксида железа II, он представляет из себя грязный серо-зеленый осадок, и при подготовке к ЕГЭ нам говорят то же самое. Однако, это не правда, цвет этого осадка обусловлен примесью железа III, что образуется из-за растворенного в воде кислорода воздуха и окисления солей железа II при хранении.
На самом же деле чистый Fe(OH)2 является бесцветным, но для простоты составители ЕГЭ, говоря о нем, имеют ввиду этот серо-зеленый осадок, так как мало кто на практике видел его в чистом виде.
А сегодня я вам его покажу ;)
Для получения чистого гидроксида железа II необходима бескислородная среда, она достигается длительным пропусканием инертного газа через растворы, то есть вытеснением растворенного кислорода инертным газом, например азотом, либо вакуумированием.
В лаборатории, где я работаю, есть специальные вакуумируемые ячейки, одной из таких я и воспользуюсь. В кварцевую кювету ячейки я налил раствор хлорида железа II, а в стекляненный отросток - калиевую щелочь. Далее ячейка закрывается и вакуумируется несколько минут.
Казалось бы, завакуумировал и сливай растворы уже! Но в исходном FeCl2, и без растворенного в воде кислорода, полно железа III. Ну знаете, Sigma Aldrich поставляет самые чистые реактивы, но они чистейшие лишь на небольшое время после поставки, а не спустя пару десятков лет.
Благо у нас в лабе есть высокоинтенсивная УФ лампа, которая позволяет фотохимически восстанавливать некоторые металлы. Таким образом и лишнее железо III будет восстановлено до II и ячейка останется под вакуумом.
И вот настал момент истины, смешение растворов. Особо глазастые могут заметить, что осадок все таки немного отдает зеленью, это из-за того, что у меня не получилось удалить кислород полностью. Ну или надо было подержать кювету у лампы немного подольше.
Но на этом демонстрация не заканчивается, отсталось лишь показать, что в присутствии кислорода воздуха, красивый белый осадок сразу начинает зеленеть и темнеть. Для этого надо всего лишь открыть ячейку.
И вот в вашей жизни на один химический факт больше. Гордитесь, вам довелось увидеть кадры, которые не увидеть в школьной, да и не в каждой университетской, лаборатории.
Как всегда ваш @Danushkis, и до новых встреч!
Золотой снегопад
Сначала крупные заметные кристаллы образуются на стенках колбы, поскольку они холоднее массы раствора. Затем, по мере остывания, в объеме начинают появляться сначала едва заметные лишь по блеску, а потом всё более крупные золотистые чешуйки. И чем больше они становятся, тем быстрее опускаются на дно колбы, ведь иодид свинца (который и образует их) – весьма тяжелое вещество (6,16 грамма на 1 кубический сантиметр). В результате все чешуйки опустятся на дно.
Небольшая предыстория видео
Еще пару месяцев назад я нашел здесь, на Пикабу, давний пост с опытом «Золотая метель» и задался целью его повторить. У меня в лаборатории, конечно же, не оказалось нужных реактивов (ацетат свинца и иодид калия не особо нужны в моей работе.), поэтому пришлось попросить у коллег. Ацетат свинца пришлось заменить нитратом свинца, однако именно он и нужен согласно оригинальному рецепту.
Забавно, но всё получилось буквально с первого раза. Сначала я хотел просто оставить результат для украшения своей лаборатории, но потом решил, что снять небольшое, но красивое видео тоже будет неплохой идеей. Поэтому опыт был поставлен заново и с учетом того, что результат будет снят на видео.
Снял несколько фрагментов и уже смонтировал видео, чтобы создать этот пост, но COVID-19 был сильнее и несколько дней я лежал в почти бреду с температурой около 40 градусов. Поэтому пост пришлось вынужденно отложить почти на полторы недели.
Сразу прошу прощения за нелепый монтаж, поскольку навыками монтирования видео я практически не обладаю. Местами видео ускорено в сотни раз и на это указывает число в нижнем правом углу кадра. Всего же от момента выключения нагрева колбы, до окончания кристаллизации прошло около 3 часов.
Все реагенты и их пропорции и навески вы найдете в оригинальном посте.
К сожалению, видео пришлось сделать с очень низким битрейтом (3 Мб/с), поскольку Пикабу видео большего размера не смог обработать.
Конечно же, спасибо всем, кто дочитал. С наступающим Новым годом!
Как грызть химию
Привет, химикам!
Вопрос от праздного любопытства: интересно как химия работает в мире. То есть не глубины взаимодействий и попытки предсказать новые вещества, а просто азы что б понять основы химических процессов вокруг. Не очень глубоко но не так и объемно. Ну например объяснить мог почему в железных канистрах кислоты возят.
советуйте книги, курсы, блогеров заодно.
Всех обнял
Топ 25 интересных устройств для любителей экспериментов по физике и химии
1) Двигатель Стирлинга
Интересная экспериментальная модель двигателя Стирлинга, выполняющее преобразование тепловой энергии в механическое движение. Ссылка на источник.
2) Эксперименты со светом
Специальная призма-куб для опытов с дисперсией света. ссылка
3) Эксперимент на водородных топливных элементах
Экспериментальный обучающий набор для любителей физики и химии, при помощи которого можно получить чистую энергию при помощи электролиза. Ссылка
4) Экспериментальный автомобиль
Экспериментальная модель автомобиля, которая работает от газов, выделяемых в колбе. ссылка
5) Миниатюрный бензиновый двигатель
Интересная модель бензинового двигателя, также его можно поместить в самодельную радиоуправляемую модель. ссылка
6) Водородная машина
Еще одна модель для изучения принципа работы водородного двигателя. ссылка на источник
7) Турбийон
Модель турбийона для изучения принципа работы механики, это механизм, который компенсирует земное притяжение. ссылка
8) Электрофорная машина
Электростатический генератор, то есть электрическая машина для генерирования высокого постоянного напряжения. ссылка
9) Модель дизельного двигателя
Модель для изучения принципа работы двигателя внутреннего сгорания. ссылка
10) Горизонтальная камера для электрофореза
Электрофорез — метод разделения макромолекул (белков и нуклеиновых кислот, а также их фрагментов) под действием электрического поля. ссылка
11) Механическая машина-рисовальщик
Суперинтереснейший набор для самостоятельной сборки и изучения механики, после сборки получится прикольная рисующая машина. ссылка на источник
12) Опыты с линзами
Набор для изучения рефракции света с помощью линз и лазера. ссылка
13) Аэродинамика
Модель для демонстрации принципа подъема летательного аппарата, а именно подъемной силы крыла самолетов. ссылка
14) Ручной генератор
Демонстрация модель генератора с ручным приводом, электромагнитный эксперимент по физике. ссылка
15) Поляризация
Интересное оборудование для демонстрации поляризации света. ссылка
16) Молекулы
Набор из 440 деталей для сборки моделей молекул. ссылка на источник
17) Металлы
Различные материалы (алюминий, цинк, свинец, медь, латунь, железо) нарезанные в маленькие кубики для использования в различных экспериментах. ссылка
18) Магнитное поле
Устройство для демонстрации явления магнитного поля. ссылка
19) Радиометр
Радиометр Крукса (или вертушка Крукса) — четырёхлопастная крыльчатка, уравновешенная на игле внутри стеклянной колбы с небольшим разрежением. При попадании на лопасть светового луча крыльчатка начинает вращаться. Причиной вращения служит радиометрический эффект — возникновение силы отталкивания за счёт разницы кинетических энергий молекул газа, налетающих на освещённую, нагретую сторону лопасти и на противоположную, более холодную. ссылка
20) Пароход
Интересный эксперимент со свечкой и паром, приводящим в движение лодку. ссылка на источник
21) Закон Архимеда
Закон Архиме́да — закон гидростатики и аэростатики: на тело, погружённое в жидкость или газ, действует выталкивающая сила, численно равная весу объёма жидкости или газа, вытесненного телом. Как подводная лодка может погружается в воду, плавать и всплывать? Ссылка
22) Электромагнитное поле
Прибор для демонстрации линий индукции магнитного поля. ссылка
23) Электричество из картошки
Простой эксперимент для получения электричества из овощей. ссылка
24) Плазма
Прибор чувствительный к прикосновениям с установленным внутри электродом. На электрод подаётся переменное высокое напряжение с частотой около 30 кГц. Внутри сферы находится разреженный газ (для уменьшения напряжения пробоя). В качестве наполнения могут выбираться разные смеси газов для придания «молниям» определённого цвета. Ссылка
25) Опыт с выращиванием кристаллов
Интересных химический реактив для увлекательного опыта, который позволяет вырастить кристаллы у себя дома. Ссылка на источник.
Помните! При проведении опытов или экспериментов, не забывайте о технике безопасности.