Это должен был быть первый пост который я хотел сделать, но что-то пошло не так)
Я попытаюсь рассказать о самой важной части химии, а именно о химической связи и атомах. Причем, попытаюсь показать эволюцию представлений о строении веществ вокруг нас. Придется окунуться в историю.
Представьте, что играет лира, @castiar бегает и подсматривает за Зевсом, вы пьете вино разбавленное водой, и Дионис ваш лучший друг. Но сегодня нашей спутницей пусть будет Афина.
Древняя Греция, где-то V—IV веков до н. э. , в философии существуют два принципа:атомизм и континуум. Атомизм учит о том, что материя состоит из атомов и пустоты. Атомы идеальны, и именно их движение причина всего. Континуум учит, что материю можно делить бесконечно,и конечно же она идеальна.
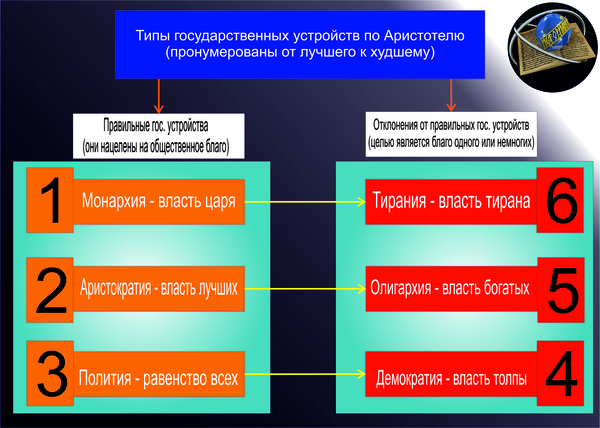
Атомизм поддерживал Демокрит, после Платон,об экспериментах никто и не думал, все были уверены, что до всего можно дойти умом. Самым знаменитым критиком и противником атомизма был Аристотель(а еще самый знаменитый философ,гений, плейбой, филантроп... так так... не туда,ученик Платона кстати). Имя Аристотеля и сейчас авторитет, именно по этой причине атомизм был забыт до 17-го века, только в 17-ом веке стали опять говорить про атомы, и то с большим трудом.
Критика атомизма была проста:
первое, если есть пустота, то она "ничто", а как может быть "ничто"?
Природа не терпит пустоты (лат. natura abhorret a vacuo) — Аристотель.
второе, если атомы идеальны, как они цепляются? Если у них есть "крючки", то значит эти "крючки" часть атома, и он уже не идеален, а состоит из каких-то частей.
Атомизм стали поддерживать хоть кто-то, только в в XVI-XVII веках, и то на них сыпалась критика, от сторонников Аристотеля. Полностью он возродился, только в начале XIX века. Как только всё стало базироваться на экспериментальных данных, так сразу стали появляться научные теории.
В начале XIX века Дальтон открыл несколько новых эмпирических закономерностей: закон парциальных давлений (закон Дальтона), закон растворимости газов в жидкостях (закон Генри-Дальтона) и, наконец, закон кратных отношений (1803). Объяснить эти закономерности (прежде всего закон кратных отношений), не прибегая к предположению о дискретности материи, невозможно. В 1808 году Дальтон изложил свою атомистическую гипотезу в труде «Новая система химической философии». Вики.
Основные положения теории Дальтона состояли в следующем:
1. Вещества не сплошные, а дискретны, состоят из мельчайших частиц(атомов), различия между веществами лишь различия в свойствах этих частиц.
2. Атомы одного вещества одинаковы. Тождественны, и неразличимы, а еще атомы неделимы и неизменны.
3. Частицы различных веществ различны, по свойствам, по массе.
4. Атомы различных элементов могут объединяться в определенных соотношениях.
5.Важнейшее свойство атомов, атомный вес(впоследствии мы узнаем, что заряд ядра).
Ну тут и началась химия, теория хороша, но вопросов стало больше чем было. Что за атомы, какой размер, из чего состоят, почему держатся, и т.д. и т.п.
Еще Дальтон ввёл символы химических элементов, и писал их в таблицу.
Как видите, его массы во многом неверны. Но в правильном определении масс, помог закон Авогадро, который утверждал, что одинаковые объемы газов, содержат одинаковые количества молекул газа.
Во времена Ломоносова еще писали формулу воды то как HO, то как HO2, то еще черти пойми как. Но в итоге разобрались.
С развитием органической химии стало ясно, что вещества это не просто набор атомов, а атомы еще и как-то соединены, возможно образуют структуру. Появляется понятие "валентность". Было несколько ученых которые вводили это понятие , но их идеи не сразу были приняты, а решающее значение сыграл Кекуле. (он еще структуру Бензола придумал)
Кекуле утверждал, что у атома помимо веса, есть еще одно свойство основность(валентность), это способность атома соединяться с другими атомами. В качестве примера метан CH4,где углерод соединен с 4 атомами водорода.
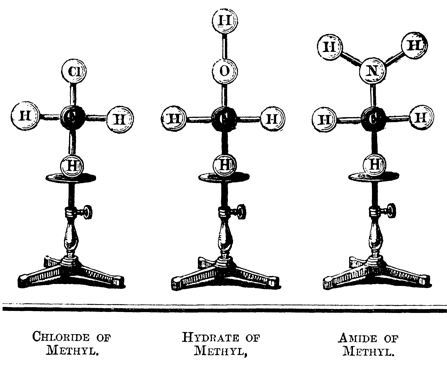
Бутлеров улучшил подход Кекуле, и объяснил химическое различие атомов в молекуле. В 1865 г. А. фон Гофман продемонстрировал первые шаростержневые модели, в которых роль атомов играли крокетные шары.
А следом и в учебниках стали рисовать структуры.
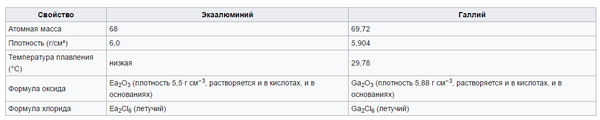
Пару лет спустя. В 1869 году, Менделеев открыл периодический закон, и придумал систему химических элементов. Она настолько была хороша, что Дмитрий Иванович очень точно предполагал свойства еще не открытых элементов. Вы только посмотрите на это, он гений, просто гений. Слева предсказанные Менделеевым свойства, справа экспериментальные данные.
Если я я сделаю на компьютере квантовый расчет, боюсь по некоторым пунктам у меня ошибка будет больше! Это просто феноменально. Структура таблицы и причина периодичности, стала ясна только в первой половине 20 века, после открытия строения атома, и появления уравнения Шредингера.
О 20 веке, и современных представлениях я напишу в следующем посте.