Всем привет, на связи психиатр, психотерапевт, в прошлом судебно-психиатрический эксперт. В этом посте попробуем разобраться, можно ли подобрать антидепрессант с помощью генетического тестирования и какие реальные границы есть у этого метода.
Фармакогенетическое тестирование сейчас предлагают многие лаборатории. В справочных материалах и рекламе обычно используются примерно такие формулировки (цитаты с сайтов пары известных лабораторий):
"Расширенное генетическое исследование позволяет оценить индивидуальную эффективность и безопасность более 30 самых распространённых антидепрессантов и нейролептиков".
"Исследование помогает сократить время подбора препарата и дозировки до минимума благодаря индивидуально рассчитанному риску токсичности (риску побочных эффектов)".
"Прогнозирование эффективности терапии и вероятности развития побочных эффектов перед началом терапии ингибиторами обратного захвата серотонина и норадреналина".
Формально здесь вроде бы даже нет прямой лжи. Но, скажем прямо, подобные формулировки вводят в заблуждение. Чтобы понять, где именно здесь лукавство, придётся немного залезть в скучное и нудное. Мы все знаем, что действие лекарств в определённой степени индивидуально. Один и тот же препарат у разных людей может вызывать разные побочные эффекты, работать по-разному или не работать вовсе. Особенно это заметно для препаратов, влияющих на центральную нервную систему - слишком уж сложная это система.
Причин такой вариабельности много, и одна из них - то, как именно метаболизируется препарат. Антидепрессант, попадая в организм, в печени окисляется ферментами, из-за чего теряет активность (некоторые препараты, наоборот, приобретают активность, но это уже другая история), становится более водорастворимым и легче выводится. Если эта система ферментов работает быстрее или медленнее обычного, концентрация препарата в крови будет другой, выше или ниже ожидаемой. Соответственно изменится и эффективность.
Для антидепрессантов (СИОЗС, СИОЗСН, трициклических) достоверно выделены два ключевых гена ферментов - CYP2D6 и CYP2C19. Они определяют, насколько активны соответствующие ферменты у конкретного человека. Важно помнить, что эти ферменты окисляют не только антидепрессанты, но и множество других лекарств. У обоих генов существуют вариации, которые условно определяют "мощность" ферментной системы. Грубо говоря, фермент может работать нормально (как у большинства людей), быстрее или медленнее. Если фермент "быстрый", препарат выводится быстрее, если "медленный" - дольше.
Если упростить, представьте трёх человек, которые принимают одну и ту же дозу антидепрессанта, например 10 мг. Первый с обычным метаболизмом: он получает ровно ту концентрацию в плазме, на которую и рассчитывали в клинических исследованиях. Второй с "быстрым" метаболизмом: его 10 мг по факту эквивалентны примерно 5 мг у первого. Третий с "медленным" метаболизмом: его 10 мг это уже что-то ближе к 20 мг для первого. Получается, что чтобы поставить их в равные условия, первому нужно оставить 10 мг, второму повысить дозу до 20 мг, а третьему снизить до 5 мг. Клинически мы, скорее всего, увидим у первого какой-то эффект (хотя и это не гарантировано), у второго - отсутствие эффекта, а у третьего - повышенный риск побочных эффектов. Модель, конечно, очень примитивная, но она хорошо иллюстрирует сам принцип.
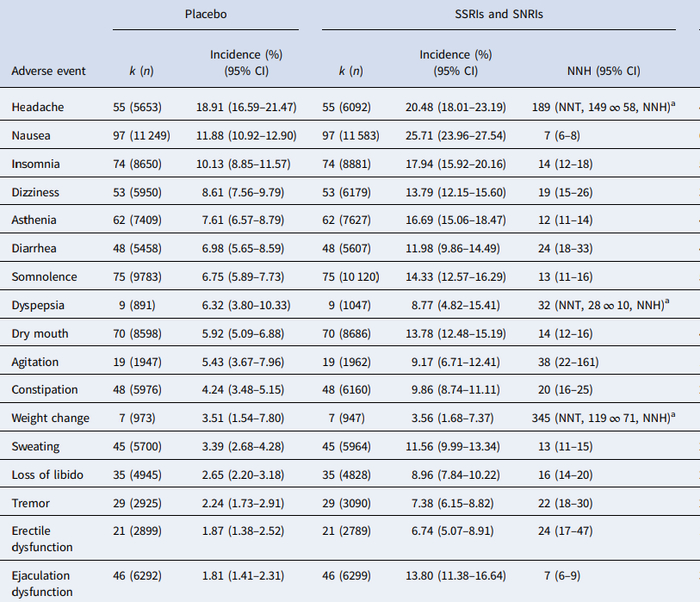
Если посмотреть на статистику по популяции, то основные данные есть для Европы. По CYP2D6 усреднённая картина такая: около 5-10% людей имеют отсутствующий или почти не работающий фермент, 10-15% - "медленный", 65-80% - нормальный и до 10% - "ультрабыстрый". Этот фермент влияет на метаболизм пароксетина, флуоксетина, венлафаксина, дулоксетина и трициклических антидепрессантов (амитриптилин, имипрамин, кломипрамин).
По CYP2C19 распределение другое: 2-5% - отсутствующий или практически не работающий фермент, 25-30% - "медленный", 35-45% - нормальный, 20-25% - "быстрый" и до 5% - "ультрабыстрый". Он влияет на метаболизм эсциталопрама, циталопрама, сертралина и флувоксамина. То есть довольно большая часть людей, принимая стандартную дозу препарата, фактически получает либо больше, либо меньше ожидаемой дозы.
Собственно, именно гены CYP2D6 и CYP2C19 и предлагают определять лаборатории. По результатам теста человеку сообщают фенотип его ферментной системы и делают выводы о "подходящих" или "неподходящих" препаратах. И вот здесь начинается самое важное ограничение: такое тестирование не показывает, какой антидепрессант будет эффективным. То, что препарат метаболизируется "стандартно", совершенно не гарантирует, что он подействует. Поэтому фраза "оценить индивидуальную эффективность" по сути является лживой. Максимум, что мы можем сделать, так это предположить, что у конкретного человека стандартная доза приведёт к стандартной концентрации в крови. Но вот эффективность антидепрессанта уже совсем другой уровень, который пока непостижим для фармакогенетики. Точно также это исследование никак не гарантирует, что на стандартную концентрацию препарата в плазме не начнутся побочные эффекты, это невозможно предсказать.
Теоретически фармакогенетика может немного сократить время подбора лечения. Логика понятна: если мы видим, что определённый препарат будет метаболизироваться нетипично, мы либо не будем его выбирать, либо сразу скорректируем дозу. Однако на практике большинство пациентов всё равно попадает в самую большую группу с нормальным метаболизмом. Кроме того, CYP2D6 и CYP2C19 лишь часть картины. На метаболизм влияют другие ферменты, последующие этапы биотрансформации, состояние печени, возраст, пол, курение и лекарственные взаимодействия. Есть и ещё один важный момент: разные лаборатории используют разные панели, разные алгоритмы анализа и по-разному переводят генетические варианты в фенотипы. В итоге один и тот же человек может получить заметно разные рекомендации в разных лабораториях. Дело тут не в том, что лаборатории плохие, просто ген даже одного фермента это иногда сотни вариантов аллелей.
В реальных исследованиях влияние фенотипа фермента на концентрацию препарата в плазме действительно подтверждается, но оно гораздо менее наглядно и более вариабельно, чем в моем примере с тремя пациентами. Качественных исследований, показывающих влияние фармакогенетического тестирования на клинический процесс, пока немного, и их дизайн лично мне не кажется удачным. Результаты противоречивые и довольно скромные. Если обобщать ту информацию что есть, то на данный момент фармакогенетика в контексте антидепрессантов может несколько снижать риск побочных эффектов, но не демонстрирует существенного ускорения достижения клинического улучшения. Для среднего пациента этот метод пока не показывает заметной эффективности именно в плане подбора успешного лечения. Повторю ещё раз: фармакогенетическое тестирование не отвечает на вопрос, какой антидепрессант будет работать, оно лишь позволяет спрогнозировать особенности метаболизма некоторых препаратов, но на практике выходит, что и через это она влияет на лечебный процесс довольно слабо.
В национальных клинических руководствах фармакогенетические методы начали упоминать, но пока именно как упоминание, а не как фактор, определяющий тактику лечения. В этом плане Финляндия сейчас чуть впереди остальной Европы, в местных рекомендациях этот подход присутствует, и мы периодически используем фармакогенетические панели в практике. Мои практические ощущения пока совпадают с результатами исследований, это занимательно, но не особо помогает в процессе. На ум приходит пару случаев, когда нам могло бы помочь выполнение фармакогенетической панели на ранних этапах лечения, но оно было выполнено значительно позже.
В каких же случаях есть смысл задуматься о таком исследовании? На текущем этапе определённая рациональность есть, когда у пациента несколько препаратов вызывают выраженные побочные эффекты в обычных дозах, когда отмечается резистентность к лечению или когда пациент принимает множество лекарств по поводу других заболеваний. В этих ситуациях понимание особенностей метаболизма может немного повысить безопасность и, возможно, ускорить подбор терапии. Но это точно не будет полным решением проблемы, лишь один из вспомогательных инструментов в подборе терапии, и то он будет эффективным только в умелых руках.
Выполнять такое исследование без показаний, скорее всего, будет пустой тратой денег. Повторюсь, оно точно не даст ответа, какой антидепрессант окажется эффективным. В целом фармакогенетика в психиатрии действительно перспективное направление, но пока находящееся на этапе развития. Активное внедрение в рутинную практику на данный момент выглядит преждевременным: это очень индивидуальная история с не самым большим практическим выхлопом.
Думаю важно указать, что в медицине есть области, где фармакогенетика уже стала стандартом. Это области, где ген определяет либо саму возможность лечения, либо риск тяжёлой, иногда смертельной реакции (онкология, гематология, кардиология). Так что я с большой надеждой смотрю на фармакогенетику, но рекомендую вам понимать, что конкретно вы идете оценивать в лабораторию.
Дополнительно для интересующихся:
Вводим в поиск clinical pharmacogenetics implementation consortium genes-drugs - это рекомендации международного экспертного консорциума, который разрабатывает клинические рекомендации по тому, как использовать уже имеющиеся фармакогенетические данные при назначении лекарств. Там вы можете поискать лекарства, которые принимаете или назначаете и актуальную информацию по ним.
Попроще Table of Pharmacogenetic Associations FDA - официальная справочная таблица FDA, в которой перечислены известные связи между генетическими вариантами и лекарственными препаратами.