Здравствуй уважаемый 21 подписчик, и все, кто вдруг за каким-то делом решил почитать про источники ионизирующего излучения - ИИИ (ИИ - читай радиация), встречающиеся в природе.
Вместо предисловия: удивлен, что вообще кому-то стала эта тема интересна, т.к. обычно попытки в своем круге рассказать о чем то близком, приводят к примерно такому:
Сразу упомяну (чтобы не набежали профессора физтеха, ученые из ЦЕРНА и прочие Лауреаты нобелевских) все, что я тут пишу ¬– максимально упрощенно. Мы даже не будет сегодня вдаваться в виды излучений(альфа, бета, гамма и т.д.). Сегодня мы также не будем говорить про космическое ИИ.
ИИИ встречаются в природе повсеместно. В принципе все, что вы держите в руках, что едите, абсолютно вся мебель и любая органика радиоактивны. Это факт. Просто примите это и живите дальше. Слышишь читатель?! Ты тоже ИИИ.
Немного нырнем в теорию.
Причина ИИ всего одна: у всех, абсолютно у всех элементов периодической таблицы Менделеева есть изотопы: стабильные и нестабильные. Для тех, кто прогулял физику с химией вот вам определение из вики: Изотопы — разновидности атомов (и ядер) какого-либо химического элемента, которые имеют одинаковый атомный (порядковый) номер, но при этом разные массовые числа.
Если ты все еще ничего не понял из вышеописанного - поясню. Большинство элементов может имеет несколько форм (изотопов / нуклидов): нуклиды в стабильном ядерном состоянии (это все элементы от водорода до изотопа свинца-208), и их братья по заряду и электронной оболочке, но с другим числом нейтронов в ядре, которые как правило радиоактивны (считай со временем распадаются до более стабильных ядер). И собсно все. Говорят где-то там за уно-уно- пентием (115 элемент ) есть островок стабильности, но пока ученые до него не добрались и не подтвердили свою теорию, будем считать, что его нет.
Почему вообще происходит радиактивный распад нужно писать отдельный пост.
Здесь приведены все известные человечеству изотопы, радиоактивные и стабильные. https://ru.wikipedia.org/wiki/%D0%A2%D0%B0%D0%B1%D0%BB%D0%B8...
Монументальная таблица!
За тот факт, что за элемент представляет тот или иной атом и какими ХИМИЧЕСКИМИ свойствами он обладает – отвечают два параметра атома, выходящий один из другого: заряд ядра и строение электронной оболочки
За ФИЗИЧЕСКИЕ свойства элемента отвечает в том числе такой параметр как масса ядра.
То - есть у нас есть два изотопа одного вещества, один пусть будет стабильный, а другой радиоактивный: и они будут вести себе ОДИНАКОВО с точки зрения химии и по разному с точки зрения ФИЗИКИ. Это важно понимать.
Иными словами вы НИКАК не сможете разделить два изотопа химическими способами. Смиритесь. Разделение изотопов одного элемента основано на разнице физических свойств.
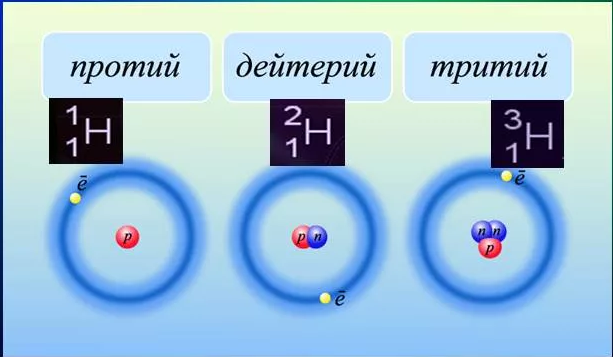
Такой пример - Вы пьете воду. В воде в природе два стабильных изотопа водорода: протий и дейтерий. Протий это тупо протон с электроном. Оторви у протия яйца, кхм элетрон и он будет чисто протоном. У дейтерия в ядре есть еще нейтрон.
В ядерном реакторе мы кроме того можем найти еще и тритий. У трития протон и два нейтрона.
Нейтроны дают только дополнительную массу ядру, но не добавляют заряд, т.к. сами его не имеют. Итого напихиваем в ядро дополнительной массы и меняем физические свойства атома.
Формула воды Н2О, соответственно если у нас в молекуле воды есть один(реже) или два(чаще) атома дейтерия, то такая вода называется тяжелой и у нее другие физические свойства в отличии от обычной воды. Так, например, температура плавления тяжелой воды на 3.82 градуса выше обычной воды. Меняются даже поверхностное натяжения и pH. Но если мы нальем вам в стакан даже тритиевую воду, вы скорее всего не поймете, что она радиоактивна (только если у вас есть бета чувствительный дозиметр). Природное содержание дейтерия 0,0115 ± 0,0070%. Период полураспада Трития 12 с хвостиком лет.
Сегодня нас интересуют радиоактивные изотопы: их можно разделить на две группы: изотопы четырех радиоактивных семейств тяжелых элементов (U235(уран235), U238(уран238) и Th (торий), Np (Нептуний)) и оставшиеся с момента зарождения нашей Солнечной системы радиактивные элементы, которые вследствие своего огроменного периода полураспада все еще присутствуют в литосфере, атмосфере или мировом океане.
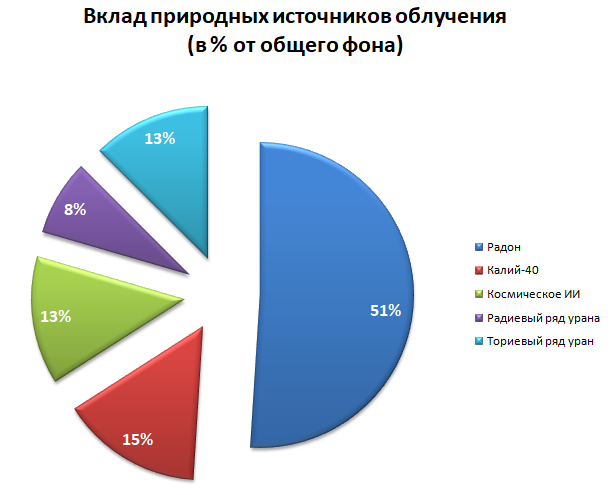
Поэтому суммарное влияние различных источников фон выглядит как-то так
Сразу скажу что когда искал информацию, встречались и другие распределения, поэтому диаграмма выше какбэ не догма. Зависит от региона и среды обитания.
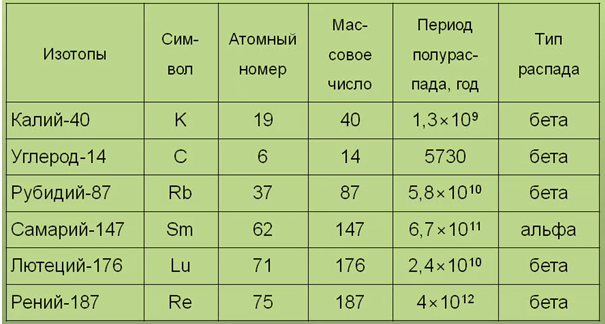
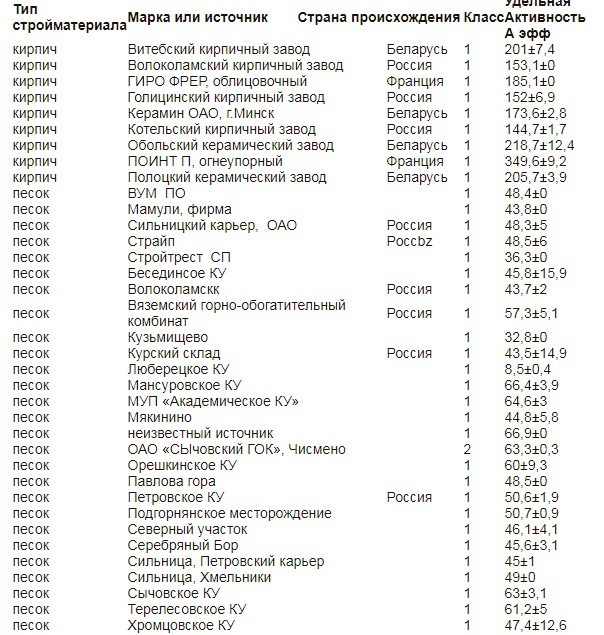
Ниже я приведу таблицу с не входящими в трансурановый ряд радиактивными изотопами.
Как видно период полураспада например рубидия-87 в 11 раз больше срока существования нашей планеты (4,35 *10^9 лет) поэтому вклад в фон все изотопы сверху ( кроме калия и углерода) вносят незначительный.
Мы также понимаем, что раньше на земле было больше радиоактивных веществ и соответственно, и если мы вдруг решим проведать динозавров и у нас окажется дозиметр, то фон будет чуть выше.
Самых близких для нас источников ИИ вне трансуранового ряда в природе два: Калий и Углерод (остальные как правило не учитываются )
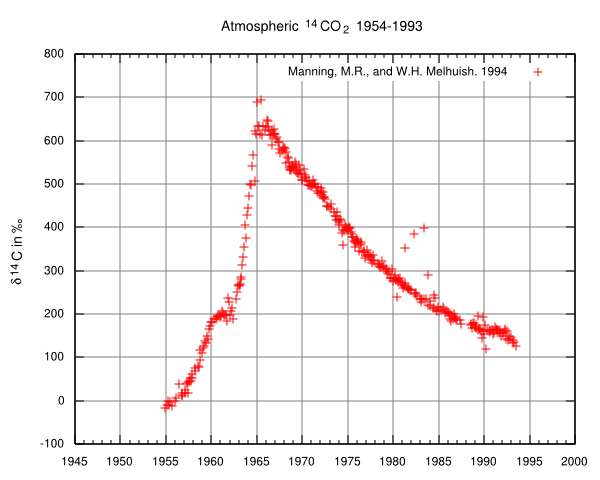
Стоит отдельно выделить углерод 14,т.к. он образуется вследствие облучение СО2 в верхних слоях атмосферы под действием солнечной радиации. С наибольшей скоростью углерод-14 образуется на высоте от 9 до 15 км на высоких геомагнитных широтах, однако затем он равномерно распределяется по всей атмосфере. В секунду над каждым квадратным метром земной поверхности в среднем образуется от 16 400 до 18 800 атомов углерода-14. То есть чисто теоретически даже через овер мильярды милиардов лет, если на земле все также будет атмосфера и почти все изотопы распадутся. останется один углерод 14(но это неточно). На основе углерода 14 основан углеродный метод датирования органических материалов. Пока дерево росло, за счет обмена углеродом с внешней средой в нем поддерживалось природное содержание углерода 14. И как только его свалил ураган, подача углерода извне прекращается. Следовательно углерод -14 начнет распадаться и за 5730 лет его концентрация сократится в двое. Мерим, считаем. Все просто. Ложку ну или почти черпак гумна в это замечательный метод вбрасывают воздушные испытания атомных бомб в 50-60х годах. Когда Мы человечество сами того не предполагая наработали кучу углерода-14 в атмосфере.
Или возьмем вот например калий-40. Калий-40 рассеян по всей земле. В природном калии его распространённость составляет 0,0117(1) %. Если наковырять в какой-нибудь хим. лаборатории чистый металлический калий то его удельная активность будет 31 Бк/г.
Для тех кто не знает 1 Бк=1 Беккерель=1 распад в секунду.
На радиоактивности Калий-40 основан так называемый банановый эквивалент радиоактивности.
Средний банан содержит около 0,42 грамма калия. Радиоизотопы, содержащиеся в бананах, имеют активность 130 Бк/кг или 12 Бк в 150-граммовом банане. Эквивалентная доза в 365 бананах (один банан в день в течение года) составляет 24 микрозиверта (цитата из ВИКИ)
Тоесть пока вы не покакали бананом можно считать, что вы увеличили свою массу тела на этот банан.
Зеленые-радиофобы негодуют:
Впринципе съеденный банан не повышает уровня радиации в организме, поскольку избыточный калий, полученный из банана, приводит к выводу из организма эквивалентного количества изотопа в процессе метаболизма. Ну только если у вас все нормально с почками и нет уремии.
Общее содержание калия в организме человека оценивается в 2,5 грамма на килограмм массы тела или 175 г в 70 кг человеке. Такие количества калия имеют активность порядка 4-5 тысяч Бк (ещё около 3 тысяч Бк — от изотопа углерода-14)
Вывод: не стоит бояться ИИ. Оно вокруг нас все время, как радиоволны, как свет и как воздух. Если бы мы видели в радиодиапазоне, то визуально светились бы как лампочки. Главное понимать, когда и в каких количествах ИИ может навредить. Об этом я напишу в следующих постах.
ЗЫ Сначала я хотел запилить пост про урановые и ториевый ряды и про распространенность этих элементов и их продуктов распада в минералах, но видимо это будет в следующем посте.
ЗЫЫ Баянометр ругался на картинки как сотона.
Зыыыы комментарий для минусов внутри