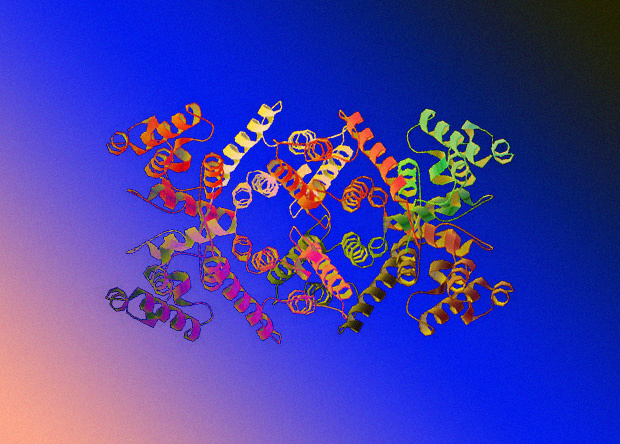Что такое CRISPR?
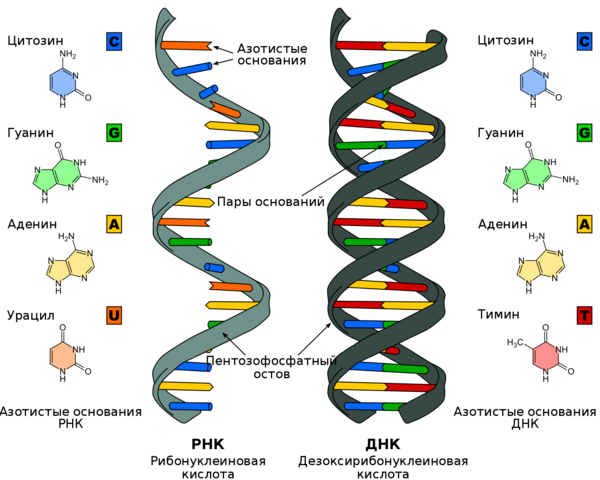
Те из вас, кто старается следить за достижениями в области современной биологии, хотя бы раз наверняка сталкивались с упоминанием загадочной технологии CRISPR, которая вроде как революционировала поле боя молекулярных генетиков. Предполагаю, что даже многие биологи плохо себе представляют, как эта штука работает и какие возможности дает, так что решил запилить пост на эту тему. Сразу скажу, что для понимания содержания статьи потребуется как минимум знать, что такое ДНК. Если надо освежить знания – добро пожаловать в мой прошлый пост.
Итак, встречайте:
CRISPR - Clustered Regularly Interspaced Short Palindromic Repeats (регулярно расположенные группами короткие палиндромные повторы) – это вообще такие участки генома бактерий и архей, отвечающие за любопытную систему защиты от вирусов. Еще в далеком 2013м ученые смогли заставить эту систему работать в искусственно созданных условиях, заставляя ее резать ДНК не в бактериях, а вполне себе в эукариотических клетках. С тех пор много воды утекло, элементы этой системы подпилили до совершенства и коммерциализировали все кому не лень. Но как же оно все работает в лаборатории и помогает ученым? Давайте разбираться.
Одна из задач, которую решают современные молекулярные генетики – зачем нужен какой-то ген. Прочтение генома в наше время – довольно простой процесс, но он даст нам тупо последовательность букв, а не понимание того, какой ген за что отвечает. Классический способ узнать, зачем нужен какой-то ген – вырубить его и посмотреть, что будет. Научным языком это называется «нокаутировать» ген, а полученный организм – «нокаут» по такому-то гену. Далее можно исследовать, что же не так с несчастным животным/растением, и делать выводы о функциях вырубленного гена.
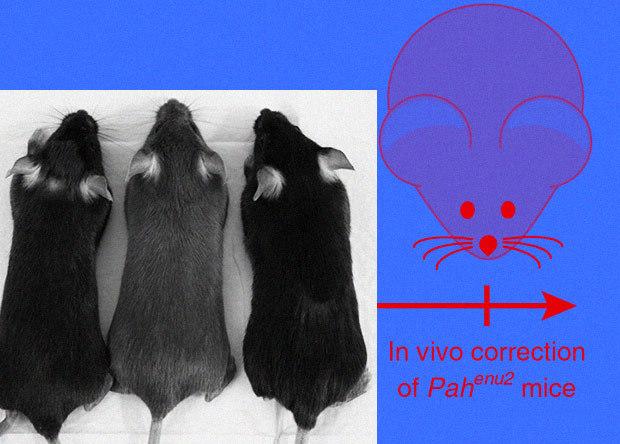
Казалось бы, нормальная мышка, но на самом деле это нокаут по гену RAG1, и у этой мышки нет иммунитета.
И вот очень классно было бы иметь способ, позволяющий просто резать ДНК в ровно нужном тебе месте, вырубая именно тот ген, который надо... В принципе, до прихода CRISPR такие методы существовали (см. TALEN, например), но, как правило, они все были довольно трудоемкими в исполнении. CRISPR же - сравнительно простая технология, применение которой легко поставить на поток. Что же конкретно происходит при ее применении? Чтобы разобраться, давайте сначала введем несколько важных терминов, без которых никак.
Сas9 – бактериальный белок, способный вносить двунитевые разрывы в молекулу ДНК (вы же помните, что там две нити, да?).
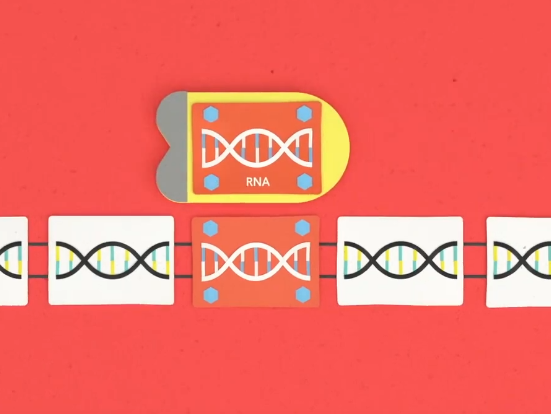
Guide RNA, или gRNA – специальная молекула РНК, которая служит как система наведения – она заставляет белок Cas9 резать там, где надо. Напомню, что РНК химически очень похожа на ДНК, но так исторически сложилось, что РНК выполняет в клетке иные функции, чем ДНК.
CRISPR RNA, или crRNA – часть gRNA, отвечающая непосредственно за наведение Cas9 на цель.
Tracer RNA, или tracrRNA – вторая часть gRNA, она отвечает за связывание с белком Cas9. В природе эта и предыдущая штуковина – две отдельные молекулы, но в лабораторных опытах, как правило, используют химерную молекулу, в которой эти половинки просто сшиты друг с другом.
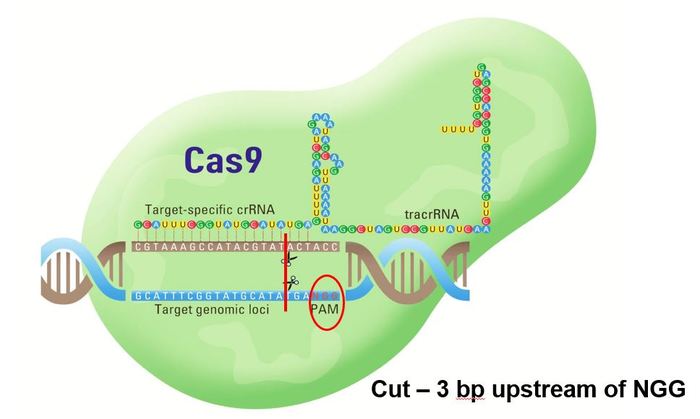
Вот теперь можно переходить к практике. Допустим, ученым надо вырубить ген А в культуре клеток. Культура клеток, кстати – это такая каша из клеток, как правило, одного типа, которая просто растет в специальной емкости в лаборатории. Ученые часто с ними работают, чтобы не париться с настоящими животными и не мучить людей. Так вот, ученым известна последовательность ДНК того самого гена А в этих клетках, и они решают использовать метод CRISPR, чтобы сделать грязное дело. Для этого берется (заказывается у поставщика или синтезируется самостоятельно) молекула gRNA, причем молекула эта подбирается таким образом, чтобы ее кусок – crRNA – был комплементарен тому участку гена А, который надо разрезать. К ней подмешивается белок Cas9 – эдакие безумные ножницы, которые очень любят резать ДНК. Однако сами они резать как попало не могут – им надо показать, где резать – именно это и делает gRNA. Эту смесь из gRNA и Сas9 засовывают внутрь клеток (тут есть разные способы, это отдельная история), где она и приступает к работе. Вторая половина gRNA называется tracrRNA, и за нее белок Cas9 цепляется к gRNA. Благодаря crRNA дружная парочка gRNA+Cas9 садится на нужный участок ДНК клетки и режет обе цепи ДНК. Причем не где-нибудь, а в строго определенном месте – между шестой и седьмой буквой того участка генома, который был комплементарен crRNA. Единственное условие тут – первые три буквы этого участка должны быть NGG, где N – это вообще любая буква. Не хочу излишне пудрить вам мозги, но эти волшебные важные три буквы называются PAM site (Protospacer Adjacent Motif).
Схема работы комплекса CRISPR-Cas9. Зеленая блямба – белок Cas9 – вместе с цветастой молекулой gRNA, состоящей из crRNA и tracrRNA, сел на геномную ДНК в клетке. Красной линией отмечено, где именно Cas9 разрежет двунитевую ДНК – 3 буквы «вверх по течению» от триплета NGG.
И вот тут начинается самое интересное. Заметьте, система CRISPR просто вносит разрез, она больше ничего не умеет! Достаточно ли этого, чтобы вырубить ген в клетке? Никак нет. За миллионы лет эволюции живые системы научились беречь ценную ДНК и исправлять в ней всякого рода разрывы, химические поражения и прочие гадости. Занимается этим специальная клеточная контора под названием система репарации ДНК. Как только она замечает, что имеет место двунитевой разрыв ДНК, на место аварии сразу рекрутируются разные белковые комплексы, которые пытаются исправить ситуацию, причем каждый по-своему. Доходит до того, что они реально конкурируют друг с другом за право починить ДНК, и в итоге существует несколько вариантов развития событий.
Вариант 1. Процесс идет по пути негомологичного слияния концов – Non-Homology End Joining (NHEJ). Чертова куча белков прилетает на место разрыва, и работает прям как ваш сантехник – одни отрезают чуть-чуть оборванные концы (не всегда, правда), другие достраивают концы как надо, третьи сшивают место обрыва. Удобно, быстро – но не всегда точно!! Во время достраивания концов иногда в последовательности оказываются буквы, которых там изначально не было, причем их количество тоже может варьировать. Извини, начальник, так получилось... Ну а если все сделали как надо – наш комплекс CRISPR-Cas9 никуда не делся, и он опять порежет это место! И так до тех пор, пока рьяные белки-помощники не изменят место разрыва до такой степени, что Cas9 больше не сможет на него сесть. Ну или Cas9 самовыпилится, устав хреначить ДНК.
Вариант 2. Процесс идет по пути гомологичной репарации – Homology Directed Repair (HDR). Тут все еще сложнее: вместо того, чтобы тупо сшить два куска ДНК, попутно вставив пару сомнительных букв, эти белки решают «заглянуть в инструкцию» - в данном случае, во вторую копию этого гена в сестринской хромосоме! Вы ведь помните, что у большинства организмов (включая нас с вами) в каждой клетке содержится две (а то и больше) копии ДНК? На всякий ген есть его гомологичная «сестричка», которая более или менее на него похожа. В случае HDR путем хитрых манипуляций белки используют сестринскую копию гена, чтобы правильно восстановить место разрыва. Этот метод более надежный, чем NHEJ, и дает ученым одно важное преимущество, о котором мы поговорим чуть позже. Напомню, что если системе репарации удалось восстановить исходную последовательность порванной цепи, то ее, беднягу, опять режет Cas9, и все начинается с начала.
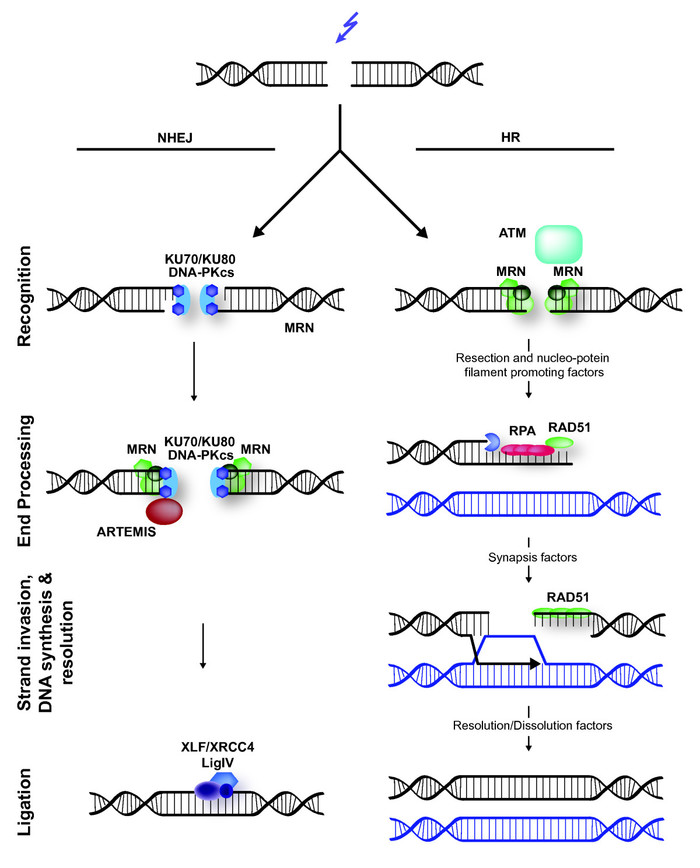
Схема путей репарации ДНК. Слева – путь NHEJ, быстрый и неточный. Справа – HDR, использующий гомологичную хромосому в качестве инструкции.
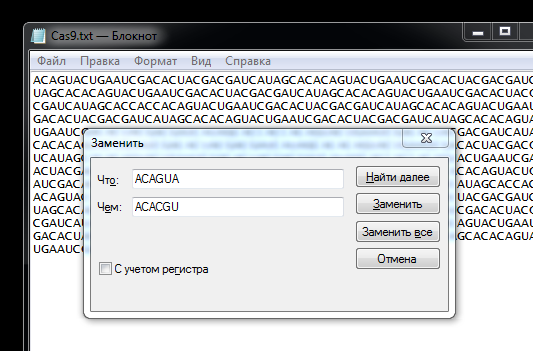
Итак, если мне хочется просто нокаутировать ген в моем объекте исследования, мне достаточно надеяться, что клетка после обработки CRISPR-Cas9 запустит первый вариант репарации (NHEJ), и в итоге часть клеток получит мутации, которые вырубят нужный мне ген. Профит, дело сделано. Но зачем я тогда упоминал про второй вариант репарации, спросите вы? Давайте еще раз на него посмотрим. Белки используют гомологичную копию гена, чтобы исправить повреждение. А что если...(с этого начинаются все безумные идеи ученых)...что если этим белкам под видом гомологичной копии подсунуть кусок ДНК, который мы сами создали, который содержит нужные нам изменения в гене? Тогда они вставят информацию с этого куска в геном в твердой уверенности, что сделали все как надо... Образно говоря, мы слегка подправили им инструкции. И действительно, так и происходит! Такая технология позволяет нам не просто вносить заранее непредугадываемые изменения в ДНК, но и абсолютно точно изменять нужные нам ее участки. Обратите внимание, что CRISPR в этом случае тупо ломает ДНК там где надо, чтобы тем самым вызвать «сантехников», а всю реальную работу делают уже они. С точки зрения лабораторного эксперимента все просто: в этом случае вместе с gRNA и белком Cas9 мы также вводим в клетку кусок ДНК, несущий нужный нам код – он называется донором. В идеальном варианте информация донора в неизмененом виде встроится в целевой геном, добавляя клеткам или организму нужные нам генетические особенности.
Итак, суммируем: для простого нокаута нам достаточно полить клетки/организмы смесью из gRNA и Cas9, чтобы сами клетки при попытке исправить устроенные Cas9 разрушения с помощью механизма NHEJ внесли в ДНК случайные мутации, вырубающие ген. Для точной же модификации ДНК мы также добавим в нашу взрывную смесь донорную последовательность, которую клетки благополучно используют в процессе HDR, чтобы «поправить» свою ДНК (а на деле внести в нее необходимые нам изменения).
Разумеется, такие эксперименты требуют нехилых умственных и временных затрат: надо заранее продумать последовательность gRNA, чтобы она вела Cas9 к нужному месту в геноме, а не куда-нибудь еще. Если мы идем по пути HDR, то также надо продумать последовательность донора. Кроме того, надо спланировать, как и в каком виде мы будем доставлять все это в клетки – тут есть разные варианты в зависимости от кучи факторов (тип клеток, размер вставки и т.п.). Наконец, последняя часть эксперимента самая нудная – нам надо отсортировать клетки, в которых ничего не поменялось (клетки дикого типа), от тех, где мутация произошла! Тут у ученых тоже имеется целый арсенал методов, от простых на основе ПЦР, типа GCD (Genomic Cleavage Detection), до полногеномного секвенирования на монстроподобных агрегатах.
Надеюсь, мне удалось простым языком объяснить, что же такое CRISPR, и как его применяют! В качестве бонуса фотка меня пару лет назад, когда мне удалось лично познакомиться с применением технологии CRISPR.
Эти зеленые клеточки на экране микроскопа еще вчера были синими, но потом пришел автор и с помощью протокола HDR внедрил однонуклеотидную замену в ген BFP, превратив его в GFP.
Спасибо, что прочитали! До встречи в новых постах!