Лига Химиков
Два года ожидания. Мы помним.
Лига Химиков, как научное сообщество, всегда нуждается в интересном контенте, а как пикабушное сообщество - всегда помнит об обещаниях, что были даны пользователям.
Так вот, сегодня исполняется ровно два года, с того момента, как мы ждём от господина @Hazael серию постов про аффинаж драгоценных металлов 🌚 (#comment_95160880)
Надеюсь, моё напоминание хоть немного подтолкнёт автора к созданию постов и сдвинет дело с мёртвой точки...
В общем, Hazael, всё ещё ждём посты про аффинаж.
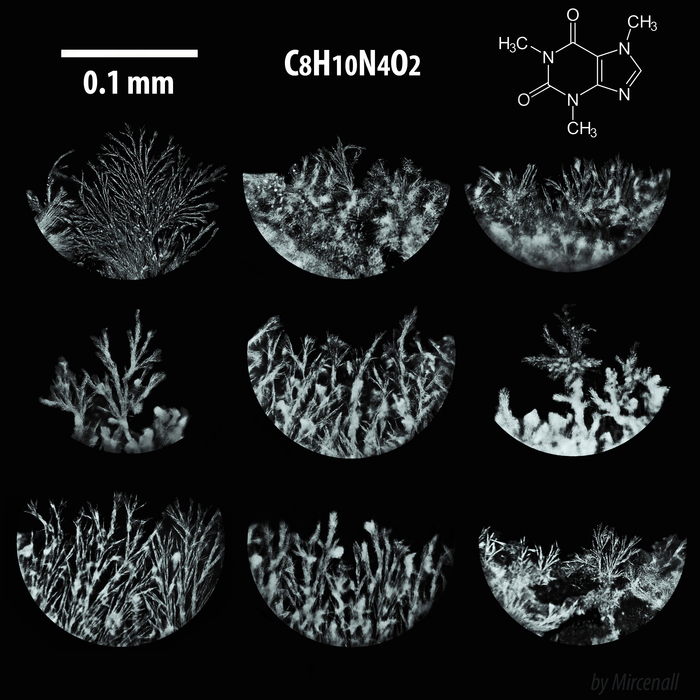
Кристаллы кофеина
На химии было, поставил кислород и получил 5)). Но я хочу с объяснением.
Ar(?)=16
Вопрос-это какой-то элемент из таблицы Менделеева.
Титановая абстракция
Оксидная плёнка на поверхности изделия из титана после нагрева до 500 °C
Моя страница ВК: https://vk.com/mircenall
Хемобия или как страшно жить
Существует версия, что кровавые большевики построили Днепровскую ГЭС, чтобы как можно больше людей умирало от удара электрическим током. Вряд ли кто-то сможет оспорить тот факт, что электрификация стала причиной появления нового фактора опасности для человека, тем не менее, вряд ли хоть один пикабушник откажется от возможности почитать посты из-за потенциального риска умереть от электрического удара зарядным своего смартфона. Мы идем на риск, потому что считаем его оправданным и приемлемым. Чтобы оценить опасность нужно хорошо представлять ее природу, в случае с электричеством можно сказать, что практически любой, кто осилил школьный курс физики, имеет представление о том, что это и с чем его едят.
К сожалению, с химией дело обстоит куда хуже. Уровень преподавания химии в современной школе неудовлетворителен, людей изучающих химию в институте, либо как хобби относительно мало что дает широкий простор для страхов спекуляций и обмана. И тут мы подходим к теме поста. Хемофобия – хтонический страх, перед страшными словами и формулами который никого не оставит равнодушным.
Наверное, треть всех проявлений хемофобии последний пяти-десяти лет в странах СНГ относятся к страху разбивания ртутного термометра. Данное медицинское изделие, плотно вошедшее в обиход населения, имеет свойство разбиваться в самый неподходящий момент, приводя в ужас всех созерцающих данное явление. При мыслях о ртути мозг мгновенно выдает картинку с черепом и костями и отключается. Человек начинает судорожно гуглить и о ужас оказывается что он его семья, его кот и соседи в смертельной опасности.
Первая же страница в поиске пестрит лютыми пугалками совмещенными с рекламой контор по демеркуризации. Стоимость таких услуг зависит от жадности демеркуризатора и платежеспособности пострадавшего. Важно понимать, что в большинстве своем это развод.
Ртуть страшна не сама по себе, страшна она парами. Так что ртуть можно брать руками, можно проглатывать можно (но не нужно) хранить в закрытой таре. Но даже если шарики ртути предательски разлетелись по всей комнате это не повод для паники, в жилом доме всегда присутствует вентиляция, а значит, пары ртути в результате обмена воздуха будут неминуемо выноситься из помещения. На практике в результате разбивания одного градусника в жилом помещении опасная концентрация ртути в воздухе просто не достигается. Чтобы отравиться ртутью, нужно разбить несколько градусников в кастрюлю, поставить ее на плиту и интенсивно дышать, накрывшись полотенцем.
Демеркуризация может потребоваться, в случае если речь идет о разливе, по крайней мере, десятков граммов ртути, но даже если с вами приключилась такая беда, ртуть отлично связывается (переходит в нетоксичный сульфид) порошком серы.
В случае с ртутными лампами все обстоит еще забавное, учитывая что количество ртути в них измеряется миллиграммами, обычно эти миллиграммы уже покинули помещение еще до того как испуганный гражданин успеет набрать номер конторы демеркуризаторов.
Следующая пугалка – формальдегид (а так же фенол, «плохой запах», яд для травли соседей «Новичок»). Обнаружив у свежеприобретенной табуретки неприятный запах, гражданин начинает искать ответы в гугле, обнаруживая, что виной всему формальдегид. Через несколько дней табуретка перестает источать запахи, но гражданина уже не остановить, он уверен что имеет место быть формальдегид, кроме того на табуретке успел посидеть любимый кот и успел постоять любимый чайник, как же теперь с ними быть, куда бежать и что делать?
Естественно на просторах обнаруживается множество организаций, которые за долю малую проведут анализ и вынесут табуретке приговор. Естественно тот же анализ может провести и СЭС, но она скорее всего не найдет никаких нарушений, потому что их и не было. Еще раз повторюсь, что в условиях жилого проветриваемого помещения создать опасную концентрацию очень трудно, так что табуретку можно оставить в покое.
Можно привести еще много примеров бытовой хемофобии, начиная от боязни буквы «Е» в составе продуктов, до сказок про ежиков и батарейки. Все это ограничивает человека, создает иррациональные, основанные на предрассудках и бредовых идеях концепции. Данное мышление активно эксплуатируется и монетизируется маркетингом, поддерживается и взращивается чуть ли не на государственном уровне.
Мораль как всегда незамысловата: не нервничайте, думайте головой, досконально изучайте вопрос с которым довелось столкнуться и не бойтесь химии)
Тантал - металл маминой подруги
Всё это и прочее на странице ВК:
21 пост первого года:
#comment_145408550Предыдущие посты второго года:
Радон (Радон - да уж, нашёл про что рассказать...)
Литий (Литий - металл живущий по своим правилам)
Рутений (Рутений - образец для подражания)