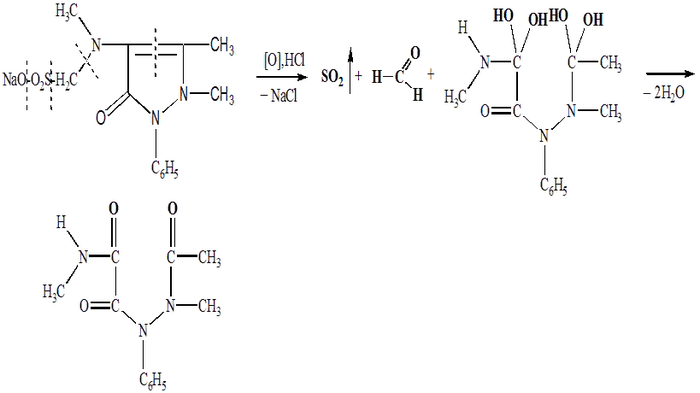
Аллергия на анальгин после вакцины О_о
Вакцинировался тут недавно, перенес как по методичке - день провалялся с 38.1, потом резко прошло. Через неделю как-то болела башка, принял анальгин, поехал домой. По дороге чувствую рожа чото чешется. Приехал домой, сижу за столом, чувствую рожа чешется уже прямо невыносимо, иду к зеркалу, а морда лица вся красная и в волдырях как от укусов комаров. Думаю чо за хрень, чо я сожрал такое, вспоминаю анальгин, гуглю аллергию на анальгин, нахожу что так и бывает. Вопрос тока - у меня никогда в жизни не было аллергии на анальгин, так что это было?
Противоречивая дымовуха: часть вторая
Нужных ионов вам, уважаемые подписчики сообщества и читатели! В этом посте мы будем продолжать наши попытки по выяснению и описанию природы известной дымной реакции. Слухи о том, что же таки исходит из смеси в виде дыма и каков состав продуктов реакции, ходят давно и столь же долго волнуют умы химиков-энтузиастов. В комментариях под предыдущим постом некоторые пользователи выразили свои опасения насчет реакции. Напомню, что моей целью НЕ является популяризация этой самодельной дымовухи, мы стараемся показать, что контролируемые условия есть краеугольный камень безопасного исследования. Все-таки почти никто не знает пока, с чем мы имеем дело. Ссылка на прошлый пост: Самая противоречивая дымовуха, или Трудная история одной знаменитой реакции
Осторожно! В этом посте вас ждет много экспромта и безумных (может быть, даже придурковатых) решений.
В ходе прошлого процесса изучения мы выяснили, что реакция имеет, вероятно, окислительно-восстановительный характер, анальгин выступает в роли неплохого восстановителя, а пероксид водорода его антиподом, окислителем. Состав твердых продуктов реакции (будем для удобства звать ее смолой) до сих пор никому не известен, не достигли этого знания и мы. Я придерживаюсь наиболее популярной точки зрения насчёт смолы: продукт реакции не один, а несколько, возможно даже, что их не меньше десятка. В связи с этим трудно судить и о составе дыма. Итоги проведения реакции как при растворенных реагентах, так и при сухих показали, что неизвестное соединение красно-оранжевого цвета образуется при нагревании реакционной смеси. Именно нагревание дает начало всей этой сложной истории таинственной ОВР-реакции. Без повышения градуса ничего из вышеуказанного не работает. Вы резонно укажете, что вообще-то дымовуха самовозгорается и дымит без всякого внешнего нагрева. Это верно, но ход реакции ускоряется, если слегка подогреть смесь обычной горящей спичкой. Как бы там то ни было, взаимодействие реактивов в этой дымовухе может смело носить звание экзотермической, то есть сопровождающейся выделением тепла. Причем большого его количества, ведь температура активированной смеси в момент реакции достаточна высока, чтобы расплавить пластик и поджарить кожу неосторожного испытателя. Не забывайте и том, что продукты реакции в виде красной "смолы" и дыма пока не изучены, а их угроза здоровью вполне вероятна, так что одним ожогом вы можете не отделаться.
Доказать, что в образовании твердых окрашенных продуктов реакции играет в первую очередь пероксид водорода, мы повели реакцию с нагреванием смеси и получили соединение аналогичного окраса (возможно, и аналогичного состава).
Залипательное видео реакции из прошлого поста вставлять не буду, чтобы самоцитирования не было (так что вот результат, если забыли)
Любопытно, что полученный р-р обладает точь-в-точь таким же запахом, как и дым (смола после реакции всухую имеет тот же аромат). Ничего другого в ходе реакции не образуется, дыма тоже нет. Заметим, что любой намек на воду в реакционной смеси предотвращает выброс дыма, даже если ее было пару капель на несколько граммов смеси. Это важное наблюдение, ведь я часто ленюсь высушивать пробирки после мытья, и на дне всегда собираются капли воды со стенок. Эта мелочь меняла характер реакции. Данную особенность предполагал один из пользователей форума Химик.ру:
...реакция анальгина с пероксидом водорода сложна и неоднозначна. Судя по всему, реакция идет сразу по двум местам: по сульфогруппе и метиламиниловой группировке. Соответственно, по сульфогруппе может образовываться сероводород, а также вода и кислородВот только неясно, имеет ли приведенная им реакция смысл в реальной картине процесса? Пойдем дальше.
-SO3 + 2H2O2 = H2S + H2O + 3O2.
Образующаяся вода приводит к частичному гидролизу по связи С - N и отщепляется метиламин, и тоже образуется вода и кислород:
-N(CH3) + H2O2 = H2NCH3 + H2O +1/2 O2
Один из комментаторов справедливо заметил, что я упустил из виду реакцию анальгина с карбамидом, вторым компонентом гидроперита. Исправляюсь:
Реакция без нагревания, ничего интересного
С огоньком (ускорено в 8 раз)
Нагреем просто р-р карбамида:
Р-р тоже едва заметно пожелтел. Дыма вновь не наблюдаем, равно как и запаха.
Не стоит думать, что карбамид такой уж безобидный. Если вы прокалите таблетку гидроперита на огне, то она расплавится, высвободив кислород и аммиак. Будьте осторожны, если попытаетесь повторить, ведь газы выходят тоже горячими, а раскаленного аммиаку нюхнуть никому не пожелаешь.
В ходе реакции пероксид водорода из клатрата распадается на воду и кислород, а мочевина разлагается до аммиака.
Быть может, высвобождающийся аммиак каким-то образом связывается с серой анальгина и образует взвесь некой их соли?
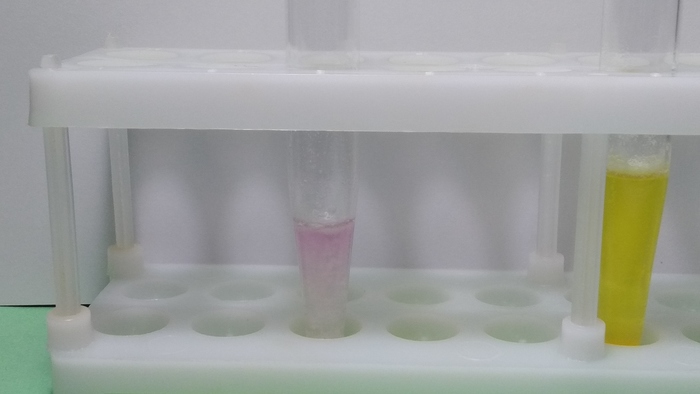
Вот такие результаты отдельных проверок анальгина: слева - с перекисью, справа - с мочевиной
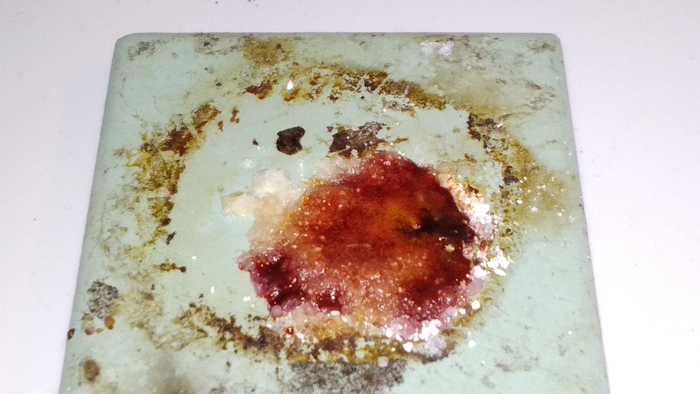
Из чистого и непорочного любопытства решил прокалить порошок анальгина и понаблюдать, долбанет али нет. Ценой этого любопытства стала жизнь целой пробирки, покинувшей наш неидеальный бренный мир:
Что же тут можно увидеть? Как только препарат начинает сгорать и чернеть, над порошком поднимается некий белый дымок, очень скоро преходящий в нещадный дымоган. Вам повезло, что вы находитесь по другую сторону экрана и не слышите эту отвратительную вонь, захватившую весь оставшийся объем комнаты. По ощущениям, это похоже на сильный смрад от чего-то тухлого, сначала вообще показалось, что кто-то изрядно испустил кишечных газов. Думаю, мы имели дело с сероводородом, хотя никаких фармакопейных доказательств этого суждения нет. Сгоревшие остатки реактива также пахнут очень дурно, после ликвидации эксцесса руки пахли несколько часов, и никакие мыла не помогали. К сожалению, эта реакция не очень помогла мне разобраться: дым явно не тот, а значит, надо ехать дальше. Газ выделился вместе с белым дымом, а не отдельно, но если это действительно сероводород, то сульфат меди он точно превратит в черный сульфид. Возникла правда одна проблема: из-за очень скверного зловония провести безопасно этот опыт я пока не смог.
Зато я попробовал осуществить задумку с нашей дымовухой. Дым ни в какую не лез в протянутую трубку для пропускания газов, пузырьков на конце трубки в подготовленном р-ре не появилось. Что это может значить? Я полагаю, что летучим продуктом реакции является все-таки именно дым, а не какой-то газ. Последний бы обязательно вытолкнул воздух из трубки и дал знать о себе через пузырьки, однако дым этого не сделает. Дело в том, что дым является золем некого твердого вещества в воздухе или газе (аэрозолем), т.е. это твердая дисперсная фаза в газообразной дисперсной среде. Мелкие частицы неизвестного вещества навряд ли можно с таким же успехом пропустить через трубку и что-либо толковое получить. Некто из пользователей утверждает, что дым включает серосодержащие соединения, позволяющие получать нерастворимые соли меди, сульфиды, например. Дым не пробулькивается через р-р купороса, поэтому приходится доставить медный купорос прямо в само зловонное пекло. Я приготавливаю липкую смесь из муки и сульфата меди и наношу на палочку, а далее подвешиваю ее над порошком.
Сверху: вышло такое вот голубое медное тесто, бадяга, одним словом. Ну и как после того не назовешь меня сумасшедшим?
Снизу: согласно гениальному и надежному, как швейцарские часы , плану, газ должен подняться к подвешенному сульфату меди и начать там ионную заварушку, в итоге которой кашица должна окраситься в черный цвет из-за сульфида меди (II).
Нагреваем смесь и смотрим, что там деется. Извините за руки в кадре:
Заметно, что кусочки нашего "медного теста" на стекле пожелтели, но черного, как уголь, сульфида меди что-то не видать. На столь малой дистанции реакция бы точно пошла, но пока мы судить о ней никак не можем.
После стольких испытаний мы пришли в тупик: дым, походу, не стоит из сульфида аммония или чего-нибудь в этом роде, зловонный запах образуется в реакции и без карбамида, а продукты разложения всех составляющих дымовухи отличны сами по себе и никак не вписываются в общую картину взаимодействия.
А что если попробовать собрать частицы дыма на мокрой ткани? Понятно, что присутствие воды в реакторе может загубить все веселье на корню, но мы разместим смоченную салфетку чуть повыше. Дальше в моих планах было изучить впитавшееся в воду вещество путем вымывания, тестов и т.д. Давайте вместе поглядим, что стало с бедной испытуемой:
Результат оказался неожиданным: салфетка сама по себе пожелтела, хотя верхняя часть пробирки была чистой, и собрать остатки красной смолы она никак не могла.
На фоне увиденного сразу вспомнились слова одного из пользователей форума:
Тут 2 продукта реакции: смолообразное вещество и дым. Желательно разбираться что представляет собой каждое из них по отдельности. Что касается дыма: это газ или взвесь? Скорее всего это углекислый газ и/или азотметан и взвесь какого-то органического соединения.
Судя по тому, что мы изволили лицезреть, дым - это не что иное, как само красновато-оранжевое вещество, образующееся на дне пробирки! Выходит, что все это время мы имели дело просто аэрозольным состоянием неизвестного продукта окисления анальгина? Распыленный в воздухе продукт просто поднялся к смоченной бумажке и впитался, растворившись в воде.
Я уж конечно, извиняюсь, что показываю это бесстыдство с точки зрения современных методов аналитики, но...все перед вами, и я не знаю, как это еще можно интерпретировать.
На фото даже можно заметить, что на ближнем конце одна из салфеток даже стала чуть красноватой. Ну а если состав дыма аналогичен составу плавящейся конечной смеси, то и состав его останется для нас, вероятно, тайной в ближайшее время. Но это еще не совсем конец, если смолу растворить воде и прилить немного сульфата железа (III), то р-р темнеет почти до цвета сажи, только с бурым оттенком, осадка вроде не образуется:
С сульфатом меди, как вы уже поняли, неизвестное вещество не реагирует. Наверное.
Это был второй этап нашего исследования, все выводы пока делайте сами. Возможно, это еще не всё. Будьте осторожны, если захотите повторить, запаситесь терпением и хорошей вентиляцией, а то много страшилок тут рассказывают про эту дымовуху.
Самая противоречивая дымовуха, или Трудная история одной знаменитой реакции1
Нужных ионов вам, уважаемые подписчики сообщества! Этот пост выпущен по просьбе одного из читателей, а затрагивает он довольно старую и известную реакцию анальгина с гидроперитом. На просторах Рунета мною было обнаружено достаточно много упоминаний этого дымного феномена. Поглазеть на частные случаи, конечно, вы можете и сами, однако во всем этом разнообразии не хватает одного: описания и объяснения явления. Забавная дымовуха из подручных средств прочно закрепилась на многих форумах самодельщиков и т.п. Однако в местах сосредоточения химиков эта реакция вызывает вопросы и порождает споры. Попытаемся разобраться в проблеме настолько, насколько это позволяют наши знания и ресурсы.
Какова же из себя реакция? Соединение сухих мелко измельченных порошков анальгина и гидроперита спустя несколько минут при н.у. приводит к малоизученной реакции, сопровождаемой выделением большого объема дыма с резким горьким запахом, напоминающего по "аромату" обычный табачный дым. Так уж вышло, что в недавнем посте мы подробно разобрали химические свойства анальгина на примере некоторых фармакопейных и не только реакций. Если вы его прочитали, то наверняка вспомните, что метамизол натрия (анальгин) является довольно заметным восстановителем.
При реакции со многими окислителями вроде иода, гипохлорита натрия, пероксида водорода метамизол обычно превращается в т.н. тетраокоспроизводное, а затем и в диоксопроизводное. Первое из них обычно сильноокрашенное вещество, например в реакции гипохлоритом натрия (она же обычная бытовая хлорка) р-р резко синеет, затем окрас быстро доходит до зеленоватого, пока вовсе не тускнеет и не становится просто желтым. Очевидно, что реакция привела к образованию первичных продуктов окисления синего цвета, которые быстро сыграли в ящик и разложились до более светлых вторичных продуктов. На самом деле, точную формулу этих конечных веществ довольно сложно установить. Чтобы вы вспомнили реакцию, приведу ее ниже:
Сколько раз не повторяй, все равно завораживает
Таким образом, прочитавшие предыдущий пост про анальгин, точно знают, что присутствие пероксида водорода (неплохого окислителя в данных условиях) создаст условия для окисления метамизола. Ведь гидроперит, второй реагент, состоит из двух компонентов: мочевина-карбамид и наш пероксид водорода. Процентное содержание последнего всего 35%, а сам препарат по химическому строению является клатратом пероксида водорода с мочевиной. Поскольку мы пока не знаем, кто именно реагирует в нашей реакции, столкнем только анальгин и перекись. Организуем мы эту встречу в водной среде:
3% пероксид водорода и р-р анальгина
Реакция ничем себя не обнаруживает, цветовых переходов нет, отсутствуют вообще какие-либо признаки. Неужто окисления не случилось? Лишь в случае, если вы возьмете достаточно насыщенный р-р анальгина, может возникнуть тусклое фиолетовое кольцо (оно есть в прошлом посте, взгляните на досуге). Но мы не отчаиваемся и начинаем жечь р-р пламенем. Происходит одно очень любопытное и красочное взаимодействие:
Между прочим, эта реакция впервые была упомянута в древних сообщениях 12-летней давности на форуме XuMuK.ru :
01.02.2009:...чтобы не было дыму, решили в водичке разбавить гидроперита и к нему подкинуть тертого анальгина. Погрели чуток, пошла реакция и получилась смесь темно-вишневая. Точнее раствор.Автор задает вполне опосредованные вопросы насчет пиразолонового цикла, который, как мы помним из всё того же прошлого поста, склонен разрушаться по месту двойной связи меж двумя атомами углерода.
Отлили малость раствора в пробирочку и сыпанули туда соды. Раствор посветлел заметно и стал светло-оранжевый. Реакция бурная.
Отлили в другую пробирочку. Долили уксуса, ничего не произошло. Сыпанули соды, пошла реакция. По началу нейтрализовался уксус видимо (запах пропал). Смесь стала темнеть и дотемнела темно-бардового цвета (темнее первоначального продукта). Затем начала светлеть и стала светло-оранжевой.
Идет ли разрыв N-N связи в пиразолоновом цикле метамизола?
Вишнево-красный продукт реакции. Может стать оранжевым при дальнейшем нагревании.
Однако автора больше волнует вопрос разрыва по другой связи цикла. Заметим, что суть реакции, судя по всему, заключается в окислении. Окрашенные продукты и наличие хорошего окислителя прилагается, но как именно протекала реакция? Точного ответа у нас пока нет. Если дальше следовать приведенным инструкциям и добавить щелочи или карбоната натрия, р-р приобретет желто-оранжевый окрас:
Сначала реагирует с карбонатом натрия, а потом с щелочью
Если нейтрализовать щелочь кислотой, то р-р вновь покраснеет:
Один из пользователей заметил, что все полученные выше соединения не образуют взвесей и преципитатов, а следовательно они должны быть хорошо растворимыми в воде. Из этого был сделан вывод: всё это соли неких карбоновых кислот. В пользу этой гипотезы говорит смена и восстановление цветов при изменениях рН из-за привнесения серной к-ты или щелочи. Установить природу этих солей, сами понимаете, довольно непросто. В связи с указанным предполагается и разрушение связи N-N в молекуле метамизола, "ибо рядом есть карбонильная группа". Вероятно, комментатор решил, что по месту кетонной группы произойдет окисление до карбоксильной группы, а присоединит она ионы натрия от щелочи или карбонатов.
Вы спросите: "А какое нам вообще дело до этих жидкостных реакций и парадоксов? Мы ждем, когда долбанёт!"
Скоро вы поймете, а пока мы удовлетворим вашу потребность хотя бы в одной бурной хим. реакции. Воспроизведем всё так, как должно быть:
Лично мне было лень дожидаться самопроизвольного начала горения, и я решил повысить градус
Пока вы в который раз наслаждаетесь дымком, обращу ваше внимание на продукт реакции. Реагенты словно сплавляются в какую-то смолу, имеющую... уже знакомые нам вишнёво-красный и оранжевый цвета! Уверены, что вам это ничто не напоминает?
Совершенно отчетливо видны похожие оттенки красного
Если растворить в воде продукты реакции, то получим р-р такого цвета:
Насчет состава дыма тоже есть вопросы. Если не забыли, гидроперит включает в себя еще и мочевину. Она вроде не участвует в образовании окрашенных продуктов реакции, и опыт с одним пероксидом водорода это доказал. При нагревании мочевины может образовываться аммиак - немного едкий газ с очень сильным резким запахом, отлично растворимый в воде и образующий в ней гидроксид аммония. В безводных условиях аммиак также может создавать аэрозоли солей, в состав коих он входит, например, хлорида аммония. Что если дым - это тоже какая-то соль в виде мельчайших частиц? Откуда только катиону аммония взять анион? Один из пользователей выдвинул свою гипотезу, согласно которой этим анионом является гидросульфид-ион.
Дело в том, что окисление метамизола может идти не только по циклу пиразолона, но и по сульфогруппе, в прошлом посте такой сценарий запускал иод. Реакция по сульфогруппе и метиламиниловой группировке.
По сульфогруппе может образовываться сероводород, а также вода и кислородЕдинственное, что остается неясным, так это странный, горьковатый запах аэрозоля. Да и в самих реакциях остальные спецы нередко находили неточности.
-SO3 + 2H2O2 = H2S + H2O + 3O2.
Образующаяся вода приводит к частичному гидролизу по связи С - N и отщепляется метиламин, и тоже образуется вода и кислород:
-N(CH3) + H2O2 = H2NCH3 + H2O +1/2 O2
И наконец становится понятным, что за дым получается в этой реакции:
Сероводород взаимодействует с метиламином и получается гидросульфид метиламмония:
H2NCH3 + H2S = [H3NCH3]HS.
И взвесь его мелких кристалликов в воздухе и создает визуальное ощущение "дыма".
Что касается окрашенных продуктов, то есть также версии, утверждающие типичный их ход появления:
Вот такой вариант развития событий подан другим пользователем.
Именно эта реакция объясняет принцип многих окислительных реакций с участием метамизола. Но этот случай нам е подходит, т.к. он требует наличия кислоты, а в условиях опыта ее нет. Этой же схемой пытались объяснить и альтернативную гипотезу строения дыма, мол состоит он из сероводорода и аммиака. Но как видим, пока безрезультатно.
Многие юзеры уверены, что связь N-N легко поддается разрушению, но вот единогласия насчет природы дыма и точного хода реакции нет.
Был один специалист, который посоветовал пропустить дым через р-р сульфата меди, например. Это должно помогло бы обнаружить и осадить ионы металлы посредством тех же сульфид-ионов. Читатель форума также утверждал, что осуществил эту операцию сам и получил черный сульфид меди. Однако никаких данных и доказательства этого он не привел, хоть пиши [ДАННЫЕ УДАЛЕНЫ]. Вероятно, исход этого опыта что-то объяснил бы, но пока нет возможности повторить это самому.
Определить природу продуктов все же остается очень сложно задачей, зависящей от слишком большого количества условий. Предполагаемые механизмы окисления могут протекать нескольким функц. группам и даже расщепление трех метильных групп с последующим разрывом пиразолонового кольца в теории может к образованию различных промежуточных продуктов в виде гидроксилированных и карбоксильных производных. Самым сложным, пожалуй, считается определение состава белого дыма, поскольку решение этой задачи позволило бы прикинуть ход реакции.
Продолжаем работать, но вопрос очень сложный. Я попытался внести хоть какую-то практическую ясность. Возможно, я только больше всё запутал, но химикам всё ещё есть над чем поразмышлять.
Все выводы пока делайте самостоятельно
Как отвергнутый миром анальгетик в художники подался и что из этого вышло
Гаптен, быть может, порождает,
И тримепиридина он слабей,
Но буйство красок окисленья пробуждает
Знакомый наш среди лекарственных "солей"...
Нужных ионов вам, уважаемые подписчики сообщества и читатели! Нередко бывает так, что проводимые самостоятельно химические реакции поражают не только своими продуктами, но и восхитительными цветовыми переходами, которыми они сопровождаются. Если вы читали предыдущие посты про хлоргексидин и сочли это своего исключением из мира фармацевтики, то вы ошиблись. Поскольку сегодня речь пойдет о самом незаурядном, по моему мнению, художнике среди лекарственных препаратов.
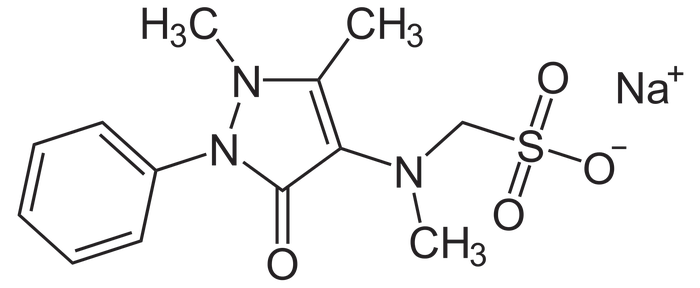
Познакомьтесь, это анальгин (он же метамизол натрия)
Это лекарственное вещество сейчас хоть и продается в аптеках отдельно или в совокупности с другими веществами, но в остальном мире на него долго точили зуб, покуда вовсе не запретили.
В Великобритании метамизол выведен из фармацевтического рынка в 1965 году. В Норвегии изъят из обращения 1976 году. В США изъят из обращения в 1977 г. В Саудовской Аравии запрещён с 1980 г. В ОАЭ изъят из обращения в 1981 г. В Израиле метамизол-содержащие комбинированные средства изъяты из обращения с 1985г. В Дании запрещены все метамизол-содержащие препараты с 1979 г. Метамизол изъят из обращения в Малайзии 1987г, в Пакистане, Гане, Нидерландах, Бахрейне, Ирландии, Сингапуре, Венесуэле, Непале, Германии и др. Сейчас метамизол-содержащие средства бесконтрольно используются лишь в России и нескольких развивающихся странах.Дело было в том, что препарат довольно агрессивно настроен как ко многим другим медикаментам, так и к организму. Выяснилось, что анальгин способен вызывать агранулоцитоз, т.е. заболевание, при котором сильно страдают лейкоциты, их число заметно снижается за счёт гранулоцитов и моноцитов. Я полагаю, что конкретно этот агранулоцитоз имеет иммунную природу, а виноватыми следует считать экзогенные антигены. Эти антигены, носящие название "гаптены", возникают благодаря не только нашему анальгину, но и многим анальгетикам и седативным препаратам.
Неиммуногенные гаптены то и дело вставляют палки в колеса иммунитета, поскольку их природа не позволяет вырабатывать антитела, зато эти тунеядцы легко с ними связываются. Иждивенчество их обеспечивается обычно белками-носителями ("шаперонами"), с которыми гаптены и могут стать иммуногенными, но это для них единственный путь к этому. Результатом порождения гаптенов часто становится не только лейкоцитопения, но и саботаж иммунной реакции (с чем напрямую связан предыдущий дефект). Выявление взаимосвязи анальгина с гаптенами является лишь моим предположением, так что ошибки вполне возможны.
Забыл сказать: анальгин тоже является болеутоляющим, но в связи с вышеуказанными подробностями он не шибко популярен. Гораздо чаще его используют вкупе с антипиретиками и другими анальгетиками, например, в многокомпонентном препарате "Спазмалгон" (с него, кстати, и началось мое знакомство с анальгином). Сам по себе метамизол натрия относительно недорог, так что приобрести его не является задачей сложной.
Обратим теперь свой взор на химическую природу анальгина. Метамизол натрия представляет собой довольно сложную сульфоновую кислоту, а точнее, ее натриевую соль. Относится он к нестероидным противовоспалительным препаратам (НПВП), а истоки берет он от пиразолона (пятичленного гетероцикла с двумя гетероатомами азота). Самая яркая его черта - это примечательные восстановительные свойства. Помните аскорбиновую кислоту и наши попытки стабилизировать соли железа против окисления? Так вот теперь, она не одинока, метамизол натрия может составить ей хорошую компанию бытовых восстановителей. Чем же обуславливается такой характер препарата? Причина кроется в неустойчивой и частично гидрированной системе пиразолина и гидразиновой группировки. Метамизол натрия в процессе окисления склонен образовывать свои нестабильные тетраоксипроизводные, имеющие как правило, заметный окрас. Реакции окисления обычно затрагивают именно фрагмент пиразола, но иногда могут расшевелить и другие ф. группы. Что будет с веществом дальше, узнаете в соответствии с планом поста.
Рецепт:
Анальгин (можно "Спазмалгон") - аптека (р-р 1-2 таблеток на четверть стакана воды)
Сульфат железа (III) - перекись водорода + р-р магазинного железного купороса
Иода настойка спиртовая 5% - аптека
Серная разб. к-та - электролит аккумуляторный
Дихромат аммония - вероятно, пиротехнические магазины (у меня от какого-то древнего набора остался).
Гипохлорит натрия - "Белизна".
Начнем же проверять препарат, а начнем мы с довольно простого окислителя - перекиси водорода. Да, я знаю, что она проявляет амфотерные свойства и в зависимости от реакции может быть как окислителем, так и восстановителем. Но у нас здесь имеется товарищ, желающий сбросить с себя электронов, так что перекись будет очень кстати. Чтобы реакция пошла интереснее, позовем еще разб. серку:
На видео вышел маленький косяк: р-р изначально не имел голубого оттенка, всему виной одна неосторожность. Но суть вы узрели: появилось соединение насыщенного синего цвета, которое быстро обесцвечивается.
Далее я провел одну реакцию от которой, честно говоря, ничего не ждал, но результаты меня удивили. В первом видео сначала приливалась перекись, а затем только кислота. Но при повторе я решил сделать наоборот и... остановился на первом этапе:
Снова появляется синий окрас, быстро сходящий на нет спустя секунды.
И вот тут предо мной встал вопрос: разб. кислота тоже окисляет? В школьной химии, например, окислять способны только конц. растворы серной кислоты, а разведенные же ничего такого не творят. Но что тогда мы наблюдали здесь? Ваш сноб (т.е. я) сначала долго воображал, что получил "метамизоловую кислоту" простым вытеснением более слабой. Странным для меня оставался ее цвет и свойства тускнеть с полной потерей цвета, а также удивительное сходство с обычным окислением. И всё-таки я решил, что дело именно в окислении. Каким образом эта серная кислота могла проявить окислительные свойства, остается непонятным. Может, вмешался кислород воздуха? Знатоки, выручайте.
Теперь вы ждете от меня общих пояснений. Упомянутое нами окрашенное тетраоксопроизводное имеет свойство переходить в бесцветное диоксопроизводное. Цикл пиразолина рвется по месту непредельной связи меж двумя атомами углерода, каждый из которых приобретает по две гидроксильных группы. Но для одного углерода столько незваных гостей будет слишком много, поэтому лишнее отстегивается наружу в виде воды, а углероды оставляют себе только по атому кислорода (к кислороду, разумеется, протягивается тоже двойная связь). Так анальгин ведет себя в ответ на окисление. Есть у нас еще, как любят писать в рецептах, tinctura Iodi spirituosa (настойка иода 5%):
Иод тоже неплохой окислитель, хоть и слабейший среди галогенов (астат и все, что ниже иода не учитываем). Окислить метамизол натрия для него вполне силам. На выходе получаем забавный розовый растворец.
Взаимодействие с иодом идет иначе: в данном случае окисляется не пиразолин, а сульфит-ион метамизола натрия. Переходит он в сульфат, поэтому и игра цвета тут другая. Это реакция нашла себе место в аналитической идентификации препарата (количественно, титрованием).
В качестве заключения нашего лабораторного приключения протестируем еще дихромат аммония. Это один из самых сильных ок-лей в моей лабе, а еще это жутко опасное соединение: ядовит, токсичен, канцерогенен, надменно взрывоопасен и язвительно горюч, в воде прекрасно растворяется. Цвет приятный, апельсиновый, но любоваться им приходится крайне осторожно, даже малые концентрации опасны для организма, а без перчаток к нему и вовсе приближаться не стоит. Благо, что не летучий. С ним часто проводят красочный опыт "вулкан", в ходе которого происходит эффектное извержение оксидом хрома (III), но такие эксперименты слишком опасны для дома. Пробирка же все стерпит:
Дихромат я люблю добавлять всухую, крупицами. Мне-то всё равно, а вам так приятнее и интереснее. Смотрите до конца
Если на секунду отвлечься от занимательной картинки на видео, то станет ясно: принцип реакции не слишком отличается от приведенных. Да, соединение-продукт обладает бордовым цветом, а не синим, но это уже специфика окислителя, вероятно. Хотя, если приглядеться, то в самом начале виден все-таки другой окрас, так что не спешите ворчать.
Можно побаловаться и капнуть гипохлорита натрия. Тоже будет наглядно:
Слева - реакция с гипохлоритом, все типично, ведь он хороший окислитель и все дела. Справа - сульфат железа 3. Вы ожидали восстановления железа? Зря, тут анальгин вас разочарует. Хотя, обратите внимание на первые капли, там явно образуется что-то темное. Потом окрас осветляется.
Если к окисленному гипохлоритом р-ру прилить разб. серной кислятины, то синие промежуточные продукты вновь появятся. Правда, чтобы тут же исчезнуть.
Бонус: синий окрас исчезает, р-р светлеет, а вот потом случается это - после пероксида водорода в кислой среде серки остается фиолетовое кольцо (слева).
Те, кто знаком с фармакопейными реакциями, ждали прогрева с хлороводородом, дабы понюхать формальдегида; ауринового красителя с конц. кислотами, прокаливания с карбонатами. Некоторые из них я просто не могу пока нормально повторить в силу материальной неоснащенности, а некоторые просто неинтересны для обывателя, в отличие от химика. Всё-таки Пикабу - не химический форум, а потому здесь не нужно что-то особенно сложное и непримечательное. Ну а мы продолжаем набирать знания на практике и опыте своих ошибок. И показывать занимательные штуки из тех мелочей, что находятся вокруг нас.
Все выводы, как и всегда, делайте на ваше усмотрение. Если вы считаете, что я ошибся, то так и укажите.
В России резко подорожал анальгин
В июне в России резко подорожал анальгин. Об этом пишет газета «Известия».
По данным издания, цены у разных производителей выросли от 25 до 38 процентов. В среднем, если год назад упаковка лекарства стоила 14 рублей, сейчас за нее придется заплатить 17 рублей.
Причиной подорожания называют рост стоимости импортных фармсубстанций, из которых в России делают популярное обезболивающее. Также на выросший ценник повлияли подешевевший рубль и остановившееся из-за коронавируса химпроизводство в Индии и Китае. Еще одним фактором стало исключение анальгина из перечня жизненно необходимых и важных лекарственных препаратов, из-за чего государство перестало регулировать цену на него.
Как следствие, предупреждают опрошенные изданием эксперты, в будущем возможен рост цен и на другие лекарства.
28 июня стало известно, что в России выросли продажи антидепрессантов. В период с 1 марта по 1 июня этого года россияне приобрели антидепрессантов примерно на десять процентов больше, чем за аналогичный период в прошлом году. В частности, в марте рост продаж составил 35 процентов по сравнению с прошлым годом, а за последние две недели месяца — на 60 процентов.