Физическая химия | Термодинамика
Термодинамика— раздел физической химии, отвечающий на вопрос: «Почему идет та или иная реакция?» Вы никогда не задумывались, почему например кислород может реагировать с водородом, но не может со фтором, или почему в конкретной реакции выделяется конкретное количество теплоты, ни больше, не меньше? Изучение термодинамики связано с необходимостью отвечать на эти, с одной стороны простые, с другой, весьма сложные вопросы. Работой над теорией химической термодинамики занимались такие известные ученые как Джозайя Уиллард Гиббс, Герман Иванович Гесс в основах современной термохимии лежат принципы, сформулированные Антуаном Лораном Лавуазье и Пьером-Симоном Лапласом.Также существует общая система законов термодинамики, с которой вы наверняка знакомы, однако в рамках химической термодинамики оно сформулированы немного по-другому. Первый закон термодинамики гласит, что энергия, сообщенная системе извне, расходуется на увеличение внутренней энергии системы и работу, совершаемую ей.
Но в отличии от физики, где изменение внутренней энергии часто тождественно с изменением температуры, в химии оно может характеризовать превращения вещества. Это происходит из-за перегруппировки химических элементов в новые комбинации, с другой энергией связи, в результате чего в систему освобождается некоторое количество энергии, или из системы поглощается её некоторая часть. Внутреннюю энергию химической системы характеризует величина, называемая энтальпией. Здесь следует указать, что максимальная устойчивость химической системы, как и любой другой системы, соответствует минимуму энергии. Из этого следует, что процессы, в которых уменьшается энергия системы, являются энергетически выгодными и протекают самопроизвольно. Но куда девается эта энергия? Конечно же выделяется в виде теплоты! Так мы пришли к простому выводу о самопроизвольности экзотермических реакций, вспомните хотя бы реакции горения.
Суть мы поняли, переходим к практическому применению этой теории. Пройдем по пути великих Гиббса, Лавуазье, Гесса и Лапласа и превратим привычные законы сохранения энергии в теорию, позволяющую рассчитывать тепловой эффект реакций. Начнем с закона Лавуазье–Лапласа, согласно ему, изменение энтальпии (тепловой эффект со знаком -) прямой реакции равно изменению энтальпии обратной реакции. Логично, ведь иначе было бы возможным существование бесконечного источника энергии. Теперь перейдем к законам Гесса, наш соотечественник установил, что тепловой эффект реакции не зависит от пути её протекания. То есть, превращение А в Б сопровождается изменением энтальпии равным суммарному изменению энтальпии превращения А в В и В в Б.
Но этим труд Гесса не ограничился, следствие из его законов гласит, что энтальпия реакции (не пугайтесь) равна разности суммы удельных энтальпий образования продуктов реакции и суммы удельных энтальпий образования исходных веществ. Теперь по порядку, удельная энтальпия образования вещества— это количество теплоты, которое выделяется или поглощается в результате его образования из простых веществ. Из этого понятно, что удельная энтальпия образования простых веществ равна 0*, а тепловой эффект реакции, по сути, разница между конечным и начальным состоянием системы. Для того, чтобы найти эту величину, необходимо либо измерить её, что не всегда бывает возможно, например для веществ, которые нельзя получить из простых веществ, либо рассчитать через реакции, в которых участвуют вещества с измеренной энтальпией образования. Таким образом уже собрана информация о тысячах различных веществ и, пользуясь справочником, можно рассчитать тепловой эффект любой реакции.
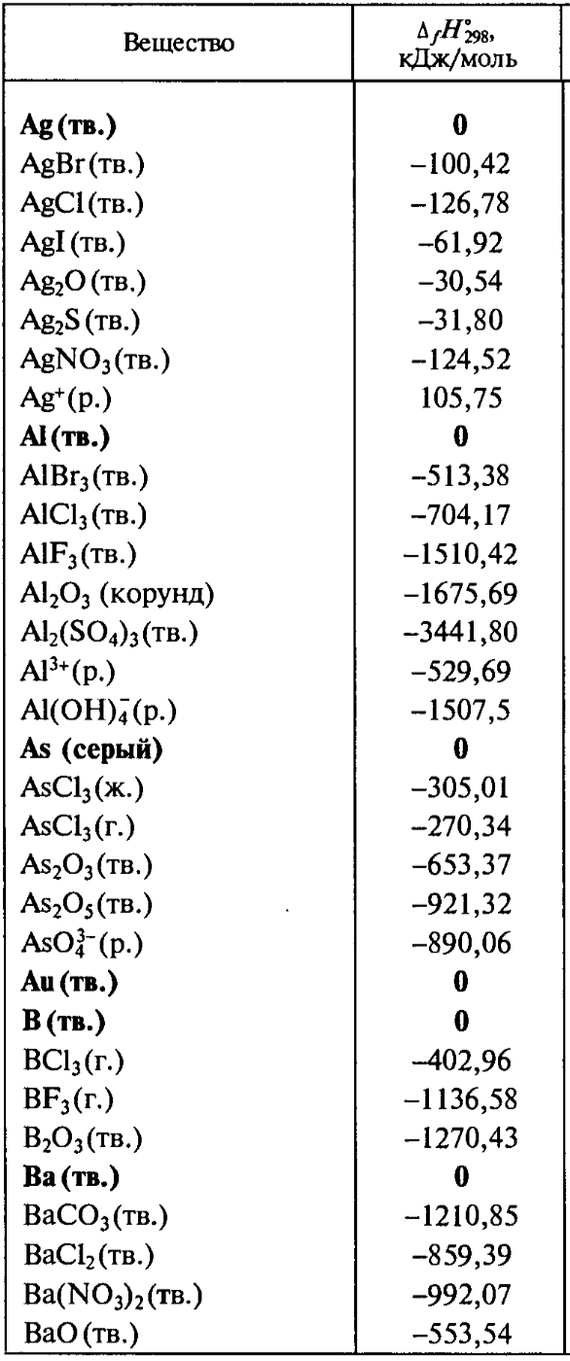
Пример справочной таблицы.
С изменением внутренней энергии разобрались, однако кроме энтальпии существует и другая фундаментальная величина– энтропия. Численно она равна отношению количества теплоты, переданной системе, к абсолютной температуре протекания процесса.
По аналогии с энтальпией можно рассчитать энтропию реакции, пользуясь законом Гесса и зная удельные энтропии образования. Реакции с положительным изменением энтропии идут самопроизвольно.
Из утверждений, приведенных выше, следуют очевидные истины вроде самопроизвольности реакций горения и разложения веществ, однако если задуматься, то можно понять, что реакций, где выполняются сразу два термодинамических условия, существенно меньше, чем реакций, о протекании которых нельзя судить на качественном уровне. Возьмем например реакцию водорода с кислородом, эта реакция экзотермическая, но в её результате количество газообразных веществ уменьшается, следовательно, так как не выполняется одно из условий протекания реакции, она не идет. Это само собой не верно, водород и кислород достаточно активно реагируют, а их смесь в соотношении 2 к 1 дает гремучий газ. Так в чём же дело? Почему одно из условий превалирует над другим?
Ответ на этот вопрос нам поможет сформулировать Джозайя Уиллард Гиббс.
Здесь мы вводим ещё одну термодинамическую характеристику химической системы– энергию Гиббса, она связывает энтропию и энтальпию (а точнее их изменения) и абсолютную температуру, относительно многих законов физической химии энергия Гиббса вычисляется по простой формуле dG=dH-T*dS (d- это дельта, знак изменения, эти величины нельзя измерить в абсолютных значениях). Если энергия Гиббса меньше 0 – реакция идет самопроизвольно, больше 0 – не идет в данных условиях, равна 0 – установилось химическое равновесие. Из этого можно сделать несколько простых выводов:
Именно по энергии Гиббса можно с уверенностью судить о возможности протекания химических реакций, для неё, как и для энтропии с энтальпией существует своя удельная величина– стандартная (удельная) энергия Гиббса, а рассчитать энергию для конкретной реакции можно так же по закону Гесса.
Если вам показалось, что было достаточно просто, то вот вам две оговорочки: :)
-Стандартные энтальпия, энтальпия и энергия Гиббса измерены в стандартных условиях и справедливы только для относительно узких температурных рамок, а для сверхбольших давлений энергия Гиббса в классическом виде неприменима.
-Не все реакции подчиняются правилам химической термодинамики, поскольку существует множество термодинамически нестабильных веществ, например оксиды азота, для которых образование из простых веществ сопровождается не выделением (как почти для всех веществ), а поглощением тепла.
Справа в столбце удельная энтальпия образования в кДж/моль (не забывайте, что изменение энтальпии противоположно по знаку тепловому эффекту реакции)
Иллюстрации и фрагменты текста из учебника "Неорганическая химия" Ю.Д. Третьякова