Залез в аптечку и сделал СВЕТЯЩИЕСЯ КРИСТАЛЛЫ - делаем люминофоры дома !!!
Заскучал в очередной раз, ну чтож - ДА БУДЕТ ДОМАШНЯЯ ВАРКА!!! Делаем снова все на гряяяяззз из борной кислоты и подручных веществ из аптечки и кухонного шкафа. Ребята погнали!!!
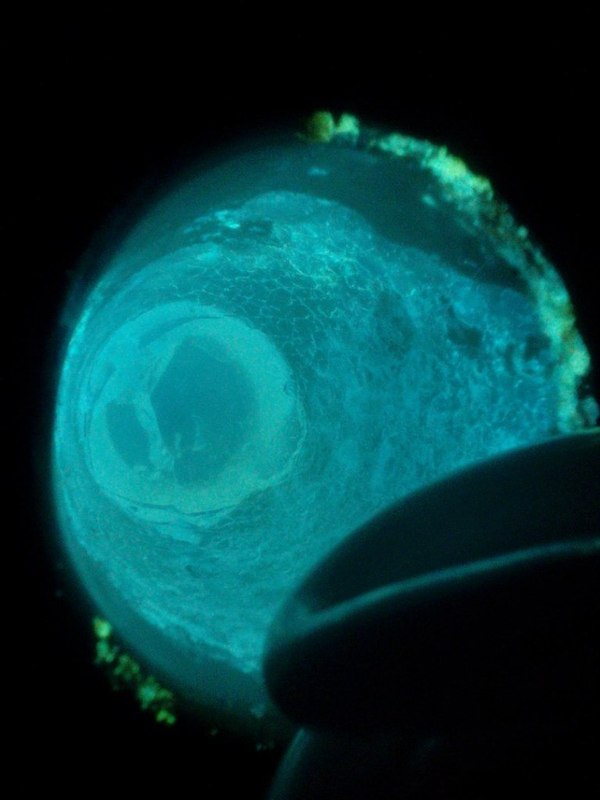
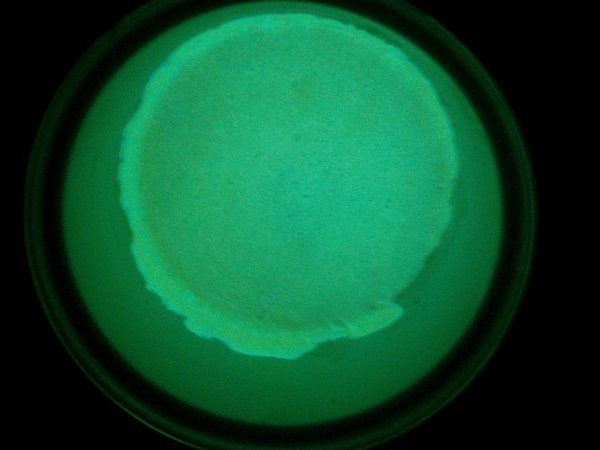
И вот например простые кристаллы из борной кислоты и салициловой кислоты!
Для того чтоб сделать люминофор, не плохо бы понять, что это за вещество. Люминофор это такое вещество, которое поглощает энергию и преобразовывает её в световое излучение. В зависимости от фильтра находящегося на поверхности люминофора или его примеси, свечение может быть различного цвета. У люминофора есть несколько видов: радиолюминофоры, электролюминофоры, рентгенолюминофоры, фотолюминофоры, катодолюминофоры. Фотолюминофор - порошок, он наделен способностью светиться в темное время суток под воздействием искусственного или естественного освещения.
Убедительная просьба ознакомиться с предыдущими постами дорогие друзья, сегодня мы рассмотрим общие моменты по получению таких кристалликов.
Делал вот по этим видосам, друзья пожалуйста ознакомьтесь, чтобы быть в теме:
Теперь о некоторых тонкостях, которые нужно знать, чтобы приготовить такие вот кристаллы:
Борные люминофоры состоят собственно из борной кислоты, которая выступает как основа с добавлением различных органических соединений, выступающие как активаторы промежуточных соединений, образующихся при частичном обезвоживании борной кислоты. Эти люминофоры могут быть приготовлены как при сплавлении до 200°С, так и интенсивным высушиванием смеси под вакуумом при 100°С
Эти пункты очень важны для выяснения общих свойств борных люминофоров и представляют следующий перечень:
• Свечение активированной борной кислоты под ультрафиолетовым излучением происходит из-за присутствия следов органического материала.
• Люминофор мог быть приготовлен с использованием самой борной кислоты, частично обезвоженной борной кислоты, так же, используя полностью обезвоженную её форму в качестве борного ангидрида - B2O3.
• Самые лучшие и успешные результаты получены с использованием частично обезвоженными борными промежуточными соединениями, которые возникают при обезвоживании борной кислоты.
• Люминофор быстро теряет свою способность к люминесценции, как при воздействии влаги находящейся в воздухе, так и при сильном обезвоживании - люминесценция у борного ангидрида намного более слабая, чем у частично обезвоженных продуктов борной кислоты.
• Интенсивность люминесценции сильно уменьшается под воздействием кислорода на борные люминофоры.
• В качестве активирующих свечение веществ могут применяться многие органические препараты и соединения.
• Тесное взаимодействие между активатором и основой не только возможно, но также вероятно в случае синтеза, который исключает обезвоживание борной кислоты путём нагрева.
• Не распавшаяся органическая молекула (активатор) единственная причина люминесценции и также единственный центр вызывающий световой эффект, а борная кислота предоставляет необходимые физические условия, наряду как в борном ангидриде в качестве активатора по большей части выступает элементарный углерод.
• Борный люминофор имеет структуру схожую с твёрдыми растворами.
• Многие борные люминофоры обладают флюоресценцией, фосфоресценцией и некоторые термолюминесценцией с заменой полос излучения.
• Большинство борных люминофоров имеют полосы возбуждения и полосы излучения в спектре, от двух до четырёх.
• Свойства борных люминофоров отличаются по нескольким параметрам от люминофоров, активированных примесями металлов, и механизмы люминесценции также резко отличаются.
• Примеси металлов как активаторов борной кислоты или борных промежуточных соединений не являются доминирующими над органическими активирующими соединениями. Флюоресценция и фосфоресценция при добавке солей металлов возникает не по причине активации металла, а по причине взаимодействия кислотного остатка соли металла с борной кислотой или её промежуточными соединениями при частичном обезвоживании, а так же распада кислотного остатка соли металла на другие стабильные составляющие при температуре приготовления. (Пример тому - внесение в борную кислоту ацетатов металлов или формиатов).
• Излучающие центры длительной фосфоресценции и короткой флюоресценции имеют между собой различия.
• Структуры фосфоресцирующих центров борного ангидрида отличаются от люминофоров борной кислоты и от сульфидных люминофоров металлов второй группы.
• Подавляющее большинство борных люминофоров имеют отдельные полосы поглощения (возбуждения), как в видимой части спектра, таких, как фиолетовой и синей, а так же большинство из них имеют оптимум поглощения в ультрафиолетовой части спектра – ближнего (А), среднего (В) и чуть реже, дальнего (С) ультрафиолета.
• Некоторые корреляции и порой существенные изменения присутствуют между составом активаторов, их вносимого количества, цвета излучения и интенсивности фосфоресценции, а так же между цветом и интенсивностью излучения фосфоресценции и флуоресценции, у одного и того же люминофора.
• Имеет место изменение цвета флуоресценции и фосфоресценции при возбуждении различными источниками излучений у одного и того же борного люминофора.
• Имеются различия между цветом флюоресценции и фосфоресценции при возбуждении одного и того же люминофора одним и тем же источником возбуждения.
• Время послесвечения в темноте не особо длительное, у самых успешных образцов фосфоресценция не превышает двух минут. Самое большое уменьшение интенсивности фосфоресценции, наблюдается в течение первых тридцати секунд после прекращения возбуждения.
• Цвет флюоресценции активирующего соединения в состоянии чистого вещества-реактива или растворённого в органическом растворителе, отличается от цвета флюоресценции люминофора на борной кислоте, приготовленного с ним же, и их излучения фиксируются в различных частях спектра.
• Активирующее органическое вещество не обязательно должно обладать флюоресценцией само по себе и флуоресцентное вещество не всегда приводит к активации борной кислоты. Таким образом, нет никакой связи между флуоресцентной способностью активатора и его способностью активировать свечение. Есть некоторые исключения, например соединение - флуоресцеин. Это общее заключение целиком согласуется с работами Томашека.
В качестве активаторов для борной кислоты могут быть применены углеводороды, гетероциклические соединения, оксисоединения, карбоновые кислоты, сульфокислоты и особенно флуоресцеин, который исследовался в борнокислотных соединениях наиболее часто. Увеличение боковой алифатической цепи действует угнетающим образом. Многие окрашенные вещества, исключая флуоресцеин, не активируют борную кислоту. Так же введение галоидов и нитрогруппы ухудшает или даже совсем уничтожает фосфоресценцию. Аминогруппы и имидогруппы, связанные не циклически, то же ухудшают эффект. Вводимые ацетаты, формиаты и прочие органические кислотные остатки дают позитивный, но часто не наилучший эффект. Введение сульфатов дает незначительный эффект. Действующие концентрации активаторов достаточно низки, но оптимумы значительно отличаются.
Наилучшие активаторы – флуоресцеин, α-оксинафтойная кислота и терефталевая кислота. Теперь, немного подробнее о некоторых активаторах и свойствах их борных люминофоров.
Ну и конечно же МЕГА КРИСТАЛЛ!!! В кастрюле на углях аккуратно расплавил борную кислоту и всыпал активатор - ФЛУОРЕСЦЕИН. Все, люминофор готов, масса кристалла 500 гр!!!!
Полосы фосфоресценции при борной кислоте представляют собой полосы разделённые и имеющие много максимумов, но более размытые, чем, например, в затвердевшем жидком воздухе или этиловом спирте, где линейчатость спектра выступает резко. При этом, чем резче полоса и ближе по своему строению к линейчатому спектру, тем меньше влияние температуры, но как правило, борные люминофоры имеют весьма низкий температурный предел верхнего уничтожения флюоресценции и при повышенных температурах и изменение температуры в пределах нормальных условий не влияет на послесвечение. Обычно уже при +160°С все борные люминофоры не светят. Исключением являются лишь люминофоры с флуоресцеином и нафталевым ангидридом.
Все эти люминофоры не обладают ни одним видом вынужденного затухания. Как указывалось выше, борные люминофоры возбуждаются лишь видимым светом и УФ. Оптимум в основном приходится на ближний и средний спектр ультрафиолетового спектра. Ни от катодных, ни от рентгеновских, а так же от излучения радиоактивных элементов эти люминофоры не светят. Даже вещества, подобные дигидроколлидин-дикарбоноводиэтиловому эфиру, хорошо возбуждающемуся от радиоактивных излучений, будучи введён в борную кислоту, дают люминофоры, прекрасно возбуждающиеся на свету, но совершенно не реагирующие на препараты радия. То же относится к пентадецилпаратоликетону, хорошо реагирующий на катодное излучение.
ДОПОЛНИТЕЛЬНУЮ ИНФУ ПО ЛЮМИНОФОРОМ МОЖНО ПОСМОТРЕТЬ ТУТ:
https://vk.com/dustximxabrprom
КСТАТИ!!!
21 мая - День Химика.
50 лет назад Химический факультет МГУ начал проводить День Химика под знаком элементов таблицы Менделеева.
Ежегодно День Химика собирает вместе студентов, аспирантов, преподавателей и сотрудников, а также выпускников МГУ и гостей из других вузов России и ближнего зарубежья.
Традиционно заглавный элемент определяется порядковым номером Дня Химика. Сурьма, будучи пятьдесят первой, стала отправной точкой для Дня Химика-51.
День Химика 2016 - это повод отдохнуть, встретиться с друзьями, погрузиться в атмосферу родного факультета! Спортивные состязания, весёлые конкурсы, непредсказуемый аукцион, традиционное Представление на ступеньках, незабываемая Ночь Химика, а также множество других важных и интересных событий - вот что ждёт вас 21-го мая!
Всем удачи друзья, надеюсь вам полезна статья по получению таких кристалликов)
Удачи, спасибо за подписку и поддержку, это очень круто!!!!
Развлекаемся дома и делаем люминофоры из аптечки
Ребятки, всем привет. Сижу я значит дома, и понимаю что очень скучно проходит время. Почему бы не сделать какую нибудь интересную штуку??? ЛЮМИНОФОР!
Делал вот по этому ролику с ютуба https://www.youtube.com/watch?v=MERDM5uz6DU
Заценивайте по фоткам что получилось))
Поиграем в бизнесменов?
Одна вакансия, два кандидата. Сможете выбрать лучшего? И так пять раз.
Фаер-шоу на уроках химии или техника безопасности.
Вспомнил историю благодаря посту http://pikabu.ru/story/science_bitch_4074450
Когда я учился в старших классах, однажды на уроке химии меня вызвали к доске продемонстрировать горение гремучего газа. Не знаю, на что рассчитывала учительница, возможно она хотела кого-нибудь поджечь. При помощи реакций мы с ней набрали в полулитровую пластиковую бутылку водород и кислород. Потом я должен был ее аккуратно открыть и поджечь газ. В результате столб пламени долетел до третьей парты! Никто не пострадал только потому, что случайно в классе в этот день было не так много народу, а средний ряд из трех традиционно не пользовался у нас популярностью, все сидели либо у стены, либо у окна. И потому, что у меня не дрогнула рука и я направил пламя ровно в середину класса, а не в учеников или в подвесной потолок. Так я себя немного почувствовал Тиллем Линдеманном.