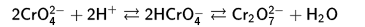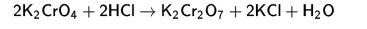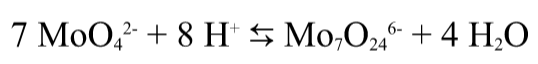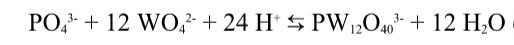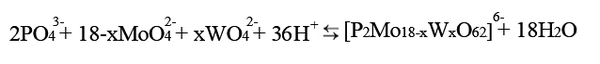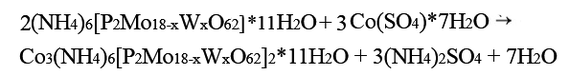Пока выдалось время, решил сделать пост о теме своей научной статьи и бакалаврской работы.
(Описывал наиболее понятным языком, но те, кто о химии вообще не имеет представления, хотя бы посмотрят фотки и картинки)
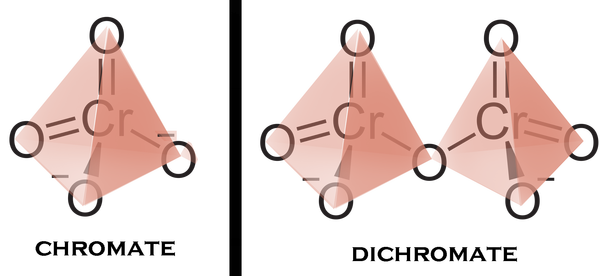
Итак, что же такое гетерополисоединения? В химии существует такой тип веществ, под названием полиоксометаллаты. Известным еще со школы веществом данного типа является дихромат, который получают подкислением хроматов:
(Или получение конкретно дихромата калия из хромата калия)
Это хорошорастворимые соли хромовой и дихромовой кислоты соответственно, и имеют следующий внешний вид:
Но больше интересна их структура. Хромат-анион представляет из себя своего рода тетраэдр, с хромом в центре и кислородами на вершинах. Структура дихромат-аниона отличается тем, что представляет из себя два тетраэдра, при том что один из кислородов является общей вершиной для двух тетраэдров, иначе говоря образуется "мостиковая связь" металл-кислород-металл. Это вещество можно отнести к самому простому примеру полиоксометаллата.
Однако анионы кислот других переходных металлов образуют более сложные по структуре полиоксометаллаты (например при подкислении молибдата получается структура, состоящая из семи октаэдров, содержащих в центре молибден и кислород на вершинах)
Вышеописанные разновидности полиоксометаллатов называются изополиоксометаллаты.
Но существует еще второй вид, с более сложной структурой и называется он гетерополиоксометаллаты или гетерополисоединения (ГПС).
Гетерополисоединения образуются, когда процесс подкисления происходит в присутствии постороннего кислородосодержащего аниона, от которого в последствии отщепляется и попадает в структуру гетероатом (например фосфор, при подкислении вольфрамата в присутствии фосфата)
Структура ГПС, изображенного в примере выглядит следующим образом: Фиолетовый шарик в центре - это фосфор (гетероатом). В центре каждого из 12 синих октаэдров находится вольфрам (полиатом) , а на вершинах - кислород, который может являться одновременно вершиной двух октаэдров. Такая структура носит название Структура Кеггина
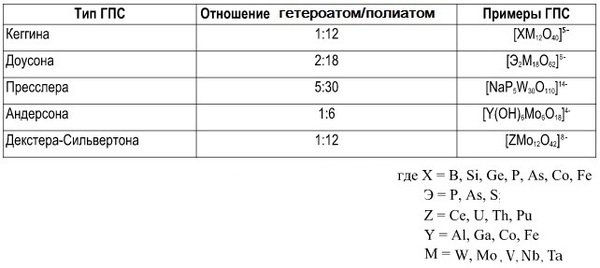
Всего есть 6 основных структур (не считая множество их изомеров), которые синтезируются исходя из начальных пропорций веществ, содержащих гетероатом и полиатом.
Все это говорит о том, что существует огромное количество различных ГПС с различными свойствами и областями применения, так например кремниево-ванадиевые соединения используются при получении антибиотиков, а фосфорно-молибденовые, как оранжевый пигмент.
Однако моя работа посвящена конкретному фосфорно-молибдо/вольфрамовуму гетерополисоединения со структурой Доусона (аналогично, предыдущей модели, два фосфора внутри структуры, в общей сложности 18 молибдена/вольфрама внутри каждого октаэдра и 62 кислорода на вершинах октаэдров)
Соединения структуры Доусона обладают очень большой растворимостью (ок 200г/л), что облегчает работу с ними. Получается такое ГПС подкислением солей вольфрамовой и молибденовой кислоты в присутствии фосфатов (но в других пропорциях, нежели для структуры Кеггина)
Одновременно вольфраматы и молибдаты берут не случайно; соли вольфрама устойчивы, но являются плохими окислителями, молибден же наоборот - соли не такие устойчивые, но зато обладают окислительными способностями. В связи с этим, целесообразно рассматривать два соединение с отношением W:Mo=12:6 и W:Mo=6:12.
При выделении гетерополисоединений из раствора они образуют монокристаллы, к сожалению очень маленького размера, так что для их наблюдения используется оптический микроскоп. Так же следует заметить, что ГПС очень гигроскопичные вещества, даже в сухом виде на одну их молекулу приходится 11 молекул воды. Ниже приведены фотографии кристаллов ГПС с соотношением W:Mo=12:6 и 6:12 соответственно
(100 µm = 0,1 мм; примерно ширина человеческого волоса)
Как видно, образуются ромбоэдрические кристаллы. Наблюдать их можно только в маточном растворе, поскольку при полном осушении они срастаются и разделить их уже становится невозможно. Благодаря образованию монокристаллов возможно определить атомную структуру конкретного образца, проводя рентгеноструктурный анализ. Молекулярные массы вышеизображенных веществ чрезвычайно велики: 4144 г/моль для (NH4)6(P2W12Mo6O62)*11H2O и 3616 г/моль для (NH4)6(P2W6Mo12O62)*11H2O.
Интересная особенность ГПС, требующая и сейчас дополнительных исследований, это реакция р-ра с металлами. В результате последние могут вставать на место полиатома (замещать вольфрам/молибден) и образовывать насыщенные синие и зеленые р-ры. Ниже приведены сильноразведенные растворы продукта реакции ГПС с металлическим серебром и железом (конц. 0.05% по массе)
Эти вещества также могут образовывать монокристаллы, правда еще меньшего размера, вплоть до диаметра лейкоцитов. Ниже приведены кристаллы, образовавшиеся в ходе реакции ГПС с металлическим цинком, железом и никелем соответственно:
Но все же, поиск практического применения этой способности ГПС реагировать с металлами, является сейчас объектом исследований.
Гетерополисоединения обладают еще одной интересной особенностью, которую как раз я и описываю в своей дипломной работе и год назад получил патент: вещество может взаимодействовать с солями переходных элементов в низшей степени окисления (например сульфат кобальта (II) или хлорид марганца (II) ) и образовывать так называемые гетерополикомплексы, где ион переходного металла (катион) будет связан с гетерополианионом.
Интересная особенность в том, что этот комплекс очень "чувствителен" к аммиаку и органическим азотистым производным: ГП-анион понижает электродный потенциал катиона, иначе говоря позволяет катиону переходного металла образовывать комплекс с азотистым производным и легко переходить в окисленную форму (в Co(III) или Mn(III)), образуя комплекс насыщенного синего цвета, соответственно концентрации присутствующего азотистого соединения. А поскольку большинство органических соединений-примесей не поглощают синий цвет и оптически не мешают определению искомого вещества, то образование определенного синего оттенка легко улавливается спектрофотометром, показания которого и говорят о той или иной концентрации.
Проще говоря, это новый спектрофотометрический метод определения концентрации азотистых соединений в атмосфере (вплоть до 0,001%), имеющий ряд преимуществ перед существующими методами, в которых порой используется токсичные реактивы или сложное оборудование, которое требует определенной квалификации от рабочего.
На данный момент синтез гетерополикомплекса находится еще в процессе и занимает 7-10 дней (проходит реакция между перетёртыми в ступке семиводным сульфатом кобальта(II) и ГПС с отношением W:Mo=12:6, 9:9 и 6:12, представленные соответственно на фото)
В дальнейшем, образцы будут протестированы на этилендиаминтетрауксусной кислоте, проведен ряд анализов, в частности ИК-спектроскопия, которая даст точные данные о составе и строении вещества.
Тем не менее, всё, что здесь описано - лишь крупица в изучении ГПС. Вещества, образованные различными элементами, имеющие ту или иную структуру и её изомер, обладают различными свойствами и находят себе применение в качестве аналитических реагентов, в нефтяной и газовой промышленности, в медицине и технике, а также в других отраслях науки, развитие которых является основной задачей на данный момент.
P.S. если вы поняли всё, что здесь описано, то ваше понимание химии как минимум на уровне четвертого курса)