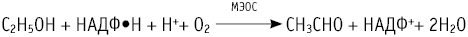Строение и метаболизм мышечной ткани
Движение. Как много и как мало в данном слове. Для человека такое естественное свойство его опорно-двигательного аппарата открывает тысячи возможностей, и каждый наш день наполнен движением. И человек вовсе не заключен в своем теле, как в душной камере, напротив, люди вольны использовать ресурсы, данные им природой во всю мощь. Мышцы – удивительная ткань, возможности которой в условиях меняющихся нагрузок поражают воображение, а функциональные возможности скелетно-мышечной системы восхищают изящностью исполнения. А потому интересно было бы взглянуть на то, как же обеспечивается мышечная работа в целом.
В мышечной ткани происходит преобразование химической энергии в механическую работу. В качестве источника энергии химических связей используется АТФ, получаемая мышечными клетками в результате метаболических процессов.
Миоциты разных типов мышечной ткани обладают различным набором ферментов, а также отличаются по количеству митохондрий и миоглобина – белка, осуществляющего перенос кислорода. Мышечные волокна, выполняющие взрывную работу за короткое время покрывают необходимые энергетические затраты посредством анаэробного гликолиза, ферменты для осуществления которого присутствуют в клетках в норме в надлежащем количестве. За счет сравнительно низкого содержания миоглобина в клетках таких мышечных волокон, под микроскопом они выглядят светлыми и потому называются белыми волокнами. Им в противоположность существуют красные мышечные волокна, которые обеспечивают совершение продолжительной работы мышцами, и характеризуются более высоким содержанием миоглобина. Клетки красных мышечных волокон, которые, кроме прочего, составляют и сердечную мускулатуру, нуждаются в кислороде и потому имеют много митохондрий, а также богаты ферментами цикла Кребса и дыхательной цепи.
Глюконеогенез в мышечной ткани не протекает из-за отсутствия в ней нужных для его свершения ферментов. Продукты обмена веществ в мышечной ткани (лактат, возникающий при анаэробном гликолизе из пирувата, и аланин, являющийся продуктом трансаминирования из пирувата и аминокислот), пройдя циклы Кори и аланина, транспортируются по кровеносному руслу в печень для глюконеогенеза: в результате реакции повторного трансаминирования в печени возрастает количество необходимого пирувата. Гликоген печени при необходимости может стать источником глюкозы для мышечной ткани, что замыкает данный цикл. Синтез и разрушение гликогена в мышцах подчиняется гормональному контролю: инсулин способствует захвату глюкозы клетками и синтезу гликогена, тогда как катехоламины путем повышения уровня цАМФ стимулируют активность гликогенфосфорилазы. Катаболическое воздействие глюкокортикоидов ведет к разрушению мышечных белков и мобилизации аминокислот, которые в печени задействуются в глюконеогенезе.
Гидролитическое отщепление фосфатных групп от молекул АТФ дает мышечным клеткам необходимую для сокращения энергию. Еще одним макроэргическим фосфатом, используемым в мышцах, является креатинфосфат, отщепленная от которого креатинкиназой фосфатная группа переносится на АДФ. Неферментативно образующимся побочным продуктом превращения креатинфосфата является креатинин, который регулярно обнаруживается в крови и выводится через почки (суточное выводимое с мочой количество креатинина пропорционально мышечной массе). Таким образом, креатинфосфат представляет собой своего рода энергетический резерв, обеспечивая скорое восстановление количества молекул АТФ. У такой системы восстановления АТФ есть важное преимущество перед накоплением АТФ, заключающееся в том, что после превращения АТФ в АДФ вследствие разрыва фосфодиэфирной связи не создается невыгодного соотношения АТФ/АДФ, что могло бы негативно сказываться на функции АТФ из-за концентрационной зависимости от энергии Гиббса. Есть и еще одна система, служащая восстановлению АТФ в мышечной ткани, ключевым ее ферментом является аденилаткиназа (миокиназа), способная образовывать АТФ за счет АДФ, а также фосфорилировать АМФ до АДФ.
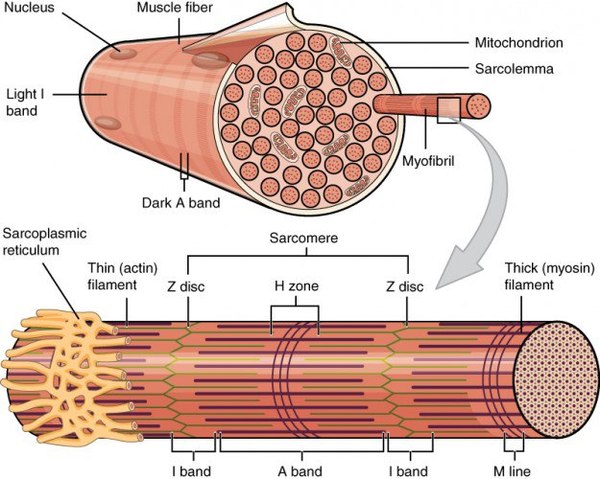
Строение мышечных волокон
Строение миофибрилл
Клетки поперечно-полосатой мускулатуры отличаются от клеток гладкой мышечной ткани и ткани сердечной мышцы. Они образуют единый многоядерный синцитий. Клеточные ядра при этом смещены к краю клеток, а основное внутриклеточное пространство занято миофибриллами. Миофибриллы окружены саркоплазматическим ретикулумом, что достигается посредством формирования продольных и поперечных трубочек, а также лабиринтообразных впячиваний плазматической мембраны, благодаря чему возбуждение достигает этих участков. Плазматическая мембрана миоцитов – сарколемма – укреплена с внутренней стороны белками цитоскелета. В связывании с интегральными мембранными белками задействован белок дистрофин, мутации в гене которого приводят к развитию миодистрофии.
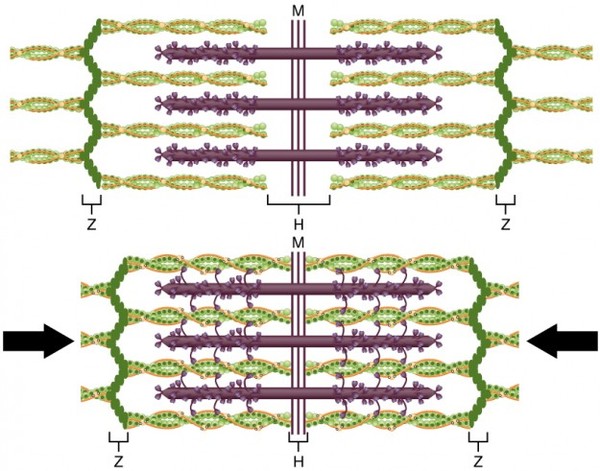
Скелетные мышцы структурно строго организованы в мышечные пучки, волокна, фибриллы и филаменты. Фибриллы поперечно-полосатых мышц состоят, прежде всего, из толстых миозиновых филаментов и тонких филаментов. Первый тип состоит из миозина и молекулярные моторные единицы. Второй тип филаментов включает F-актин и актин-связывающие белки – тропомиозин и тропонин. Головки тяжелых цепей миозина выдаются кнаружи и способны формировать связи с тонкими актиновыми филаментами. Актиновые филаменты, в свою очередь, закреплены на структурных белках, образующих так называемые Z-диски. Типичная поперечная исчерченность данного типа мышечной ткани, узнаваемая гистологически, создается благодаря устройству и расположению саркомера – функциональной единицы мышцы - который представляет собой участок миофибриллы между двумя Z-мембранами. Актиновые филаменты связываются как между собой, так и с Z-белками. Два других белка – титин и небулин – принимают участие в структурировании миофибрилл в процессе сокращения и расслабления. Титин прикрепляется к белкам Z-структуры и к М-линиям, сформированным миозином и структурными белками. Небулин закреплен в Z-структурах и исполняет регуляторную роль в построении тонких филаментов.
Несмотря на строгую организацию, скелетная мускулатура являет собой крайне гетерогенную систему относительно устройства и выполняемых функций. С одной стороны, это позволяет подстроиться мышцам под возлагаемую на них нагрузку путем разборки / увеличения количества саркомеров или миофибрилл, с другой стороны – обмен различными изоформами белков разных свойств и качеств обуславливает функциональную реорганизацию.
Мышечное сокращение
Схематичное строение саркомера.
Фиолетовым изображен миозин, головки его тяжелых цепей обращены к нитям актина и соединяются с ними. Движение головок миозина при сокращении ведет к подтягиванию актиновых филаментов к центру. Также обозначено прикрепление актиновых нитей к Z-дискам.
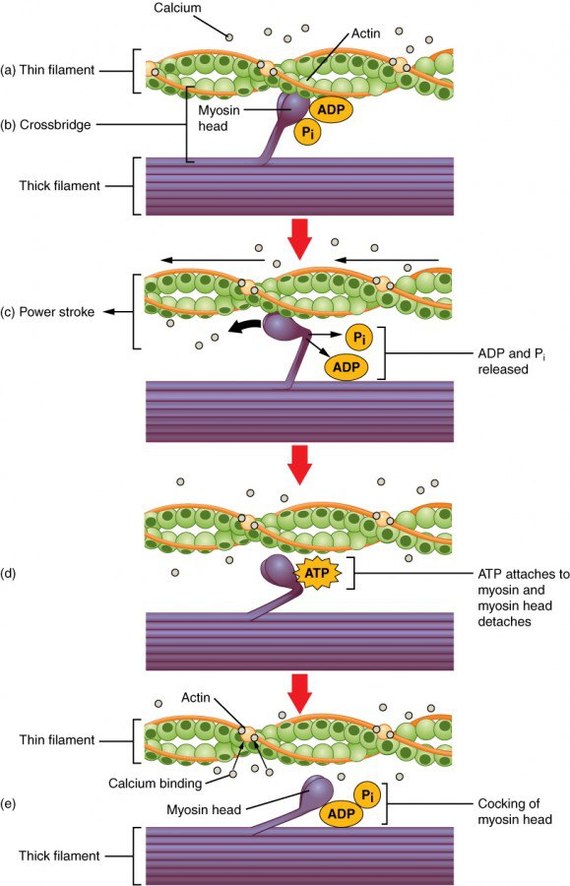
Сокращение мышц находится в зависимости от концентрации ионов кальция. Передача возбуждения на нейромышечные окончания поперечно-полосатых волокон ведет к деполяризации наружной мембраны и открытию кальциевых каналов в мембране саркоплазматического ретикулума, простирающегося через все саркомеры. Концентрация ионов кальция в цитозоле резко возрастает и они связываются с тропонином С. Это приводит к конформационным изменениям субъединиц тропонинового комплекса, что имеет следствием смещение позиции тропомиозина. Это событие делает возможным связывание участков цепей миозина с актином. Головки миозина расщепляют АТФ до АДФ и остатка фосфорной кислоты, а высвобождающаяся при этом энергия обеспечивает смену ее конформации. Свершившееся связывание ионов кальция с тропонином С является необходимым для взаимодействия миозина с актиновыми волокнами, которое влияет на изменение угла между легкой и тяжелой цепями миозина. Такой сдвиг оканчивается перемещением актинового филамента к центру саркомера. Скольжение тонких филаментов относительно толстых приводит к укорочению саркомеров и сокращению мышцы. После этого происходит экзергоническая смена конформации головки миозина, а продукты гидролиза АТФ выносятся из клетки. Для повторения цикла необходимо очередное внесение АТФ в систему. Если мотонейроны перестают получать раздражение извне, то в работу вступает АТФ-зависимый кальциевый насос, перекачивающий более не востребованные ионы кальция из цитоплазмы в цистерны саркоплазматического ретикулума, где они связываются с кальсеквестрином, обладающим высокой связывающей способностью. В связи с этим концентрация свободных ионов кальция снижается, что энергетически облегчает последующее поглощение этих ионов.
Схема мышечного сокращения.
Молекулярные компоненты системы, осуществляющей впоследствии высвобождение кальция из саркоплазматического ретикулума , известны только частично. Начало сигнальной цепочки опосредуют дигидропиридиновые рецепторы плазматической мембраны, которые сменяют свою конформацию под влиянием деполяризации мембраны. Это приводит к открытию кальциевых каналов и активации рианодиновых рецепторов терминальных цистерн саркоплазматического ретикулума. Преходящее повышение концентрации ионов кальция в цитоплазме мышечных клеток ведет и к метаболическим изменениям. Например, дефосфорилированная форма киназы гликогенфосфорилазы может активироваться комплексом кальмодулина с ионами кальция, а потому мышечное возбуждение связано с кратковременным разрушением гликогена.
На этом наше повествование не оканчивается. В последующих постах обязательно подробнее рассмотрим биохимические превращения в мышцах, а также обратимся к особенностям, происходящим с мышцами при физических нагрузках.
Источники:
Löffler, Petrides Biochemie und Pathobiochemie, Springer, 2007
Волков, Несен Биохимия мышечной деятельности, 2000
Ленинджер, Основы биохимии
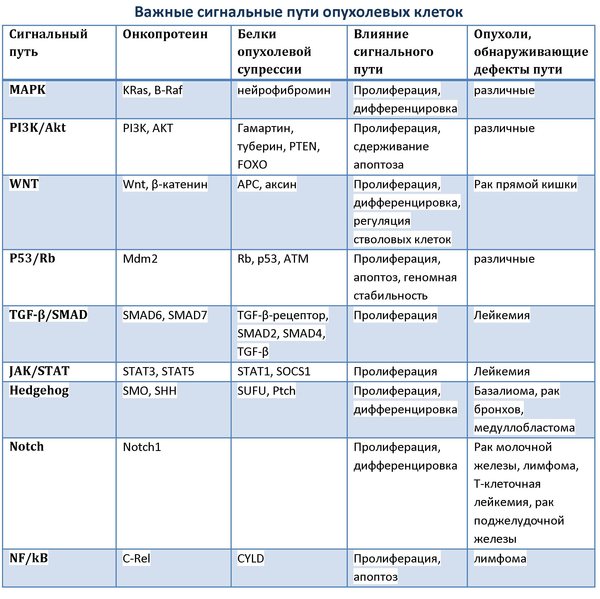
Внутриклеточные сигнальные пути и их роль в возникновении опухолевых клеток
Одним из условий для жизнеспособности сложного многоклеточного организма является стойкая и одновременно пластичная система меж- и внутриклеточных коммуникаций. Взаимодействия клеток между собой состоят в обмене адгезивными, гормональными или электрическими сигналами. На большинство поступающих в клетку сигналов она реагирует не напрямую: между поступающим раздражителем и специфической реакцией клетки лежит целый внутриклеточный каскад сигнальных молекул, представляющих собой путь биохимических превращений. Задача таких биохимических путей — усилить или ослабить передаваемый клетке сигнал и перевести его в такую форму, чтобы позволить реализоваться ответным реакциям.
Как возникновение опухолевых клеток, так и различия между клетками нормальной и опухолевой ткани берут своё начало среди базовых молекулярных механизмов. Появление каждой опухоли основывается на изменении активности, свойств и внутриклеточной концентрации онкопротеинов и белков опухолевой супрессии. Однако не сами белки опухоли как таковые, а именно их биохимическое взаимодействие и взаимосвязи, опосредующие передачу различных сигналов, лежат в основе зарождения опухолевой клетки. Комплексная взаимоорганизация всех задействованных в сигнальных путях белков формирует сеть внутриклеточной передачи сигналов, которая похожа на множество сотен сходящихся и вновь разветвляющихся, пересекающихся путей, переключающихся на различных белках, которые условно напоминают станции для пересадок в метро. Вся эта сеть представляет собой совсем не беспорядочный клубок, как может показаться поначалу, и в ней можно выделить несколько путей, которые в клетках большого количества опухолей дефектны и обнаруживают отклонения от нормы.
Одним из наиболее хорошо изученных путей является сигнальный путь MAPK (mitogen activated protein kinase), который начинается с активации трансмембранных рецепторов клетки и посредством участия цитоплазматических и ядерных протеинов принимает существенное участие в регуляции генной экспрессии. Конечно, стоит отметить, что многие сигнальные пути довольно сложно различать как функционально, так и биохимически, и между многими из них зачастую существуют прямые активирующие и/или угнетающие связи. Примером тому может служить сеть p53/Rb, объединяющая важные сигнальные пути, которые регулируют процессы клеточного деления, апоптоза и репарации ДНК.
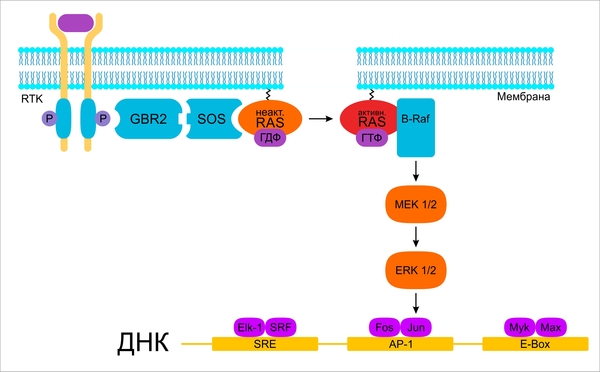
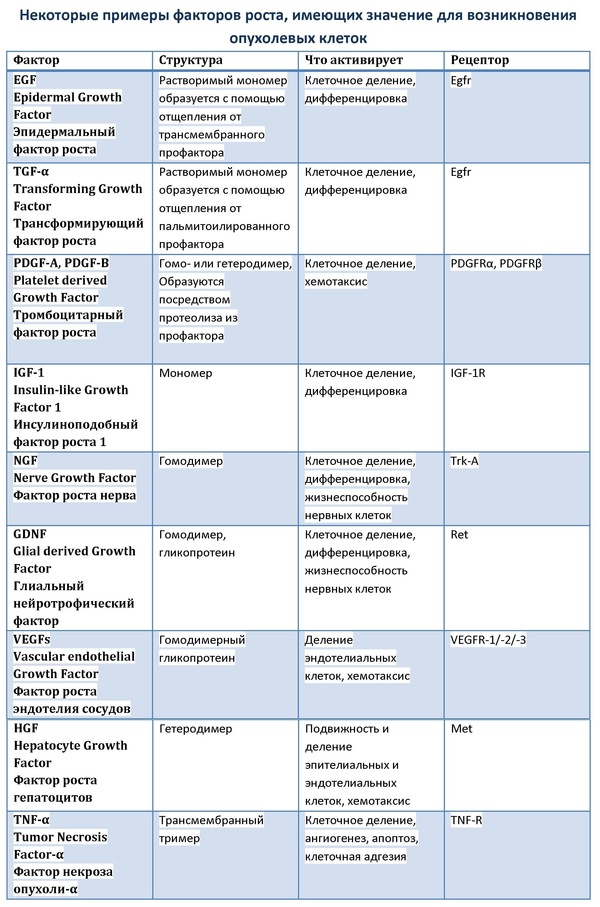
Наша цель сегодня — упрощённо рассмотреть лишь некоторые пути, чтобы составить общее представление об их функционировании и предназначении. Сигнальный путь состоит обычно из факторов, рецепторов, адапторных белков, ферментов, молекул вторичных мессенджеров. Каскад МАРК не является исключением. Как правило, данный сигнальный путь запускается посредством связывания факторов роста на специфических рецепторах с последующей димеризацией рецепторов. Рецепторы, с которых начинается путь МАРК, относятся к рецепторным тирозинкиназам (receptor tyrosine kinases, RTK). Стоит отметить, что со связывания именно с RTK начинается большое количество цепочек реакций, проводящих к целевым структурам клетки сигнал после образования комплекса фактора роста с соответствующим рецептором. В зависимости от подтипа рецептора и задействованного адапторного белка активируются те или иные пути.
Рецепторные тирозинкиназы: принципы устройства и функционирования
Все RTK включают в себя гликозилированный внеклеточный (экстрацеллюлярный) домен, на котором связывается лиганд, пронизывающий мембрану гидрофобный домен и внутриклеточную (интрацеллюлярную) часть с юкстамембранным доменом и одним или двумя каталитическими тирозинкиназными доменами. Каталитические домены состоят из аминотерминального АТФ-связывающего региона и карбокситерминального фосфотрансферазного домена. Многие гены рецепторных тирозинкиназ являются гомологами вирусных онкогенов. По структурным характеристикам внеклеточных доменов RTK можно разделить на несколько классов. К примеру, представители семейств PDGFR (рецептор тромбоцитарного фактора роста), FGFR (рецептор фактора роста фибробластов), VEGFR-1/-2 (рецептора фактора роста эндотелия сосудов) обладают соответственно пятью, тремя и семью Ig-подобными доменами. Однако, несмотря на многообразие классов рецепторных тирозинкиназ, механизм их активации практически одинаков. Согласно этой модели, в несвязанном состоянии между активными димерами и неактивными мономерами рецептора постоянно поддерживается равновесие. Присоединение лиганда ведёт к димеризации и смещает равновесие в сторону образования активной формы рецептора. Образование активных димеров может быть инициировано напрямую лигандами, связывающимися сразу с двумя мономерами, как, например, EGF (epidermal growth factor) способствует димеризации своего рецептора Egfr. Также связывание с лигандом может вызывать изменение конформации внеклеточного домена, что ведет к экспозиции сайтов связывания, как например, SCF (stem cell factor) вызывает димеризацию Kit-рецепторов. Итогом процесса димеризации является сближение внутриклеточных доменов друг с другом, вследствие чего наступает преходящая активация внутренней тирозинкиназной активности каталитических доменов, что приводит к трансфосфорилированию специфических остатков тирозина цитоплазматического домена. С фосфорилированным рецептором могут связываться белки с SH2-доменами. Комплекс связанного с таким белком рецептора может опосредовать активацию, например, какого-либо фермента или изменение реакционной способности белка. В отсутствие лигандов RTK представляют собой мономерные полипептидные цепочки (исключение — семейство рецепторов инсулина, которые состоят из 4 пептидных цепей, соединённых дисульфидными мостиками).
Классическая последовательность развития пути МАРК
После небольшого отвлечения на описание рецепторного взаимодействия, вернемся к пути МАРК. Активация RTK, предваряющая развитие событий внутри клетки, приводит к связыванию SH2-домена адапторного белка — GRB2 (Growth Factor Receptor bound 2) — на фосфорилированном остатке тирозина активированной RTK. Помимо SH2-домена, GRB2 содержит также два SH3-домена, имеющих сродство к взаимодействию с богатыми пролином участками белка, который гомологичен белку плодовой мушки Drosophila — SOS (son of sevenless) — и потому у млекопитающих данный белок также имеет название SOS. Этот белок является фактором обмена гуаниновых нуклеотидов и опосредованно (с помощью одного из Ras-белков: HRas, KRas, NRas) катализирует обмен ГДФ на ГТФ. Необходимость GRB2 для активации Ras и митогенного эффекта МАРК доказана экспериментально. Также совместная инъекция GRB2 и HRas в покоящиеся фибробласты ведет к синтезу ДНК, чего не наблюдается при инъецировании отдельно GRB2 или HRas. Инъекция антител против GRB2 препятствует вступлению клеток в S-период клеточного цикла и перестройке клеточного цитоскелета после обработки их EGF или PDGF. GRB2 связывается с помощью своего SH2-домена не только с фосфотирозином активированной рецепторной тирозинкиназы, но и с фосфотирозином адапторного белка SHC, фосфотирозинфосфатазой SHP-2 и химерным белком BCR-Abl.
В ГТФ-связанной форме белки Ras способны активировать и другие протеины. Среди важнейших эффекторов Ras можно выделить фосфатидилинозитол-3-киназу (PI3K), фактор обмена Ral (RalGEF) и фосфолипазу С (PLC). Таким образом, с помощью Ras-протеинов происходит активация нескольких сигнальных путей, неразрывно связанных между собой. Ras регулируют не только пролиферацию клеток, но и клеточную миграцию, дифференцировку, ангиогенез и контролируют препятствующие апоптозу механизмы.
Самым известным эффектором Ras является серин-/треонинкиназа B-Raf, которая ведет к запуску классического пути МАРК. Решающим моментом для активации В-Raf-киназы является не связывание на Ras-GTP, а перемещение на внутреннюю поверхность плазматической мембраны. В экспериментальном исследовании ещё 1994 года было подтверждено, что если заякорить В-Raf-протеин в мембране с помощью липидного «якоря», то он будет активным и без взаимосвязи с Ras-GTP. Поэтому считается, что В-Raf взаимодействует на внутренней поверхности мембраны с каким-либо фактором белковой или липидной природы (каким — пока неизвестно), что и становится условием для активации белка. Для завершения активирования белок должен быть также фосфорилирован, за что, вероятно, отвечает Src-киназа. B-Raf-киназа фосфорилирует и приводит в активное состояние киназы МЕК 1 и 2, которые, в свою очередь, необходимы для активирования киназ ERK 1 и 2. ERK 1 и 2, будучи активными, способствуют фосфорилированию и активации многочисленных факторов транскрипции, как, например, Elk-1, fos, Myk. Факторы транскрипции связываются со специфическими повторами на молекуле ДНК и инициируют процесс транскрипции необходимых генов, например, CCND1, FOS. Далее синтезированные в ходе трансляции продукты данных генов опосредуют развитие биологической реакции клетки на активирование сигнального пути.
Схема классического сигнального пути МАРК.
МАРК в клетках опухоли
Усиленная активация пути МАРК может быть вызвана мутациями в генах RTK, а также HRas, KRas, NRas, BRAF1, NF1. Однако активирующие мутации в генах, чьи продукты принимают участие в проведении сигнала внутрь клетки, могут быть скомпенсированы, поскольку, как правило, если один из участков сигнального пути изменён вследствие мутации, то остальные остаются нетронутыми. В качестве примера можно привести исследование клеток папиллярного рака ЩЖ. Две трети карцином несли активирующие мутации или в гене рецепторной тирозинкиназы RET, или KRAS, или BRAF1. И только в очень небольшом проценте опухолей были обнаружены мутации в двух различных генах сигнального пути. Почему в одной опухоли поврежден один ген, а в другой — иной ген одного и того же сигнального пути, пока не совсем понятно. Одно из предположений опирается на иерархию в пределах пути и мутаций. МАРК может разветвляться на нескольких уровнях, и чем выше по иерархии сигнального пути лежит изменённый белок, тем более вероятно последующее отклонение. Следуя этому предположению, мутация в генах Ras будет иметь более обширные и выраженные последствия для клетки, чем, например, мутация в гене BRAF. Следовательно, мутации в генах Ras более «выгодны» потенциальной опухолевой клетке и встречаются чаще, чем мутации на функционально нижерасположенных уровнях.
Белки Ras закреплены на клеточной мембране с внутренней стороны посредством жирной кислоты, ковалентно связанной с карбокситерминальным концом белка. И это семейство белков можно сравнить с молекулярным переключателем МАРК. В ГДФ-связанном состоянии белок неактивен, и дальнейшая передача сигнала не осуществляется. Обмен ГДФ на ГТФ и сопряжённый с этим переход неактивной формы Ras в активную катализируется SOS (SOS1, SOS2) — ферментом, относящимся к группе факторов обмена (GEF — Guanine Exchange Factors). Активная форма Ras может проявлять собственную невысокую ГТФ-азную активность и гидролизовать связанный ГТФ до ГДФ, тем самым самоинактивируясь. Этот процесс довольно длителен, но он многократно ускоряется ГТФ-аза-активирующими белками, например, p120GAP (p120 GTPase activating Protein) и нейрофибромином (NF1GAP). Мутации в генах онкопротеинов Ras ведут к предотвращению реакции гидролиза, вследствие чего сигнальный путь длительное время остаётся активным.
Семейство Rho-ГТФаз и их участие в развитии опухолевого процесса
Наряду с Ras существуют и другие ГТФ-связывающие белки, которые с помощью подобных биохимических механизмов активируются или инактивируются и имеют различные задачи. И среди маленьких ГТФ-аз хотелось бы упомянуть семейство Rho, представители которого играют ключевую регуляторную роль в сигнальной передаче от цитокиновых рецепторов, а также в организации актинового цитоскелета клетки и микротрубочек. В реализации процесса метастазирования цитоскелет имеет большое значение, поскольку помимо механической стабилизации клеточной архитектуры, сенсорные функции и транспорт внутри клетки необходимы для инвазивной активности клетки. С помощью динамической сборки и разборки структур цитоскелета клетка может активно передвигаться. Rho ГТФ-азы активны в ГТФ-связанном состоянии, а в ГДФ-связанной форме, соответственно, не проявляют функциональной активности. GEF-белки катализируют обмен ГДФ на ГТФ, опосредуя активность Rho ГТФ-аз, а белки GAP стимулируют инактивацию Rho-белков. Активные Rho ГТФ-азы располагаются на клеточной мембране, где, связывая специфические эффекторные белки, они обеспечивают последующую трансдукцию сигнала, вызывая перегруппировку цитоскелета. Тот факт, что на сегодняшний день идентифицировано около 80-ти типов GEF и 70-ти — GAP, что количественно превосходит Rho ГТФ-азы, коих имеется около 20-ти, может говорить о необходимости строгого контроля регуляции локальной активности Rho, чтобы предотвратить ошибочную передачу исходного сигнала.
В опухолевых клетках активность Rho ГТФ-аз ненормально высока, что может быть обусловлено изменённой генной экспрессией или нарушенной функцией регуляторов, в меньшей степени — активирующими мутациями в самих Rho ГТФ-азах. Среди RhoGAP-белков особенно выделяют семейство DLC-белков (deleted in liver cancer), поскольку именно их инактивация является наиболее частым изменением Rho-регуляторов при развитии опухолевых процессов. При некоторых типах рака утрата DLC1 встречается настолько же часто, как и выпадение опухолевого супрессора р53. Вообще в геноме человека закодированы три изоформы DLC, имеющие цифровое обозначение от 1 до 3. DLC1-3 обладают схожей структурной организацией и регулируют активность малых ГТФ-аз RhoА и Cdc42. DLC1 является наиболее изученным представителем и был открыт в 1998 году как вероятный опухолевый супрессор в клетках гепатоцеллюлярной карциномы печени человека. Позже было установлено, что белок DLC1 отсутствует в клетках различных опухолевых образований (молочной железы, кишечника, лёгких, простаты) по причине инактивации соответствующего ему гена. Перестройка экспрессии DLC1 в клетках различных опухолевых линий, не обнаруживавших образование эндогенного DLC1, останавливала интенсивный рост клеток и дальнейшее развитие опухоли на модели мыши. Кроме того, обеспечение стабильной экспрессии DLC1 в клетках рака молочной железы человека привело к уменьшению миграции клеток in vitro и к сокращению клеточной инвазии in vivo.
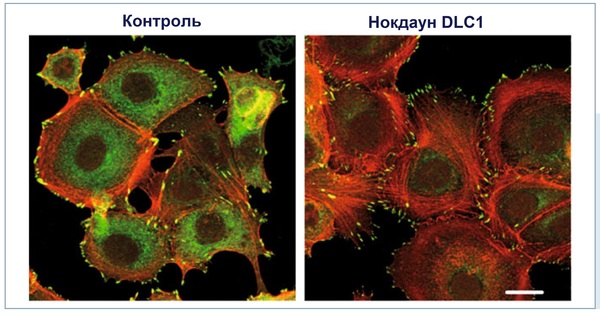
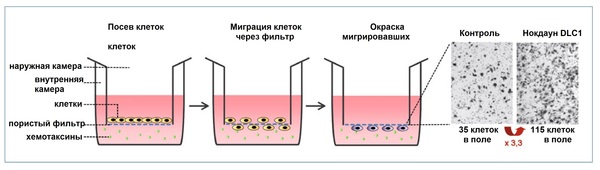
Сотрудниками лаборатории Института клеточной биологии и иммунологии Университета города Штуттгарта были исследованы последствия выпадения белка DLC1 из сигнального пути с помощью РНК-интерференции. С применением конфокальной иммунофлуоресцентной микроскопии было показано на примере клеток рака молочной железы, что «выключение» DLC1 вызывает усиленное образование т.н. активновых стрессовых волокон и фокальных адгезивных контактов. Это было сопряжено также с повышенной миграционной активностью раковых клеток, что было зафиксировано в анализе миграции клеток через мембрану, проведённом в специальных Transwell-культуральных планшетах, в которых можно моделировать хемотаксическую миграцию клеток через небольшие поры. Механистически увеличение миграционной активности может быть объяснено усилением Rho-опосредованной передачи сигнала как следствие утраты DLC1. А на примере использования клеток рака печени мыши была однозначно подтверждена функция DLC1 как опухолевого супрессора.
Образование стрессовых волокон и фокальных адгезивных контактов путем снижения экспрессии DLC1. Клеточный ответ на сниженную экспрессию DLC1 в линии опухолевых клеток MCF7 (клетки рака молочной железы) был получен после проведения РНК-интерференции. Представленные фотографии отражают результаты иммунофлуоресцентной микроскопии. Окраска адгезивных контактов произведена с помощью специфических антител к паксилину (зеленый цвет), окраска стрессовых волокон — с помощью фаллоидина (красный цвет).
Transwell-анализ для исследования хемотаксической миграции клеток. Нокаутированные по DLC1 клетки, а также клетки контрольной группы были посеяны на специальный планшет; их миграция через поры фильтра индуцирована наличием градиента сыворотки и коллагена. После этого мигрировавшие клетки были окрашены и подсчитаны.
Что же с другими членами семьи DLC? Несмотря на то, их характеристика составлена еще не в полной мере, их отсутствие отмечено в клетках многих опухолей. Также интересен тот факт, что, несмотря на схожесть структур отдельных изоформ DLC, их функции, тем не менее, не являются избыточными, а сами белки не обладают полностью взаимокомпенсирующим свойством. Об этом свидетельствует то, что утрата гена DLC1 приводит к летальному фенотипу у мышей, тогда как нокаутированные по гену DLC2 мыши остаются жизнеспособными. В связи с этим фактом довольно значительными представляются работы исследователей из Штуттгарта, поскольку в своих экспериментах им удалось также обнаружить специфичную для изоформы DLC3 функцию, заключающуюся в координации процессов внутриклеточного транспорта между отдельными компартментами клетки. Помимо этого, DLC3 осуществляет передачу сигналов от рецептора фактора роста EGFR (epidermal growth factor receptor) и выполняет функцию стабилизации в постоянных клеточных контактах. Утрата функции DLC3 в опухолевых клетках может, с одной стороны, привести к усилению сигналов в клетку от рецепторов ростовых факторов и, с другой стороны, стать причиной ослабления контактов между структурами эпителиальных тканей, что способствует как возникновению опухоли, так и её метастазированию.
На этом придётся подвести итоги. Сигнальных путей в клетке великое множество, мы взяли только несколько и пробежались по основным моментам. У вас уже наверняка возникло множество вопросов касательно путей, их компонентов и их функционирования в опухолевых клетках. В ходе написания последующих очерков по сигнальным путям будут приложены все усилия, чтобы ответить на ваши вопросы и чуть шире приоткрыть для всех интересующихся внутренний мир клетки.
Вспомогательные понятия и аббревиатуры
Автор: Александра Стеценко
Источники:
C. Wagener, O. Müller Molekulare Onkologie: Entstehung, Progressing, klinische Aspekte, 2010
A. Nordheim, R. Knippers Molekulare Genetik, 2015
Lowenstein, Daly, Batzer et al. The SH2 and SH3 Domain-Containing Protein GRB2 Links Receptor Tyrosine Kinases to ras Signaling
Van der Geer, Hunter, Lindberg Receptor protein-tyrosine kinases and their signal transduction pathways
Wittinghofer, Pai The structure of Ras protein: a model for a universal molecular switch
Noll et al. Rho-Signalgebung in der Tumorentstehung und -progression, BioSpektrum, 04.2016
Braun, Hendrick, Eisker, Schmid et al. The Rho-specific GAP protein DLC3 coordinates endocytic membrane trafficking
Braun, Olayioye Rho regulation: DLC proteins in space and time
Похмелье. Чем вызвано. Механизмы влияния на органы.
В прошлом посте был разобран метаболизм алкоголя и что он делает во время алкогольного опьянения, в этом посте будет описано состояние, которое почти всегда сопровождает чрезмерный прием алкоголя- похмелье. Похмелье известно человечеству с древних времен, еще авторы древнего Египта и Греции писали о нем в своих манускриптах. Однако, несмотря на наше длительное знакомство, похмелье было обделено вниманием ученых и медиков, поэтому многие процессы, сопровождающие похмельный синдром, еще не до конца изучены. Например, исследователи еще не до конца определились с тем, каким образом похмелье влияет на когнитивные способности человека и его сознательные движения.
Что такое похмелье? Похмелье характеризуется множеством неприятных физических и психических симптомов, которые появляются после чрезмерного употребления алкоголя. Физические симптомы похмелья включают в себя усталость, слабость, головную боль, повышенную чувствительность к свету и звукам, покраснение глаз, мышечные боли, жажду, тошноту и рвоту. Похмельный синдром сопровождает активация симпатической нервной системы, что обуславливает повышение давления, чувство сердцебиения, тахикардию, тремор конечностей и обильный пот. Психические («умственные») симптомы включают головокружение, расстройства когнитивных функций, плохое настроение, чувство беспокойства и раздражительность. Данные симптомы могут варьироваться в зависимости от человека и от того, что он пил. Похмельный синдром во многом зависит от вида и количества выпитого алкогольного напитка. Обычно похмелье наступает через несколько часов после прекращения приема алкоголя, когда концентрация алкоголя в крови (КАвК) начинает падать. Симптомы похмелья достигают своего максимума, когда концентрация алкоголя в крови снижается почти до нуля, и могут длиться до 24 часов.
Среди врачей и ученых бытует мнение, что похмелье является мягким вариантом алкогольной абстиненции (алкогольная ломка у алкоголиков). Главное отличие первого заключается в том, что похмелье может развиться уже после однократного приема алкоголя, в то время как абстиненция появляется обычно после длительного запоя. Другие различия между похмельем и абстиненцией включают более короткий период плохого самочувствия (т.е. пару часов при похмелье против нескольких дней при абстиненции), а также отсутствие галлюцинаций и припадков при похмелье (т.е. белой горячки).
Физиологические факторы, способствующие развитию похмелья. Симптомы похмелья могут быть вызваны различными причинами, такими как прямые физиологические эффекты алкоголя на мозг и другие органы; эффекты от удаления алкоголя из этих органов после алкогольного воздействия (т.е. абстиненция), физиологические эффекты соединений, полученных в результате алкогольного метаболизма, особенно ацетальдегид; и неалкогольные факторы, такие как токсические воздействия других биологически активных соединений, содержащихся в напитках, прием некоторых медикаментов и наркотических средств одновременно с алкоголем, недостаточный прием пищи и нарушения нормального режима сна, а также индивидуальные особенности (темперамент, личная и семейная история алкоголизма).
Непосредственные эффекты алкоголя. Алкоголь непосредственно способствует развитию похмелья.
Дегидратация и электролитный дисбаланс. Алкоголь увеличивает выделение мочи (является диуретиком). Потребление 50г алкоголя в 250мл воды (что равносильно по крепости портвейну) является причиной выведения из организма от 600 до 1000 мл воды в течении ближайших нескольких часов. Это происходит потому, что алкоголь способствует продукции мочи путем ингибирования антидиуретического гормона (АДГ) (ответственен за задержку воды и электролитов в крови) выделения из гипофиза. В свою очередь, снижение уровня АДГ препятствует реабсорбции воды в почках и тем самым увеличивает продукцию мочи. Обильное потоотделение, рвота и диарея также обычно сопутствуют похмелью, и эти состояния могут также приводить к потере жидкости и электролитному дисбалансу. Симптомы легкой или даже средней дегидратации включают жажду, слабость, сухость слизистых, слабость и чувство головокружения- все это обычно проявляется во время похмелья.
Нарушения со стороны ЖКТ. Алкоголь непосредственно раздражает желудок и кишечник, является причиной воспаления слизистой оболочки желудка (гастрита) и задерживает опустошение желудка, особенно этим эффектом обладают напитки с высоким содержанием алкоголя (более 15 процентов). Высокие уровни потребления алкоголя могут вызвать жировую дистрофию печени (стеатоз), которая заключается в накоплении жиров, называемых триглицеридами и их производных (свободные жирные кислоты) в печеночных клетках (гепатоцитах). К тому же, алкоголь повышает выделение желудком кислоты, а также секрецию поджелудочной железы и кишечника. Изменение микрофлоры полости рта и ЖКТ также играет важную роль в развитии похмелья, особенно при его частом потреблении. Дизбиоз (дизбактериоз), вызванный приемом алкоголя, характеризуется увеличением количества бактерий, способных вызвать воспалительные реакции, и уменьшение тех, которые им препятствуют. Кроме того, дизбиоз оказывает влияние на процессы пищеварения, нарушая переваривание и всасывание различных веществ. Патогенная микрофлора, размножившаяся на фоне гибели нормальной микрофлоры кишечника, начинает выделять различые токсины, которые также пагубно влияют на функционирование организма. Часть или все эти факторы могут вызвать боли в животе, тошноту и рвоту, что часто встречается при похмелье.
Низкий сахар в крови. Некоторые нарушения метаболизма печени и других органов возникают в ответ на присутствие алкоголя в организме и могут привезти к снижению уровнюя сахара в крови (гипогликемия). Метаболизм алкоголя приводит к жировой дистрофии печени и нарастанию промежуточного продукта метаболизма, молочной кислоты, в жидкостях организма (т.е. развивается лактоацидоз). Оба этих механизма могут ингибировать продукцию глюкозы.
Алкоголь-индуцированная гипогликемия как правило возникает у алкоголиков, которые находятся в состоянии запоя и при этом мало питаются. В такой ситуации длительное употребление алкоголя в паре вместе со скудным поступлением в организм питательных веществ, не только понижает выработку глюкозы, но также истощает запасы гликогена в печени, который идет на образование глюкозы, тем самым вызывая гипогликемию. Поскольку глюкоза является основным источником энергии для мозга, гипогликемия может вызвать такие симптомы похмелья как усталость, слабость и нарушения настроения. Диабетики в частности особенно чувствительны к алкоголь-индуцированным изменениям глюкозы в крови.
Нарушение сна и других биологических ритмов. Хотя алкоголь обладает седативными эффектами и может способствовать засыпанию, усталость, испытываемая во время похмелья, является результатом патогенного влияния алкоголя на сон. Сон, индуцированный приемом алкоголя, может быть короче и худшего качества из-за синдрома отдачи (ухудшение состояния организма после снижения концентрации этанола) после падения КАвК, сопровождающее бессонницу. Более того, когда прием спиртных напитков приходится на вечер или ночь (как это часто бывает), и может совпадать со временем, когда человек обычно спит, то уменьшение обычного времени сна также ухудшает состояние организма. Алкоголь также нарушает нормальные модели сна, снижая время, потраченное быстрофазовый сон (REM- сон, в котором мы видим сны) и увеличивая время на медленнофазовый. В добавок, алкоголь расслабляет мышцы грудной клетки, в результате чего может появиться или усилиться уже существующий храп и, возможно, периодическая остановка дыхания (апноэ).
Алкоголь нарушает многие биологические ритмы, что проявляется в период похмелья. Например, алкоголь нарушает нормальный 24х-часовой (циркадный) ритм температуры тела, снижая температуру тела при интоксикации и ненормально повышая ее во время похмелья. Алкогольная интоксикация также влияет на циркадную ночную секрецию гормона роста, который очень важен для роста костей и синтеза белков. Алкоголь индуцирует выделение аденокортикотропного гормона (АДКТ) из гипофиза, который стимулирует выделение кортизола, гормона, играющего важную роль в метаболизме углеводов и стресс реакциях; алкоголь тем самым нарушает нормальные циркадные подъемы и падения уровня кортизола. В общем и целом, нарушения циркадных ритмов, вызванных алкоголем, сходны с теми нарушениями, которые возникают при перелете из одного часового пояса в другой, что может объяснить некоторые симптомы похмелья.
Алкоголь и головная боль. В крупном эпидемиологическом обследовании головной боли в Дании лиц от 25 до 64 лет, частота встречаемости похмельных головных болей составила 72 процента от всех головных болей, делая этот тип головной боли самым распространенным. Алкогольная интоксикация может вызвать вазодилатацию (расширение сосудов), которая в свою очередь путем увеличения выхода жидкости из сосудов, повышает черепно-мозговое давление и способно головные боли. Алкоголь оказывает эффекты на ряд нейромедиаторов и гормонов, участвующих в патогенезе головных болей, это гистамин, серотонин и простагландины. Однако, этиология похмельной головной боли до конца остается неизвестной.
Влияние алкоголя на ЦНС. Как уже было сказано выше алкоголь влияет на нейромедиаторные системы головного мозга, нарушая их функционирование, чтобы лучше себе это представить можно взять гипертрофированный вариант похмелья – алкогольную абстиненцию, и на примере нее понять, что происходит в мозге.
Синдром алкогольной абстиненции (АА синдром) сопровождает прекращение длительного приема алкоголя, во время которого происходят компенсаторные изменения в ЦНС. Эти изменения включают в себя повреждения двух типов рецепторов, встроенных в мембрану нервных клеток. Один тип рецепторов имеет сродство к одному важному нейромедиатору, который называется гамма-аминомаслянная кислота (ГАМК), а другой тип связывается с другим нейромедиатором, глутаматом. ГАМК и глутамат очень важны в регуляции активности нервных клеток: ГАМК в организме в основном оказывает тормозное влияние, а глутамат возбуждающее.
После длительного приема алкоголя в организме снижется количество и чувствительность ГАМК-рецепторов и увеличивается количество и чувствительность глутаматных рецепторов, это происходит для того чтобы нивелировать алкогольный седативный эффект. Когда алкоголь удаляется из организма, ЦНС и участки нервной системы, которые координируют ответ на стрессовые воздействия (симпатическая нервная система), остаются в несбалансированном перегруженном (“overdrive”) состоянии. Симпатическая нервная система находится в гиперактивном состоянии, что может вызывать тремор, обильное потоотделение и тахикардию, все это встречается как при похмелье, так и при АА синдроме.
Эффекты метаболитов алкоголя. Метаболизм алкоголя был описан предыдущем посте, посвященному этой теме. Если вкратце, то алкоголь подвергается двухэтапному метаболизму. Сначала фермент АДГ превращает алкоголь в промежуточный продукт, ацетальдегид; затем второй фермент АЛДГ метаболизирует адетальдегид в ацетат. Ацетальдегид химически активное вещество, которое связывается с белками и другими важными соединениями. В высоких концентрациях, он оказывает токсический эффекты, такие как частый пульс, обильное потоотделение, гиперемия кожи, тошнота и рвота. У большинства людей АЛДГ метаболизирует ацетальдегид быстро и эффективно, поэтому этот метаболит не накапливается в высоких концентрациях, хотя небольшое количество присутствует в крови во время алкогольной интоксикации. У некоторых людей, однако, генетический вариант АЛДГ приводит к накоплению ацетальдегида. Эти люди обычно краснеют, обильно потеют и чувствуют себя больными после небольших доз алкоголя.
Факторы, несвязанные с алкоголем. Есть ряд вещей, способствующий развитию похмелья, помимо самой молекулы этанола.
Конгенеры. Многие алкогольные напитки содержат небольшое количество других биологически активных соединений, в том числе и другие спирты. Эти компоненты известны как конгенеры (соединения, образующиеся одновременно с этиловым спиртом при сбраживании заторов), они участвуют в создании вкуса, запаха и внешнего вида алкогольного напитка. Конгенеры могут быть получены вместе с этанолом во время ферментации, генерируются в процессе настойки и обработки, путем разрушения органических компонентов алкогольных напитков или добавления их во время производственного процесса. Считается, что конгенеры могут участвовать в развитии интоксикации и последующего похмелья. Показано, что напитки, состоящие по большей части из чистого этанола, такие как водка или джин, вызывают менее выраженные похмельные эффекты, чем те напитки, которые содержат большое количество конгенеров, такие как виски, бренди или красные вина. Тем не менее похмелье также может возникать и при введении чистого алкоголя.
Один из конгенеров, замешанный в развитии эффектов похмелья, это метанол, который также является спиртом и встречается в алкогольных напитках наряду с этанолом. Эти два соединения немного различаются химической структурой, метанол содержит на один атом углерода и два атом водорода меньше, чем этанол. Часть ферментов, метаболизирующих этанол, АДГ и АЛГД, также метаболизируют и метанол; однако продукты метаболизма метанола (формальдегид и муравьиная кислота) чрезвычайно токсичны и в высоких концентрациях могут вызвать слепоту и даже смерть.
Крепкие спиртные напитки, которые часто вызывают развитие сильного похмелья, такие как бренди и виски, содержат высокие концентрации метанола. Более того, в экспериментах с людьми, которые потребляют красные вина, содержащие 100 миллиграмм на литр метанола, было показано, что повышенный уровень метанола в крови встречается через несколько часов после того, как этанол метаболизируется, что соответствует времени проявления симптомов похмелья. Метанол остается до тех пор, пока уровень и количество этанола в крови не снизится, потому что этанол полностью подавляет метаболизм метанола. Факт, что введение этанола во время похмелья снимает его симптомы, подтверждает предположение о участии метанола в развитии похмелья, учитывая способность этанола блокировать метаболизм метанола, в результате чего скорость образования формальдегида и муравьиной кислоты резко снижается.
У некоторых людей развивается головная боль после питья красного вина, но не развивается после белого вина или водки. Недавнее исследование показало, что красное вино, но не белое вино или водка, может повышать уровень серотонина и гистамина в плазме крови. Специфические агенты в вине ответственные за повышение уровней этих медиаторов неизвестны. Повышенные уровни серотонина и гистамина в плазме могут вызвать головные боли у ряда людей.
Индивидуальные факторы. Некоторые данные свидетельствуют о том, что симптомы похмелья во многом зависят от индивидуальных характеристик, таких как нейротизм (черта личности, характеризующаяся эмоциональной неустойчивостью, тревогой, низким самоуважением), гнев и защитность. Негативные моменты и чувство вины из-за приема алкоголя также способны влиять на силу похмелья.
Лечение похмелья. Было описано много подходов в лечении для предотвращения, сокращения длительности и уменьшения тяжести симптомов похмелья. Часть методов лечения относится к народной медицине. Однако, немногие подходы прошли соответствующие исследования. Консервативное лечение представляет собой лучше лечение. Время- наиболее важный компонент, потому что симптомы похмелья обычно прекращаются через 8-24 часа.
Внимательность к количеству и качеству принимаемого алкоголя может дать значительный эффект для предотвращения похмелья. Похмельные симптомы появятся с меньшей вероятностью, если человек пьет небольшое, неопьяняющее количество алкоголя. Даже среди людей, которые пьют до опьянения, те, кто потребляют меньшее количество алкоголя имеют меньший шанс развития похмелья в сравнении с теми, кто пьет большие дозы.
Тип потребляемого алкоголя также может оказать существенное влияние на развитие похмелья. Алкогольные напитки, которые содержат мало конгеренов (например, чистый этанол, водка, джин) связаны с менее выраженным похмельем, чем напитки, которые содержат большое количество конгеренов (например, бренди, виски и красное вино).
Другие вмешательства могут уменьшить интенсивность похмелья, но они не изучены в должной степени. Потребление фруктов, фруктовых соков или других фрукто содержащих продуктов может уменьшить интенсивность похмелья. Также продукты, содержащие углеводы, такие как тосты или крекеры, могут помочь при низком уровне сахара у людей с гипогликемией и могут облегчить тошноту. В добавок, адекватный сон может облегчить усталость, связанную с недостатком сна, а питье безалкогольных напитков во время и после приема алкоголя может предотвратить дегидратацию вызванную алкоголем.
Некоторые лекарства могут облегчить симптомы похмелья. Например, антациды могут облегчить тошноту и гастрит. Аспирин и другие НПВС (ибупрофен или напроксен) могут уменьшить головную и мышечную боль связанные с похмельем, но должны применяться с осторожностью, особенно если есть боли в верхней части живота и тошнота. Противовоспалительные средства могут самостоятельно раздражать желудок, что может вызвать алкоголь индуцированный гастрит. Хотя ацетаминофен (парацетамол) является распространенной альтернативой аспирину, его не следует использовать во время похмелья, потому что метаболизм алкоголя усиливает токсическое действие ацетаминофена на печень.
Пропанолол, бета-адреноблокатор, используют для купирования высокого кровяного давления и головной боли по типу мигрени, снижает симпатическую гиперактивацию при АА синдроме; однако, был проведен ряд исследований, который не показал эффективности пропанолола для ослабления симптомов похмелья, включаю головную боль. Антагонитсы серотониновых рецепторы, такие как ондансетрон и трописетрон, являются противорвотными средствами (т.е. контролируют тошноту и рвоту) и блокируют центральные эффекты алкоголя. Кофеин обычно используют для предотвращения усталости и недомогания связанные с состоянием похмелья.
Повторное введение алкоголя также может облегчить состояние, но дополнительный прием алкоголя может только усилить токсическое действие алкоголя, принятого в прошлый раз и может усилить вероятность частого выпивания, поэтому люди, испытывающие похмелье должны избегать частых приемов алкоголя.
На сегодняшний день проводится ряд исследований, направленных на поиск лекарственных средств, которые могли бы помочь лечении похмелья. Например, Jacqueline Iversen (Sen-Jam Pharmaceutical, USA) и его команда изучают препарат под кодовым названием JMI-001, который необходимо принимать перед приемом алкоголя. Препарат является одновременно и НПВС, и блокатором H1 гистаминновых рецепторов, что дает возможность препарату предотвращать такие симптомы похмелья, как головная боль, жажда и усталость. Также описан целый ряд трав и других продуктов природного происхождения, которые так или иначе влияют на развитие похмелья.
Вывод. Похмелье, как и алкогольная интоксикация, влияет на многие системы органов и тканей, вызывая в них отклонения разной степени выраженности. Особенно страдают нервная система и ЖКТ, на них приходится наибольший удар. На сегодняшний день нет эффективных препаратов, которые могли бы избавить от похмелья, но в последние несколько десятилетий врачи и ученые активно принялись изучать это состояние, открывая каждый год новые его аспекты и механизмы, что приближает нас к тому дню, когда мы перестанем боятся того состояния, которое почти всегда нас ожидает после веселого вечера в компании с любимым напитком.
Немного об этаноле. Метаболизм этанола. Воздействие на мозг.
Вино, Водка, Пиво, Виски, Текила, Ягуар этот список можно продолжать бесконечно. У многих из нас есть свой любимый алкогольный напиток, который помогает расслабиться, провести весело время, решиться на какой-нибудь поступок и т.д. Все эти напитки объединяет их действующее вещество- этанол. Именно этанол обуславливает все знакомые нам эффекты алкогольного опьянения.
Попав в организм, этанол хорошо всасывается из ЖКТ. Всасывание начинается уже в полости рта и пищевода, около пятой части его абсорбируется в желудке (в стенке которого уже начинается его метаболизм), но большая часть этанола всасывается в двенадцатиперстной кишке. Этанол хуже всасывается, если желудок заполнен пищей, особенно обладающей обволакивающими свойствами (каши, картофель, масло, кисели и т.д.), сахар также тормозит всасывание алкоголя. Поэтому народная мудрость, что нужно всегда закусывать, имеет свой смысл. Углекислый газ же, который содержится в ряде алкогольных напитков, наоборот, ускоряет всасывание этанола в кишечник, так как стимулирует кровообращение и приток крови к кишечнику.
Попав в кровь, этанол попадает в различные органы и ткани и накапливается в них, особенно этанол любит мозг, яичники, яички, простату, в которых его концентрация бОльше, чем в других органах. Попав в мозг, алкоголь влияет на функции многих нейромедиаторных систем. Увеличивается выброс катехоламинов в синаптическую щель и тормозится их метаболизм, как следствие, повышается уровень дофамина в неостриатуме и центре положительного подкрепления гипоталамуса, а также повышает содержание норадреналина в гипоталамусе и ретикулярной формации среднего мозга обуславливая болеутоляющий эффект. При активации дофаминовых и адренорецепторов возникает эйфория, исчезает эмоциональная напряженность, что побуждает к повторному потреблению этанола. Усиливается ГАМК-ергическое торможение, что приводит к снятию возбуждения и оказывает успокаивающее действие. Одновременно угнетаются глутаматные NMDA-рецепторы. Нарушаются межнейронные возбуждающие воздействия и механизмы памяти, исчезают тяжелые воспоминания, снижаются болевые ощущения, возникает заторможенность. Следует заметить, что реакция организма на этанол строго индивидуальна и может сильно различаться от одного человека к другому.
Продукт окисления этанола ацетальдегид является источником образования норморфина, сальсолинола, метилтетрагидрокарболина, тетрагидроизохинолинов, которые, имея структурное сходство с морфином, действуют на опиоидные рецепторы, имитируют эффект опиоидных пептидов и обусловливают формирование психической зависимости от этанола.
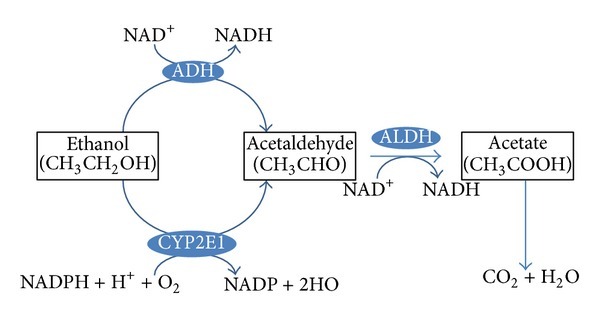
Около 10% этанола выводится организмом через легкие, почки и пот в неизменном виде, однако большая часть этанола оказывается вовлечена в процесс биотрансформации (обезвреживания) и окисляется до ацетальдегида. Этот процесс идет с помощью фермента алкогольдегидрогеназы, который в основном синтезируется в печени и желудочно-кишечном тракте.
При поступлении в организм значительных объемов этанола индуцируется другая система, которая его окисляет – цитохром P450 (CYP2E1). Особенно активно экспрессия CYP2E1 идет в центральной части печеночной дольки, это может также объяснить почему именно эти части долек больше всего подвержены токсическому действию алкоголя. CYP2E1 также превращает этанол в ацетальдегид. Также окисление этанола до ацетальдегида происходит с помощью каталазы, оксидаз и пероксидаз тканей.
Далее большая часть полученного ацетальдегида превращается в уксусную кислоту посредствам ацетальдегиддегидрогеназы, которая расположена в цитоплазме клеток и их митохондриях. Уксусная кислота окисляется до углекислого газа и воды с образованием энергии, промежуточные продукты метаболизма уксусной кислоты участвуют в синтезе жирных кислот и холестерина. Все перечисленные ферменты наиболее активны именно в гепатоцитах, поэтому наибольший токсический эффект этанола и продуктов его метаболизма приходится на эти клетки. В других клетках организма процесс обезвреживания этанола идет не так интенсивно.
Этанол обладает высокой калорийностью — при сгорании в организме 100 г этилового спирта выделяется 710 кал. При этом следует помнить, что этанол не является питательным веществом, он не служит строительным материалом для формирования тканей, не депонируется и при этом обладает высокой токсичностью.
Похмелье в основном обусловлено действием продукта окисления этанола- ацетальдегида, который в несколько раз токсичнее этанола, а также обладает большей тропностью к нервным тканям, присоединение ацетальдегида к ферментам нарушает их функциональную активность и метаболизм таких эндогенных аминокислот, как глутаминовая кислота, ГАМК и глицин, что вызывает расстройства со стороны ЦНС в виде всем известной головной боли, чувства разбитости, заторможенности и т.д. Также в развитии похмельного синдрома не последнюю роль играет метаболический ацидоз (сдвиг pH крови в кислую сторону), что отражается на функции всех органов и тканей, а также сильная потеря организмом воды (дегидратация). Похмельный синдром сильно варьирует от вида алкогольного напитка, так как помимо этанола, они содержат еще целую кучу различных веществ (эфиры, сивушные спирты), каждое из которых воздействует на организм по-своему.
МГУ. МОЛЕКУЛЯРНАЯ БИОФИЗИКА. Лекция 6
Всем доброго времени суток, исключительно для популяризации науки, в соответствии со статьёй 1274 ГК РФ продолжаю выкладывать лекции с портала openedu, т.к. не все умеют скачивать, а смотреть онлайн не всегда удобно.
Автор курса - доктор биологических наук, профессор кафедры биофизики биологического факультета МГУ имени М.В. Ломоносова Георгий Владимирович Максимов.
Лекция 1.Часть 1. Специфика биологических молекул.
Лекция 1. Часть 2. Явления гравитации и инерции для биологических молекул.
Лекция 1. Часть 3. Роль теплового движения биологических молекул.
Части 1-3: http://my-files.ru/s7oh95
Лекция 2. Часть 1. Роль молекул воды для функционирования биологических молекул.
Лекция 2. Часть 2. Принципы молекулярного узнавания.
Лекция 2. Часть 3. Термодинамика биологических молекул.
Части 1-3:http://my-files.ru/jygech
Лекция 3. Часть 1. Физические взаимодействия в биологических молекулах (ковалентные и не ковалентные взаимодействия, водородные связи, гидрофобные взаимодействия.
Лекция 3. Часть 2. Причины разнообразия биологических молекул.
Лекция 3. Часть 3. Аминокислоты, классификация аминокислот.
Части 1-3: http://my-files.ru/3odyfz
Лекция 4. Часть 1. Белки – первичная структура; вторичная структура белка; третичная структура белка; четвертичная структура белка. Фолдинг молекулы белка.
Лекция 4. Часть 2. Нуклеиновые кислоты, структура и функции.
Лекция 5. Часть 1. Углеводы, структура и функции.
Лекция 5. Часть 2. Катализ и биокатализ. Специфика биокатализаторов и основные понятия химического катализа.
Лекции 4-5, Части 1-2: http://my-files.ru/uikru3
Лекция 6 Часть 1. Фермент-субстрантный комплекс и особенности функционирования ферментов.
Лекция 6. Часть 2. Стабилизация ферментами переходного состояния химических реакций. Первичные механизмы ферментативных реакций.
Части 1-2: http://my-files.ru/dajypa
Лекция 6. Часть 3. Биофизические механизмы ферментативного катализа.
Лекция 6. Часть 4. Электронно-конформационные взаимодействия молекул белка при ферментативном катализе.
Лекция 7. Часть 1. Термодинамика ферментативной реакции.
Лекция 7. Часть 2. Кинетика ферментативных реакций; регуляция ферментативной активности (температура, рН).
Лекция 7. Часть 3. Биофизика трансформации энергии: митохондрии и хлоропласты. Клеточное дыхание. Фотосинтез; фотосистемы и компоненты цепи переноса электронов в митохондрии.
Лекция 8. Часть 1. Мембрана. Состав и свойства.
Лекция 8. Часть 2. Биофизика транспорта ионов. Электро-химическим потенциал. Пассивный и активный транспорт ионов. Возбудимые и не возбудимые мембраны. Распространение возбуждения в клетках.
Лекция 8. Часть 3. Биоэлектрические потенциалы. Уравнение Нернста и уравнение постоянного поля Гольдмана-Ходжкина-Катца. Пассивные свойства мембраны.
Лекция 8. Часть 4. Потенциал покоя и потенциал действия в клетках.
Лекция 8. Часть 5. Липиды. Состав и строение молекул, самоорганизация молекул, мембрана (фазовые переходы, асимметрия, поверхностный заряд). - Белок- липидные взаимодействия.
Лекция 9. Часть 1. Нейрофизиологические свойства каналов нейрона.
Лекция 9. Часть 2. Биофизика межклеточной передачи электрического сигнала. Синаптические потенциалы.
Лекция 10. Часть 1. Молекулярные механизмы сокращения мышцы.
Лекция 10. Часть 2. Строение и свойства актина и миозина. Механизмы регуляции мышечного сокращения; Миозиновый и актиновый механизм регуляции мышечного сокращения.
Лекция 10. Часть 3. Электромеханическое сопряжение в мышцах. Механика мышечного сокращения.
Лекция 11. Биофизика рецепции.
Лекция 11. Часть 1. Передача сигнала в фоторецепторных клетках.
Лекция 11. Часть 2. Молекулярные механизмы обоняния и тактильного восприятия.
Лекция 11. Часть 3. Биофизика транспорта макромолекул.
Лекция 12. Часть 1. Биофизика действия электромагнитного излучения.
Лекция 12. Часть 2. Свободнорадикальные процессы.
Лекция 12. Часть 3. Ионизирующее излучение. Биологические факторы радиобиологического эффекта. Клеточная мишень при действии радиации.
Источник:https://courses.openedu.ru/courses
МГУ. МОЛЕКУЛЯРНАЯ БИОФИЗИКА. Лекции 4-5
Всем доброго времени суток, исключительно для популяризации науки, в соответствии со статьёй 1274 ГК РФ продолжаю выкладывать лекции с портала openedu, т.к. там видео не КЭШируется, а смотреть онлайн не всегда удобно.
Автор курса - доктор биологических наук, профессор кафедры биофизики биологического факультета МГУ имени М.В. Ломоносова Георгий Владимирович Максимов.
Лекция 1.Часть 1. Специфика биологических молекул.
Лекция 1. Часть 2. Явления гравитации и инерции для биологических молекул.
Лекция 1. Часть 3. Роль теплового движения биологических молекул.
Части 1-3: http://my-files.ru/s7oh95
Лекция 2. Часть 1. Роль молекул воды для функционирования биологических молекул.
Лекция 2. Часть 2. Принципы молекулярного узнавания.
Лекция 2. Часть 3. Термодинамика биологических молекул.
Части 1-3:http://my-files.ru/jygech
Лекция 3. Часть 1. Физические взаимодействия в биологических молекулах (ковалентные и не ковалентные взаимодействия, водородные связи, гидрофобные взаимодействия.
Лекция 3. Часть 2. Причины разнообразия биологических молекул.
Лекция 3. Часть 3. Аминокислоты, классификация аминокислот.
Части 1-3: http://my-files.ru/3odyfz
Лекция 4. Часть 1. Белки – первичная структура; вторичная структура белка; третичная структура белка; четвертичная структура белка. Фолдинг молекулы белка.
Лекция 4. Часть 2. Нуклеиновые кислоты, структура и функции.
Лекция 5. Часть 1. Углеводы, структура и функции.
Лекция 5. Часть 2. Катализ и биокатализ. Специфика биокатализаторов и основные понятия химического катализа.
Лекции 4-5, Части 1-2: http://my-files.ru/uikru3
Лекция 6 Часть 1. Фермент-субстрантный комплекс и особенности функционирования ферментов.
Лекция 6. Часть 2. Стабилизация ферментами переходного состояния химических реакций. Первичные механизмы ферментативных реакций.
Лекция 6. Часть 3. Биофизические механизмы ферментативного катализа.
Лекция 6. Часть 4. Электронно-конформационные взаимодействия молекул белка при ферментативном катализе.
Лекция 7. Часть 1. Термодинамика ферментативной реакции.
Лекция 7. Часть 2. Кинетика ферментативных реакций; регуляция ферментативной активности (температура, рН).
Лекция 7. Часть 3. Биофизика трансформации энергии: митохондрии и хлоропласты. Клеточное дыхание. Фотосинтез; фотосистемы и компоненты цепи переноса электронов в митохондрии.
Лекция 8. Часть 1. Мембрана. Состав и свойства.
Лекция 8. Часть 2. Биофизика транспорта ионов. Электро-химическим потенциал. Пассивный и активный транспорт ионов. Возбудимые и не возбудимые мембраны. Распространение возбуждения в клетках.
Лекция 8. Часть 3. Биоэлектрические потенциалы. Уравнение Нернста и уравнение постоянного поля Гольдмана-Ходжкина-Катца. Пассивные свойства мембраны.
Лекция 8. Часть 4. Потенциал покоя и потенциал действия в клетках.
Лекция 8. Часть 5. Липиды. Состав и строение молекул, самоорганизация молекул, мембрана (фазовые переходы, асимметрия, поверхностный заряд). - Белок- липидные взаимодействия.
Лекция 9. Часть 1. Нейрофизиологические свойства каналов нейрона.
Лекция 9. Часть 2. Биофизика межклеточной передачи электрического сигнала. Синаптические потенциалы.
Лекция 10. Часть 1. Молекулярные механизмы сокращения мышцы.
Лекция 10. Часть 2. Строение и свойства актина и миозина. Механизмы регуляции мышечного сокращения; Миозиновый и актиновый механизм регуляции мышечного сокращения.
Лекция 10. Часть 3. Электромеханическое сопряжение в мышцах. Механика мышечного сокращения.
Лекция 11. Биофизика рецепции.
Лекция 11. Часть 1. Передача сигнала в фоторецепторных клетках.
Лекция 11. Часть 2. Молекулярные механизмы обоняния и тактильного восприятия.
Лекция 11. Часть 3. Биофизика транспорта макромолекул.
Лекция 12. Часть 1. Биофизика действия электромагнитного излучения.
Лекция 12. Часть 2. Свободнорадикальные процессы.
Лекция 12. Часть 3. Ионизирующее излучение. Биологические факторы радиобиологического эффекта. Клеточная мишень при действии радиации.
Источник:https://courses.openedu.ru/courses