За Алхимию или Самый вкусный рецепт приготовления золота
Собственно говоря все, кроме может быть тех, кто лечится гомеопатическими препаратами, знают, что алхимия эта лженаука, которая существовала когда люди еще плохо шарили что к чему в науке и пытались получить то, чего, собственно, получить нельзя.
Лично мне, как и возможно много кому, запомнилось 2 вещи - они хотели создать Философский камень и превращать ртуть в золото.
Тему философского камня пока что оставим в покое, а вот превращение ртути в золото я бы и хотел обсудить.
Я честно говоря, пока не копнул поглубже, думал что это какой-то абсолютно бредовая и не реализуемая идея, примерно как превращение человека в кролика или наоборот. Что-то вроде было-бы круто почему бы и нет.
То же самое, что превратить медь в титан или олово в серебро.
Конечно, теоретически все мы знаем, что при помощи альфа и бэта распадов можно превратить любой элемент в любой другой. Но во-первых это надо его еще заставить распадаться (то есть сделать радиоактивным, или уже найти)где-то в природе), во-вторых заставить распадаться именно тем распадом, которым надо, и в-третьих, после того как окончательный элемент получится, нужно, чтобы он сам не распадался, а был стабильным.
Все эти мысли подсказывали мне, что такой череды удачных совпадений быть не может. И так я и думал, до тех пор пока не заглянул в таблицу Менделеева и еще кое-куда.
Рисунок 1. Фрагмент таблицы Менделеева и моя реакция на такое совпадение
Опа Опа! Оказывается золото и ртуть находятся рядом и для получения золота достаточно одного бэта-распада. Ну совпадение бывает, но вообще не плохо, у алхимиков не было таблицы Менделеева. Но после этого я решил что точно нужно глянуть какие бывают изотопы у ртути и как они любят распадаться.
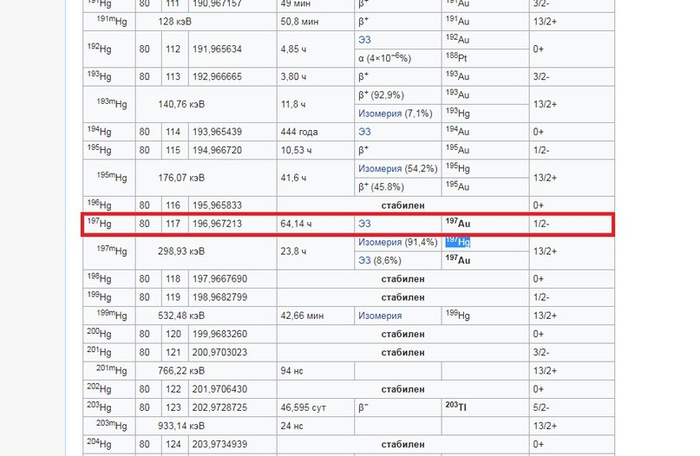
Рисунок 2. Список изотопов ртути.
И тут я тоже слегка удивился, оказывается существует изотоп ртути Hg-197, который имеет период полураспада всего 64 часа (если бы он был скажем миллион лет - нам бы не подошло-слишком долго ждать) и он при помощи электронного захвата (типа распада, при котором ядро захватывает с нижней орбитали электрон и один из протонов превращается в нейтрон) превращается в Au-197 - единственный стабильный изотоп золота.
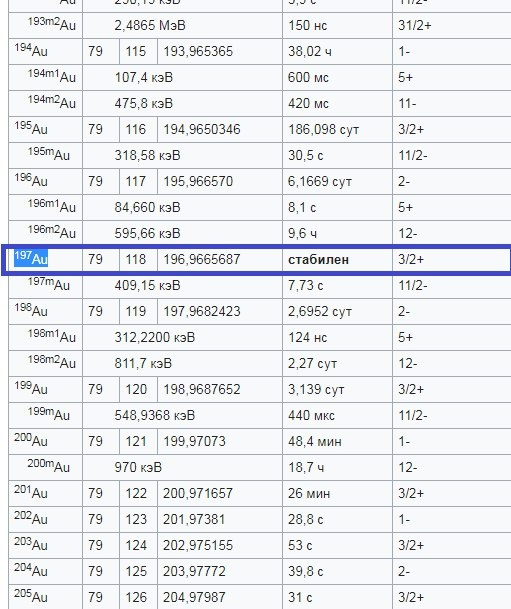
Рисунок 3. Список изотопов золота
Божечки-кошечки, вот это уже, по-моему, супер удача, потому как получившееся золото не будет радиоактивным, и получится достаточно быстро!
Ну ладно, а где взять то этот Hg-197, если он имеет такой маленький период полураспада, то в природе его, конечно не существует, потому что он взял да и распался весь. Однако сделать вещество радиоактивным можно, для этого нужен всего лишь источник нейтронов.
И о удача! Она сопутствует нам практически на каждом шагу - изотоп Hg-196 является стабильным, а значит существует в природе. И если ему скормить всего 1 нейтрон, при помощи нейтронного источника, то он превратится в так нам желанный Hg-197.
Есть конечно небольшое огорчение, если посмотреть на массу ртути в таблице Менделеева, там написано 200,59 (а масса в таблице берется как среднее значение массы изотопа с учетом его распространения в у нас на Земле). То есть это означает, что в произвольно взятом стакане ртути нам будут попадаться в основном изотопы с другой массой. И в самом деле Hg-196 содержится в нашем стакане всего 0,155%.
Не густо, конечно, но сколько есть.
Таким образом рецепт готов – можно записать его в нашу алхимическую кулинарную книжку.
«Как приготовить золото»
1) Возьмите много ртути, примерно в 650 раз больше, чем вы хотите золота.
2) Выделите из общей массы 196 изотоп Ртути.
3) Теперь достаньте нейтронный источник и облучайте им нашу ртуть, будьте осторожны - он активирует любое вещество до которого дотянется, и запросто может вас убить.
4)Довольно, не стоит пугаться того, что изотоп может захватить более одного нейтрона он превратиться просто в другой изотоп ртути причем стабильный(!!). Это означает, что спустя месяц в золото превратится 99,95% 197-й ртути. Плюс там, конечно будут другие стабильные изотопы ртути, и остатки радиоактивной 197-й ртути (0,05%), но все равно неприятно.
5) Поэтому отделяем химическим путем золото от ртути.
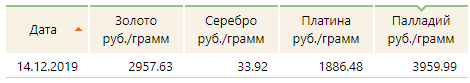
6)Вуаля! Вы великолепны – приятного аппетита. Золото готово – миссия алхимика выполнена. Вы сказочный...богач, но это не точно. Главное не вздумайте считать рентабельность такого способа.
Рисунок 4. Вы, после приготовления золота указанным способом
Источник: Cat_Cat. Автор: Максим Савин.
Личный хештег автора в ВК - #Савин@catx2
_______________________