Команда учёных из Университета Джорджии впервые в мире успешно провела редактирование генома рептилий. При помощи инструмента CRISPR-Cas9 специалисты создали четырёх ящериц-альбиносов.
"Рептилии очень плохо изучены с точки зрения репродуктивной биологии и эмбрионального развития. Пока что нет хороших методов манипулирования их эмбрионами, подобных тем, которые используются [в работе] с млекопитающими, рыбами или амфибиями. Насколько нам известно, ни одна другая лаборатория в мире до сих пор не производила генетически изменённых рептилий", – сообщил глава научной группы генетик Дуглас Менке (Douglas Menke).
Исследователи поясняют, что манипулирование генами с использованием технологии CRISPR обычно подразумевает введение специальных растворов для редактирования генов в недавно оплодотворённую яйцеклетку или одноклеточный эмбрион животного. Это должно вызвать мутацию, которая воспроизводится во всех последующих клетках.
Однако в случае с рептилиями есть несколько сложностей. Дело в том, что самки этих животных могут хранить сперму в своих яйцеводах в течение длительного времени после спаривания, что затрудняет точное определение момента оплодотворения.
Кроме того, после оплодотворения яйцеклетка покрывается гибкой оболочкой-скорлупой, и внутри отсутствует воздушное пространство, из-за чего учёным сложно манипулировать эмбрионом, не повредив его.
Но команде Менке всё же удалось обойти эти препятствия.
Для работы учёные выбрали вид ящериц под названием коричневый анолис.
Специалисты использовали инструмент CRISPR-Cas9 для микроинъекции белков CRISPR в незрелые яйцеклетки (ооциты), которые ещё находились в яичниках ящериц. В общей сложности исследователи обработали 146 ооцитов 21 рептилии, нацеливаясь на ген, ответственный за образование тирозиназы (фермент необходим для нормального синтеза пигмента меланина). Выключение этого гена приводит к альбинизму.
Затем оставалось только ждать естественного оплодотворения ооцитов.
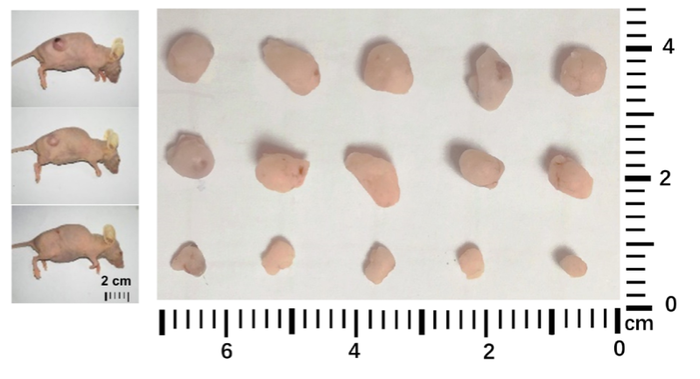
Через несколько недель команда поняла, что цель достигнута: в лаборатории появились четыре бледно-розовые ящерицы (как понятно из названия, обычные представители вида имеют коричневый окрас).
"Когда я увидела нашего первого детёныша-альбиноса, то испытала настоящее благоговение, – признаётся соавтор работы Эшли Расис (Ashley Rasys). – Больше всего меня приводит в восторг возможность использовать этот подход для многих других модельных систем рептилий, что положит начало будущим функциональным исследованиям".
Примечательно, что у ГМ-анолисов были обнаружены изменения в копиях генов тирозиназы, унаследованных не только от матери, но и от отца. Это означает, что белки CRISPR оставались активными в ооцитах матери гораздо дольше, чем ожидали учёные, и вызвали мутации в отцовских генах уже после оплодотворения.
"Это стало сюрпризом и позволило нам увидеть функциональные требования гена. По сути, нет необходимости разводить мутировавших животных, чтобы получить потомство, которое наследует изменённый ген от обоих родителей. Это сэкономит время [в будущих работах]", – отмечает Дуглас Менке.
Изучение генов коричневых анолисов, по мнению специалистов, может иметь важное значение для работы с генами человека. К примеру, ген тирозиназы играет ключевую роль в определённых процессах развития глаз. Эти механизмы общие у людей и анолисов, однако они отсутствуют у мышей и других животных, обычно используемых для биомедицинских исследований. Учёные, ищущие способы манипулировать этим геном для улучшения здоровья глаз человека, до сих пор не имели подходящей животной модели.
Добавим, что специалисты находят у животных генетические ключи к лечению многих болезней. Авторы проекта "Вести.Наука" (nauka.vesti.ru) ранее рассказывали о том, что слепая рыба-альбинос может научить людей восстанавливать ткани сердца после инфаркта и бороться с диабетом, голые землекопы помогут раскрыть секрет долголетия, а иглистые тритоны пригодятся для создания новых методов регенеративной медицины.