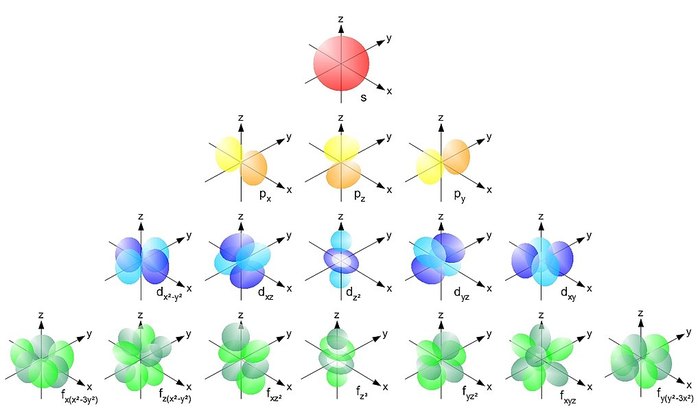
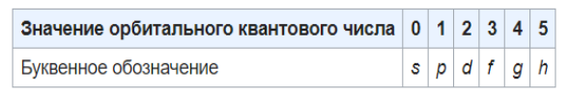
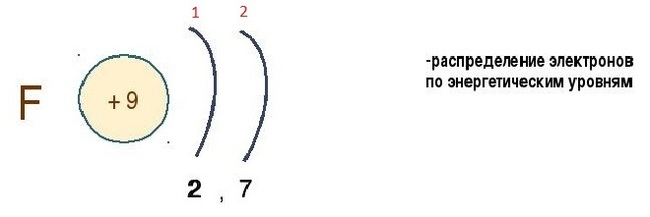Кванты: атом.
Атом - модели классической механики.
1) Первый важный прорыв в создании модели атома произошел к концу 19 века, когда ученый Джозеф Томпсон обнаружил отклонение лучей, испускаемых с катода. Они притягивались к положительно заряженным пластинам и отталкивались от отрицательно заряженных, то есть были заряжены отрицательно. Изучая частицы, Томпсон выяснил, что они в 1836 раз легче водорода, а также присутствуют во многих веществах. Так был открыт электрон - отрицательная частица, которая много легче водорода. Это открытие уже говорило о том, что атом возможно разделить и что каждый атом содержит в себе электрон.
Тогда Томпсон предложил такую модель атома - это некоторая положительно заряженная материя, в которую вкраплены электроны, выстроенные в кольцевые орбиты и способные свободно вращаться. Модель еще называют "пудинг с изюмом".
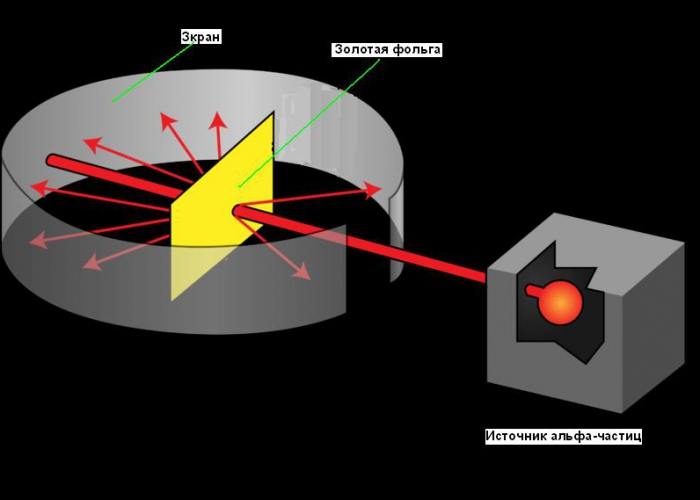
2) Модель Томпсона имела достаточно много логических оснований, поэтому ученик Томпсона, Эрнест Резерфорд, стремясь подтвердить гипотезу учителя и решил провести такой опыт: взял золотую фольгу (очень малой толщины, порядка микрометра) и облучил ее потоком альфа-частиц, то есть ядрами атомов гелия. Опыт проводили ученики Резерфорда - Гейгер и Марсден. Прозрачность атома для потока электронов было показано еще Ленардом, поэтому ожидалось, что практически все альфа-частицы пролетят сквозь фольгу - для регистрации пролетающих частиц Резерфорд расположил датчики вокруг фольги и наблюдал вспышки(сцинтилляции). Большая часть частиц действительно пролетала, угол рассеяния (отклонения) составлял не более 3 градусов от первоначальной траектории. Но была мизерная группа частиц, которая отлетала на угол до 150 градусов - из 8000 частиц находилась одна, отлетающая на угол больше 90 градусов. Почему же это происходило? Значит, был некоторый фактор, находящийся в центре, под действием которого легкие положительно заряженные альфа-частицы отлетали обратно. В любом случае, модель Томпсона была опровергнута.
Увиденное подтверждается снимками треков (следов) альфа-частиц в камере Вильсона - изредко треки заканчиваются вилками и изломами. Это происходит из-за взаимодействия ядер. Трек с вилкой показан на рисунке.
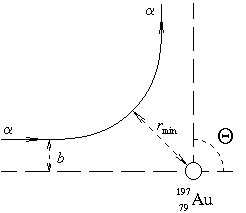
3) Спустя несколько лет Резерфорд пришел к выводу, что частицы, отлетающие на большие углы, появляются из-за взаимодействия с ядром атома. Дело в том, что между двумя заряженными частицами существует так называемая сила Кулона или кулоновское взаимодействие. Многие знают, что заряды одного знака отталкиваются, а разных знаков притягиваются - это обеспечивает как раз кулоновское взаимодействие. Поэтому когда положительно заряженная альфа-частица налетает на положительно заряженное ядро атома золота, то альфа-частица отклоняется - угол отклонения зависит от расстояния между атомами. Так Резерфордом была разработана планетарная модель атома - положительно заряженное ядро, содержащее большую часть массы, вокруг которого вращаются электроны. Расчеты показали, что ядро должно быть меньше атома по крайней мере в несколько тысяч раз. На рисунке показана траектория альфа-частицы, где b - расстояние между траекторией альфа-частицы и ядром золота. Траектория реального пролета представляет собой гиперболу.
Подобное рассеяние - отклонение, вызванное только электрическим полем одного ядра, без учета столкновений частиц - называется резерфордовским.
Несколькими годами ранее японский физик Нагаока предложил модель атома, построенную по аналогии с кольцами Сатурна - кольца удерживаются на орбите благодаря гравитационному взаимодействию массивного Сатурна с кольцами. Модель оказалась неверной, однако Нагаока предсказал два основных положения: ядро атома очень массивно и электроны удерживаются на орбитах благодаря кулоновскому взаимодействию.
С точки зрения классической электродинамики такая модель невозможна. Чтобы не смешивать все в одно, рассмотрю этот вопрос в следующем посте.
Планирую описать в своих постах основные законы атомной и ядерной физики. По всем вопросам - alexjuriev3142@gmail.com.
Литература: И.Е. Иродов "Квантовая физика. Основные законы", Д.В. Сивухин "Общий курс физики. Атомная физика".