Как работает иммунная система, лекция 4 ч. 10 (ч. 47)
ИТОГ
Молекулы ГКГ класса I функционируют как рекламные щиты, отображающие то, что происходит внутри клетки. Например, когда вирус заражает клетку, он использует биосинтетический механизм этой клетки для производства вирусных белков. Некоторые из этих белков расщепляются протеасомой на мелкие кусочки (пептиды) и переносятся транспортерами TAP в эндоплазматический ретикулум (ER). Там пептиды “опрашивают” молекулы класса I. Те из них, длина которых составляет около девяти аминокислот с соответствующими аминокислотами на концах, связываются в канавках молекул ГКГ класса I и транспортируются на поверхность клетки. Сканируя отображаемые там комплексы ГКГ I–пептида, Т-клетки-киллеры могут “заглянуть в клетку”, чтобы определить, была ли она инфицирована и нужно ли ее уничтожить.
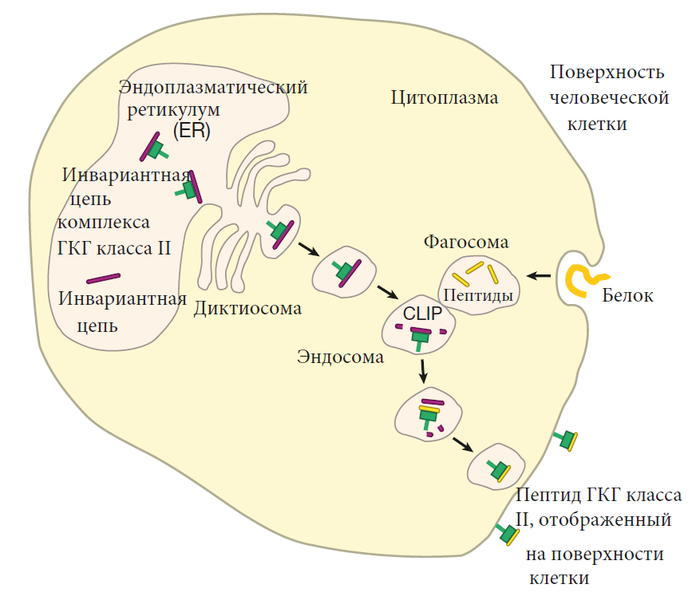
Молекулы ГКГ класса II также служат рекламными щитами, но они предназначены для предупреждения Т-клеток-помощников о том, что ведется битва. Молекулы класса II собираются в ER точно так же, как молекулы класса I, но поскольку белки с инвариантной цепью занимают свои связующие канавки, молекулы класса II не захватывают пептиды в ER. Вместо этого инвариантный цепной комплекс класса II транспортируется из ER в другой клеточный компартмент, называемый эндосомой. Там они встречаются с белками, которые приняты в клетку путем фагоцитоза и расщеплены ферментами на пептиды. Затем эти пептиды заменяют инвариантные цепи, которые защищали канавки молекул класса II, и комплексы ГКГ–пептид транспортируются на поверхность клетки для отображения в Т-клетках-помощниках. Благодаря этому хитроумному механизму молекулы класса II улавливают пептиды, полученные из белков, поступающих извне клетки, но избегают пептидов, полученных из белков, вырабатываемых внутри клетки.
Представление фрагментированных белков имеет ряд преимуществ по сравнению с представлением интактных белков. Во-первых, большинство вирусных белков обычно остаются скрытыми внутри инфицированной клетки и не обнаруживаются на поверхности клетки. Следовательно, эти белки никогда не бы не заметили Т-клетки-киллеры, если бы их не представляли молекулы ГКГ класса I. Кроме того, поскольку сворачивание белка может скрыть большие части белка от посторонних глаз, измельчение белка на мелкие пептиды выявляет множество потенциальных мишеней для Т-клеток, которые были бы недоступны в интактном белке. Следовательно, представление ГКГ значительно увеличивает вероятность того, что CTL распознают инфицированную клетку и что Т-клетки-помощники будут предупреждены о микробной атаке.
Молекулы ГКГ класса I и II чрезвычайно полиморфны, и у людей есть несколько генов для обоих классов молекул ГКГ. Следовательно, вполне вероятно, что ваши молекулы ГКГ будут способны выводить пептиды из большинства патогенов и что, по крайней мере, у некоторых людей в популяции будут молекулы ГКГ, способные выводить пептиды из любого патогена.
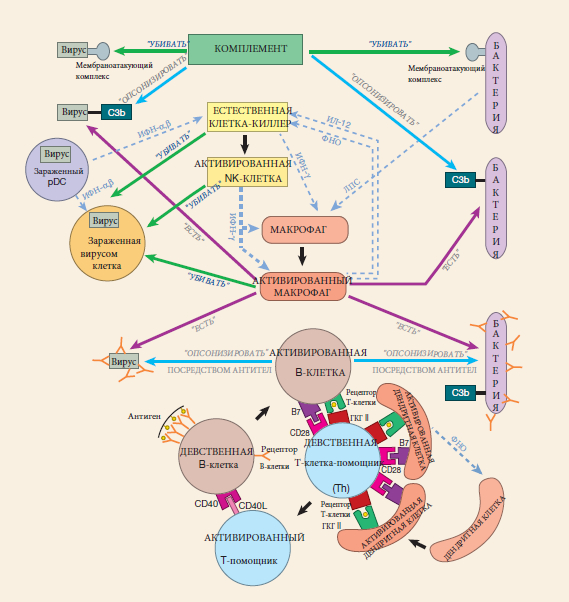
Антигенпредставляющие клетки — это особые клетки иммунной системы, которые могут обеспечивать представление ГКГ класса I и II, а также костимуляцию. Наиболее важной антигенпредставляющей клеткой на начальных стадиях атаки служит дендритная клетка, поскольку эта клетка может активировать первичные Т-клетки. Когда дендритная клетка обнаруживает сигналы опасности на месте сражения, она начинает созревать и мигрирует со своим грузом “боевого антигена” в близлежащий лимфатический узел. Там дендритная клетка использует молекулы ГКГ класса II для отображения фрагментов белков, которые она собрала в тканях, и молекулы ГКГ класса I для отображения фрагментов белков, продуцируемых вирусами или бактериями, которые, возможно, заразили дендритную клетку на месте сражения. Таким образом, дендритная клетка эффективно делает снимок того, что происходит на передовой, переносит его в место базирования Т-клеток, а затем выполняет свою функцию “показать и рассказать”, чтобы активировать Т-клетки.
Макрофаги, активируемые сигналами опасности, также могут функционировать как антигенпредставляющие клетки. Однако активированные макрофаги не попадают в лимфатические узлы для представления антигена. Они остаются в тканях и сражаются с вредителями. Следовательно, макрофаги наиболее полезны для представления антигена после активации приобретенной иммунной системы. В это время активированные макрофаги в тканях могут поддерживать активность опытных Т-клеток, продлевая время, в течение которого они эффективны в борьбе с вредителями.
Активированные В-клетки служат третьим типом антигенпредставляющих клеток, но опять же, эти клетки бесполезны для инициирования ответа приобретенной иммунной системы против нового вредителя. Причина в том, что прежде чем В–клетки смогут функционировать как антигенпредставляющие клетки, они должны сначала быть активированы Т-клетками-помощниками, а Т-клетки должны ждать активации дендритными клетками. Таким образом, В-клетки не “сертифицируются” как антигенпредставляющие клетки до тех пор, пока не сработает ответ приобретенной иммунной системы. Тем не менее, после активации В-клетки имеют большое преимущество перед дендритными клетками и макрофагами: В-клетки могут использовать свои рецепторы в качестве “сборщиков антигена” для концентрации небольших количеств антигена для представления Т-клеткам-помощникам. Следовательно, относительно поздно при начальной инфекции или рано при последующей инфекции тем же вредителем В-клетки играют важную роль в качестве антигенпредставляющих клеток.
Вопросы для размышления
1. Приведите несколько причин, по которым представление антигена молекулами ГКГ класса I важна для функционирования приобретенной иммунной системы.
2. Почему представление антигена молекулами ГКГ класса II имеет смысл?
3. Опишите различные роли, которые активированные дендритные клетки, активированные макрофаги и активированные В-клетки играют в представлении антигена во время течения инфекции.
4. В течение своей жизни дендритные антигенпредставляющие клетки могут быть “пробоотборниками”, “путешественниками” и “докладчиками”. Опишите, что они делают на каждом из этих трех этапов.
5. Некоторые пептиды представлены более эффективно, чем другие. Какие факторы влияют на эффективность представления молекулами ГКГ класса I и II?
Перевод книги LAUREN SOMPAYRAC "HOW THE IMMUNE SYSTEM WORKS", продолжение следует.