zlu4ka
Просто о химии. От установления делимости атома к планетарной модели Бора-Резерфорда.
Эксперименты по установлению делимости атома.
Основной экспериментальной предпосылкой установления делимости атома стали исследования электрического тока, проводимые физиками на протяжении всего XIX века. В 1874 г. ирландский физик Джордж Джонстон Стоуни высказал идею о том, что электричество состоит из элементарных зарядов, связанных с атомами, и вычислил величину этого элементарного заряда; в 1891 г. Стоуни предложил для него термин электрон.
Исследования электрических разрядов в разреженных газах и вакууме, которые начал в 1859 г. немецкий физик Юлиус Плюккер, привели к тому, что Вильгельм Гитторф и Уильям Крукс открыли в 1869-1875 гг. невидимые катодные лучи, распространяющиеся в вакууме от катода к аноду. Природа катодных лучей, которые распространяются прямолинейно и вызывают флюоресценцию (свечение) стекла вокруг анода, долгое время оставалась неизвестной; немецкие физики предполагали волновую, английские – корпускулярную природу катодных лучей. В 1886 г. немецкий физик Эуген Гольдштейн, экспериментируя с решетчатым катодом, открыл каналовые лучи, распространяющиеся противоположно катодным; была высказана гипотеза о том, что каналовые лучи состоят из положительно заряженных частиц.
Изучение катодных лучей привело и к другому важному открытию. Вильгельм Конрад Рёнтген обнаружил в 1895 г., что при падении катодных лучей на антикатод возникает новый вид излучения – X-лучи (рентгеновские лучи), которые обладают высокой проникающей способностью и вызывают флюоресценцию различных веществ.
Природа рентгеновских лучей также поначалу истолковывалась по-разному – помимо мнения, что X-лучи сходны с ультрафиолетом, высказывались и предположения об их корпускулярной природе. Окончательно волновая природа X-лучей была доказана лишь в 1913 г., когда Макс Теодор Феликс фон Лауэ обнаружил их дифракцию при прохождении через кристаллы.
Пытаясь проверить высказанное французским математиком Анри Пуанкаре предположение о том, что X-лучи не связаны с катодными лучами, Антуан Анри Беккерель начал изучение флюоресценции солей урана.
В 1897-1898 гг. французские учёные Пьер Кюри и Мария Склодовская-Кюри установили, что испускание уранового излучения является свойством атома урана. Результатом их работы стало открытие двух новых радиоактивных элементов – полония и радия,а так же введение нового термина – радиоактивность.
В 1899 г. английский физик Эрнест Резерфорд обнаружил неоднородность уранового излучения: в магнитном поле лучи разделяются таким образом, что можно выделить две составляющих, соответствующих потокам частиц с положительными и отрицательными зарядами.
Поль Виллар в 1900 г. выделил ещё один тип: лучи, не отклоняющиеся магнитным полем. Резерфорд предложил обозначать эти излучения первыми буквами греческого алфавита: альфа-, бета- и гамма-лучи.
Исследования радиоактивности в корне изменили классическое понятие атома; стало очевидным, что атом надлежит понимать как сложную систему, в образовании которой участвуют некие более простые частицы.
Модели строения атомов.
Первые модели строения атомов появились в начале 20 века.
В 1901 году Жан Перьен предложил планетарную модель атома. Подобную модель предложил в 1904 году японский химик Ханатаро Нагаока. В модели Нагаока атом был похож на планету Сатурн – ядро атома было планетой, а вращающие электроны его кольцами.
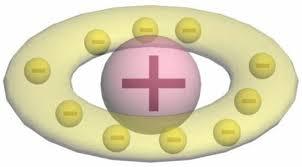
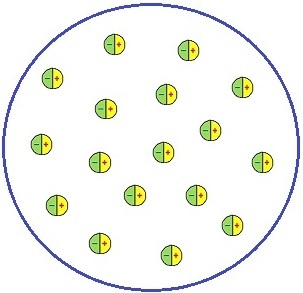
Однако более широкое представление о строении атома получила модель Томсона. В 1902 году Ульям Томсон предположил, что атом это сгусток положительно заряженной материи, внутри которой равномерно распределены электроны.
Такая модель атома напоминала кекс с изюмом (или пудинг), откуда произошло название модели – кексовая (пудинговая) модель строения атома.
Простейший атом – атом водорода – представлял собой, по мнению У. Томсона, положительно заряженный шар, в центре которого находится электрон. Детально данную модель разработал Дж. Дж. Томсон, считавший, что электроны внутри положительно заряженного шара расположены в одной плоскости и образуют концентрические кольца.
Немецкий физик Филипп фон Ленард попытался создать модель, не предполагающую раздельного существования в атоме противоположных зарядов. Атом, согласно модели Ленарда, состоит из нейтральных частиц (т.н. динамид), каждая из которых является электрическим дуплетом.
Выполненные Ленардом расчёты показали, что эти частицы должны иметь крайне малые размеры, и, следовательно, большая часть объёма атома представляет собой пустоту. Сосредоточение массы атома в небольшой части его объёма отчасти подтверждалось и проведёнными Ленардом в 1903 г. опытами, в которых пучок быстрых электронов легко проходил через тонкую металлическую фольгу.
Указанные модели атома Томсона-Томсона, Перьена-Нагаоки и Ленарда являлись сугубо гипотетическими и исключительно качественными.
В 1906-1909 гг. Ганс Гейгер, Эрнст Марсден и Эрнест Резерфорд, пытаясь найти экспериментальные подтверждения модели Томсона, провели свои знаменитые опыты по рассеиванию α-частиц на золотой фольге. Они использовали α-частицы вместо электронов, т.к. благодаря своей большей массе (в 7350 раз больше массы электрона) α-частицы не претерпевают заметного отклонения при столкновении с электронами, что позволяет регистрировать только столкновения с положительной частью атома. В качестве источника α-частиц ими был взят радий, а частицы, претерпевавшие рассеяние в тонкой золотой фольге, регистрировались по сцинтилляционным вспышкам на экране из сульфида цинка, находящемся в затемненной комнате.
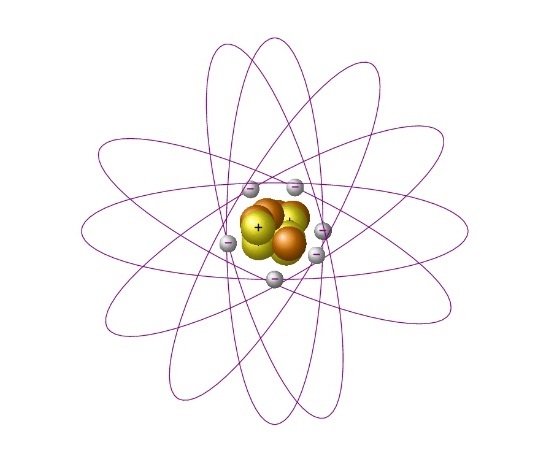
Результат опытов оказался совершенно противоположным ожидаемому. Большинство α-частиц проходило через золотую фольгу по прямым или почти прямым траекториям, но в то же время некоторые α-частицы отклонялись на очень большие углы, что свидетельствовало о наличии в атоме чрезвычайно плотного положительно заряженного образования. Основываясь на этих экспериментальных фактах, Резерфорд в 1911 г. предложил свою ядерную модель атома: в центре атома находится положительно заряженное ядро, объём которого ничтожно мал по сравнению с размерами атома; вокруг ядра вращаются электроны, число которых приблизительно равно половине атомной массы элемента.
Модель атома Резерфорда при несомненных достоинствах содержала важное противоречие: в соответствии с законами классической электродинамики вращающийся вокруг ядра электрон должен был непрерывно испускать электромагнитное излучение, теряя энергию. Вследствие этого радиус орбиты электрона должен был быстро уменьшаться, и рассчитанное из этих представлений время жизни атома оказывалось ничтожно малым. Тем не менее, модель Резерфорда послужила основой для создания принципиально новой теории, которую разработал в 1913 г. датский физик Нильс Хенрик Давид Бор.
Модель Бора опиралась на квантовую гипотезу, которую выдвинул в 1900 г. немецкий физик Макс Карл Эрнст Людвиг Планк. Планк постулировал, что вещество может испускать энергию излучения только конечными порциями, пропорциональными частоте этого излучения. Применив квантовую гипотезу для объяснения фотоэффекта, Альберт Эйнштейнв 1905 г. предложил фотонную теорию света.
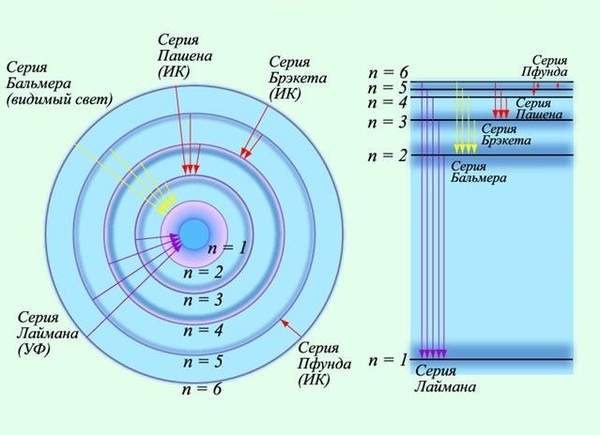
Ещё одной предпосылкой для боровской модели атома стали серии спектральных линий водорода, которые обнаружили в 1885 г. швейцарский ученый Иоганн Якоб Бальмер, в 1906 г. американский физик Теодор Лайман и в 1909 г. немецкий физик Фридрих Пашен. Эти серии (в видимой, ультрафиолетовой и инфракрасной областях спектра) подчинялись очень простой закономерности: частоты были пропорциональны разности обратных квадратов целых чисел.
Бор объяснил устойчивость планетарной модели атома и одновременно эти спектральные данные с позиций квантовой теории, сформулировав ряд постулатов, накладывающих на модель атома квантовые ограничения. Согласно постулатам Бора, электрон может вращаться вокруг ядра лишь по некоторым дозволенным ("стационарным") орбитам, находясь на которых, он не излучает энергию. Ближайшая к ядру орбита соответствует "нормальному" (наиболее устойчивому) состоянию атома. При сообщении атому кванта энергии электрон переходит на более удалённую орбиту. Обратный переход из "возбуждённого" в "нормальное" состояние сопровождается испусканием кванта излучения.
Для атома водорода расчёты спектров на основе модели Бора дали хорошее согласие с экспериментом, но для других элементов получалось существенное расхождение с опытными данными. В 1916 г. немецкий физик Арнольд Иоганн Вильгельм Зоммерфельд уточнил модель Бора. Зоммерфельд высказал предположение, что кроме круговых, электрон может двигаться и по эллиптическим орбитам.
В первой половине 1920-х гг. в модель атома были добавлены ещё два квантовых числа. Немецкий физик Альфред Ланде ввёл для описания движения электрона в атоме магнитное квантовое число, а молодые физики Джордж Юджин Уленбек и Сэмюэл Абрахам Гаудсмит в 1925 г. ввели в атомную физику представление о спине электрона, Следует отметить, что американский физик Артур Холли Комптон, основываясь на атомных спектрах высокого разрешения, ещё в 1921 г. высказывал предположение о квантованном вращении электрона, а в следующем году Отто Штерн и Вальдер Герлах экспериментально наблюдали разделение пучка атомов серебра в магнитном поле на две части, соответствующие ориентации электронных спинов.
В 1925 г. Вольфганг Паули опубликовал свою работу, содержащую формулировку принципа запрета, носящего его имя: в данном квантовом состоянии может находиться только один электрон. Паули указал, что для характеристики состояния электрона необходимо четыре квантовых числа: главное квантовое число n, азимутальное квантовое число l и два магнитных числа m1 и m2.
В 1927 г. немецкий физик Фридрих Хунд сформулировал эмпирические правила заполнения электронных оболочек. С применением запрета Паули и принципа насыщения уровней к 1927 г. была в целом построена электронная структура всех известных к тому времени 92 элементов.
Просто о химии. От античного атомизма к атомно-молекулярной теории.
Античный атомизм
Приблизительно в 5 до н.э. в древнегреческой философии возникла теория атомизма. Согласно это теории все вещества состояли из частиц – атомов. Основоположник этой теории – древнегреческий философ Левкипп, который утверждал, что существует предел деления – настолько малая частица, что дальнейшее ее деление невозможно. Демокрит, ученик Левкиппа, назвал такую частицу атомом. "Нет ничего, кроме атомов, вечно движущихся в бесконечной пустоте" – этот тезис Демокрита лёг в основу античного атомизма.
Основными характеристиками атомов, по мнению Демокрита, являлись размер, форма и весомость; число форм атомов бесконечно. Атомы вечны, неизменны, нераздельны, непроницаемы, не возникают и не уничтожаются. Соединяясь между собой в различных сочетаниях, атомы материи образуют новые вещества с различными свойствами. Сами атомы в соединениях сохраняют свою индивидуальность. Невидимые из-за своих малых размеров, они, имея неровную поверхность, способны сцепляться друг с другом и образовывать видимые вещи. Утверждая, что существуют только атомы и пустота, атомисты тем самым отвергают существование какого-нибудь "мирового ума", управляющего миром. Все события происходят путем взаимодействия атомов, их столкновения, сцепления или разъединения.
Атомы различались величиной, от которой в свою очередь зависела тяжесть. Догадка об атомном весе принадлежит древнегреческому философу Эпикуру. Однако уже Демокрит был на пути к этому понятию, признавая относительный вес атомов, который в зависимости от размеров бывает тяжелее или легче. Самыми легкими атомами он считал самые мелкие и гладкие шаровидные атомы огня, составляющие воздух, а также душу человека.
В средние века учение об атомах преследовалось религией, которая тормозила развитие всей науки и химии в частности.
Теория флогистона, кислородная теория и химическая революция как предпосылки к развитию теорий о строении атома.
Первой научной теорией химии стала теория флогистона. Основой для этой теории послужило представление о горении, как о процессе разложения тела. Создателями теории считаются два немецких химика – Георг Эрнст Шталь и Иоган Иоахим Бехер.
Суть теории флогистона можно изложить в следующих основных положениях:
1. Существует материальная субстанция, содержащаяся во всех горючих телах – флогистон (от греческого φλογιστοζ – горючий).
2. Горение представляет собой разложение тела с выделением флогистона, который необратимо рассеивается в воздухе. Вихреобразные движения флогистона, выделяющегося из горящего тела, и представляют собой видимый огонь. Извлекать флогистон из воздуха способны лишь растения.
3. Флогистон всегда находится в сочетании с другими веществами и не может быть выделен в чистом виде; наиболее богаты флогистоном вещества, сгорающие без остатка.
4. Флогистон обладает отрицательной массой.
Противоположностью теории флогистона стала кислородная теория. Она начала развиваться немного раньше теории флогистона, но окончательную «победу» над флогистоном одержала лишь после работ Пристли и Шееле по открытию кислорода. Труды этих двух химиков резюмировал третий – А.Л. Лавуазье и в 1777 году сформулировал основные положения кислородной теории горения:
1. Тела горят только в "чистом воздухе".
2. "Чистый воздух" поглощается при горении, и увеличение массы сгоревшего тела равно уменьшению массы воздуха.
3. Металлы при прокаливании превращаются в "земли". Сера или фосфор, соединяясь с "чистым воздухом", превращаются в кислоты.
Новая кислородная теория горения (термин кислород – oxygenium – появился в 1877 г. в работе Лавуазье "Общее рассмотрение природы кислот и принципов их соединения") имела ряд существенных преимуществ по сравнению с флогистоном. Она более проста, чем флогистонная, не содержала в себе "противоестественных" предположений о наличии у тел отрицательной массы, и, главное, не основывалась на существовании субстанций, не выделенных экспериментально. Вследствие этого кислородная теория горения довольно быстро получила широкое признание среди естествоиспытателей.
С созданием кислородной теории начался новый этап развития химии – «химическая революция». Именно в это время появились новая номенклатура веществ, «таблица простых тел». Так же были открыты законы, которые внесли важный вклад в развитие представлений о строении атома.
В 1789 г Лавуазье открыл закон сохранения масс:
"Можно принять в качестве принципа, что во всякой операции количество материи одинаково до и после опыта, что качество и количество начал остаются теми же самыми".
Закон эквивалентов сформулировал немецкий химик Иеремия Вениамин Рихтер (термин «эквивалент» ввел Г. Кавендиш):
"Если одно и то же количество какой-либо кислоты нейтрализуется различными количествами двух оснований, то эти количества эквивалентны и нейтрализуются одинаковым количеством любой другой кислоты"
В 1801 г Ж.Л. Пруст открыл закон постоянства состава:
"От одного полюса Земли до другого соединения имеют одинаковый состав и одинаковые свойства. Никакой разницы нет между оксидом железа из Южного полушария и Северного. Малахит из Сибири имеет тот же состав, как и малахит из Испании. Во всем мире есть лишь одна киноварь"
Закон кратных отношений, открытый в 1803 г Дальтоном.
Атомно-молекулярное учение развил и впервые применил в химии великий русский ученый М.В.Ломоносов. Основные положения этого учения изложены в работе "Элементы математической химии". Сущность учения Ломоносова можно свести к следующим положениям:
1. Все вещества состоят из "корпускул" (так Ломоносов называл молекулы).
2. Молекулы состоят из "элементов" (так Ломоносов называл атомы).
3. Частицы — молекулы и атомы — находятся в непрерывном движении. Тепловое состояние тел есть результат движения их частиц.
4. Молекулы простых веществ состоят из одинаковых атомов, молекулы сложных веществ — из различных атомов.
Через 67 лет после Ломоносова атомистическое учение в химии применил английский ученый Джон Дальтон. Он изложил основные положения атомистики в книге "Новая система химической философии". В своей основе учение Дальтона повторяет учение Ломоносова. Однако Дальтон отрицал существование молекул у простых веществ, что по сравнению с учением Ломоносова является шагом назад. По Дальтону, простые вещества состоят только из атомов, и лишь сложные вещества — из "сложных атомов" (в современном понимании — молекул). Атомно-молекулярное учение в химии окончательно утвердилось лишь в середине XIX в. На международном съезде химиков г. Карлсруэ в 1860 г. были приняты определения понятий молекулы и атома.
Большую роль в развитии атомистической теории сыграл выдающийся русский химик Д.И. Менделеев, разработавший в 1869 г. периодическую систему элементов, в которой впервые на научной основе был поставлен вопрос о единой природе атомов. Во второй половине XIX в. было экспериментально доказано, что электрон является одной из основных частей любого вещества. Эти выводы, а также многочисленные экспериментальные данные привели к тому, что в начале XX в. серьезно встал вопрос о строении атома.
Просто о химии. Атом.
Химия - наука о веществах. Эта наука исследует строение, свойства и превращения веществ.
Для того что бы понимать химические процессы необходимо подробно знать строение атома.
Атом – (от греческого atomos - неделимый) наименьшая частица химического элемента, носитель его свойств.
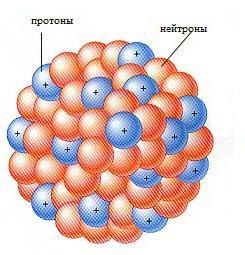
Атом состоит из положительно заряженного ядра и отрицательно заряженных электронов.
Ядро атома состоит из двух видов частиц: нейтронов, не имеющих заряда и положительно заряженных протонов, которые и определяют положительный заряд ядра.
Вокруг ядра атома вращаются отрицательно заряженные электроны, образующие электронное облако – совокупность всех электронов в атоме. О том, что такое электронное облако и электронное строение атома будет отдельная тема.
Число протонов равно числу электронов, поэтому атом – электронейтральная частица. Вспомните из школьного курса химии формулу: A = Z + N
Масса протонов и нейтронов приблизительно одинакова и равна ~ 1,67 * 10^(-27) кг. Масса электрона, в свою очередь, примерно равна 9,11 * 10^(-31) кг, поэтому основная масса атома сосредоточена в ядре.
Рассмотрим основные параметры, характеризующие атом
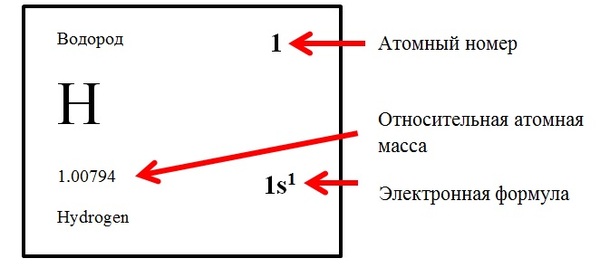
Атомный номер (порядковый номер) Z – номер химического элемента, определяемый по периодической системе элементов. Атомный номер элемента показывает количество протонов и электронов в элементе.
Атомная масса, а точнее относительная атомная масса – масса атома, выраженная в атомных единицах массы (а.е.м.). Она определяется как отношение массы данного атома к 1/12 массы нейтрального изотопа углерода 12С.
К понятию атомная масса близко понятие массовое число А – сумма чисел протонов и нейтронов (нуклонов) атома. Но численно оно равно только для изотопа углерода 12С, для остальных элементов массовое число – целочисленное значение, а относительная атомная масса нет. Например: массовое число изотопа водорода равно 1, а относительная атомная масса 1,00794 (см картинку)
А что такое изотопы?
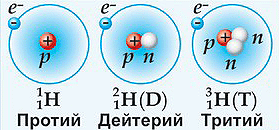
Изотоп - атомы одного элемента, имеющие одинаковый заряд ядра (следовательно, и количество электронов), но различное число нейтронов (следовательно, различные массовые числа). Например, элемент водород имеет семь изотопов, но наиболее всем известны и чаще всего встречаются из них три: 1Н протий, 2Н дейтерий и 3Н тритий.
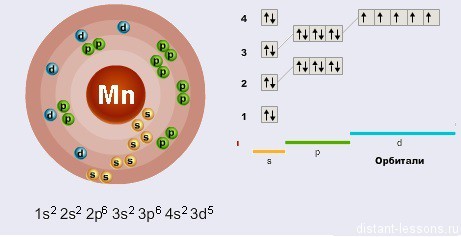
Электронная формула (конфигурация) – порядок заполнения электронов по различным электронным оболочкам.
Думаю, что на это стоит остановиться, ибо все в одном посте не охватишь.
Следующие посты будут посвящены электронному строению атома, истории открытия атома и развитию представлений о его строении.
Вот почему так?
Когда идёт худенькая девушка и ест мороженое, то это нормально, а когда ест полная, то сразу мысли в голове "хватит жрать, жируха!"
Лига юристов, прошу совета!
Мои старенькие бабушка и дедушка живут в деревне в частном доме. Одни из соседей по улице, которые находятся прямо через забор от моих родных, повадились сжигать бытовой мусор в металлическом баке прям у себя на участке (лень выносить). Запах и дым стоят невообразимые (сама свидетель). Бабушка сердечница и плохо переносит дым, начинает задыхаться. Разговоры с этими соседями и обещание вызвать пожарных/полицию не возымели воздействия. Собственно, вопрос: законно ли на своей (частной) территории сжигать бытовой мусор и если нет, то как можно законным путем воздействовать на соседей? Куда обращаться и как поступать в случае очередного акта сжигания мусора?
Перлы от пациентов
Понимаю, что тема уже триста раз обсуждена и изъезжена, но иногда не поделиться с окружающими не получается.
У моей подруги вся семья работает в медицине. Мама - участковый педиатр, отец - хирург, сестра - фармацевт. Вот несколько интересных на мой взгляд случаев, произошедших с ее родными (далее со слов подруги).
Приходит на прием молодая мама с годовалой дочкой. Жалуется на геморроидальную сыпь на спине ребенка. При осмотре - обычная крапивница. На вопрос, что это за чудный зверь - сыпь геморроидальная, мамочка гордо ответила "ну так же в тырнете пишут, я читала и картинки смотрела, очень похоже!" Выяснилось, она имела в виду геморрагическую сыпь.
Одна дама на полном серьезе спрашивала на приеме, что за препараты ряда фуфломицин и что ими лечат.
Бабулька после нефрэктомии требовала отдать ей почку, чтобы врачи не продали её контрабандистам. Обещала пожаловаться во все инстанции, если почку ей не вернут.
В приемник поступил парень с кишечной непроходимостью. Пока выясняли в чем причина, парень тихонечко шепнул на ушко медсестре, что пару дней назад была диарея и решил ее остановить с помощью... монтажной пены! Думал, что когда ему полегчает, то пена высохнет и легко выйдет наружу (ну она же не прилипнет внутри!). Не прокатило. Чем закончились дела у горе-монтажника не знаю, но никогда бы в жизни не поверила в эту историю, если бы это рассказал бы не отец.
Ну и напоследок названия препаратов, которые часто спрашивают в аптеке:
децибел - дицетел
таблетки в форме жопки/сердечка - конкор/кардиомагнил
переспал - эреспал
что-то там фен - нурофен, ибупрофен
нульфаза - нольпаза
такую огромную для желудка - гастрофарм
свечи от молочницы во рту у ребенка
Подруга моя, написано с ее разрешения, тег - моё.
Что это было?
Проснулась сегодня после ночной смены от звонка на мобильный телефон. На том конце провода оказалась девушка из социальной защиты. Звонила, что бы узнать, почему я 2 года не иду к ним оформлять льготы. Девушка была предельно вежлива и сказала, что выплаты, начисленные за 2 года ждут меня и вообще мне будут очень рады видеть меня.
Третий час думаю, а я вообще в той вселенной проснулась или как?