Про иммунитет, рак и аллергию, часть третья: анатомия
Привет, Пикабу!
Меня поглотили дела и третья часть задержалась на пару дней, но она здесь. Сегодня поговорим об анатомическом устройстве иммунной системы.
Помню, когда мне было 14, я делал доклад на одном турнире, где представлял модель червяка-конструктора. Один из членов жюри спросил меня, что на счет иммунной системы? И я на полном серьезе ответил, что ее сложно считать самостоятельной системой органов. Ох, ребят, как же я был неправ.
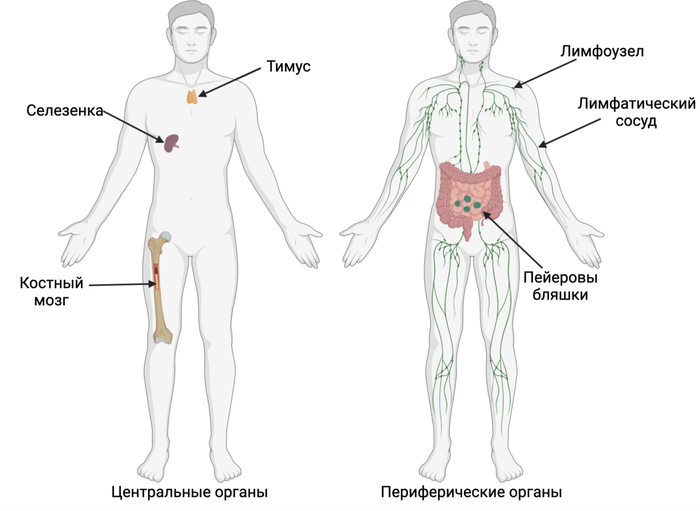
Иммунная система - сложно устроенная сеть из центральных и периферических органов, соединенных лимфатическими сосудами. Вообще это все сильно похоже на кровеносную систему:
Это, естественно, неспроста: лимфатические сосуды - трассы для движения иммунных клеток, без них нормальная функция иммунитета невозможна.
Иммунная система делится на центральные и периферические органы. Наверное, из картинки выше вы уже догадались, какие органы какие, но я все же отдельно распишу.
К центральным органам относятся те, у которых есть специфическая роль в работе системы: тимус, селезёнка и костный мозг.
К периферическим - Пейеровы бляшки, лимфоузлы и сосуды, у которых особых функций нет, это скорее система перемещения зрелых лимфоцитов.
Дальше поговорим про функции всего этого добра. Начнем, естественно, с центральных органов. Я не буду грузить вас их строением, для понимания происходящего это, честно говоря, не нужно.
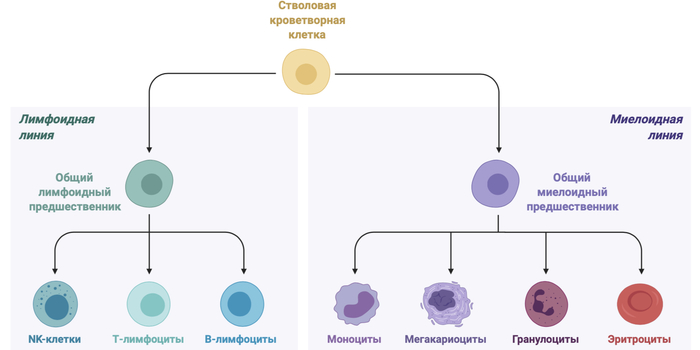
Итак, орган, с которого все начинается - костный мозг. Точнее говоря, красный костный мозг. По сути, это орган кроветворения. В нем зарождаются вообще все клетки, связанные с лимфатической и кровеносной системами:
При этом созревание В-лимфоцитов и NK-клеток идет в костном мозге (но NK дозревают вообще везде), а вот Т-лимфоциты едут в тимус и дозревают уже там. Иначе говоря, красный костный мозг критически важен для появления новых клеток.
Следующий на очереди - естественно, Тимус.
Тимус, или вилочковая железа, в качестве органа иммунной системы выполняет чуть ли не главную роль: отсев головорезов организма.
Под головорезами я имею в виду Т-клетки. Их, в принципе, есть три разных типа: T-регуляторные, Т-хелперы и Т-киллеры. Все вместе они формируют Якудза иммунной системы, именно от них очень стараются спрятаться опухоли и все внутриклеточные патогены. Мы поговорим о них позже, но важно понимать, что за Т-клетками нужен очень строгий контроль, выпустить дефектный клон, который потенциально может породить линию клеток, атакующих свой же организм, нельзя. Именно поэтому Т-клетки дозревают в Тимусе. Они проходят сложный процесс двойной селекции:
В общих чертах отбор Т-клеток заключается в двух этапах проверки активности Т-лимфоцита: сначала проверяется работоспособность рецептора, потом - атака собственных антигенов. Если клетка среагировала оба раза, она погибает. Если клетка не прошла первую проверку - она погибает. По итогу остается 5% от незрелых Т-лимфоцитов.
Это очень сложный процесс, и отвечают за него именно клетки тимуса, которые и проводят проверку.
Интересный факт: тимус, видимо, связан с процессом старения организма. Дело в том, что к 12-14 годам он претерпевает инволюцию: уменьшается в размерах, частично теряет свою функцию. Оказалось, что использование таких веществ, как мелатонин (гормон сна) или гормонов эпифиза (и так контролируют тимус) способно замедлить и даже обратить инволюцию. Жить до 150 лет это не позволит, но улучшение состояния стареющих людей наблюдаем.
Следующий гость программы - селезенка. С ней достаточно коротко.
Селезенке в разных источниках приписывают кучу разных функций, некоторые мне кажутся прямо бредовыми. Например, на Википедии вы можете прочитать, что селезенка продуцирует антитела. Она этого, конечно, не делает - продукцией антител занимаются В-клетки, которые, да, в селезенке сидят.
Основная ее функция - депо и фильтр крови. В селезенке хранится значительный процент всех тромбоцитов организма, а также в красной пульпе перерабатываются старые эритроциты.
Селезенка также участвует в процессе созревания лимфоцитов и служит их депо наравне с лимфоузлами.
Периферические органы иммунной системы - это система магистралей для лимфоидных и миелоидных клеток.
Зрелые наивные (не знакомые с антигеном) лимфоциты сидят в лимфоузлах. Резидентные клетки неспецифического иммунитета (конкретно дендритные, но об этом в следующий раз) по лимфатическим сосудам из места поражения приходят в ближайший лимфоузел и начинают искать лимфоциты, у которых есть рецептор именно к этому антигену.
Самая сочная часть этой системы - Пейеровы бляшки.
Это своего рода тоже лимфоузлы, точнее скопления лимфатических фолликулов. Бляшки сидят в подвздошной и тощей кишке, и у них офигенно интересная функция - они обеспечивают процесс рециркуляции лимфоцитов в кишечнике. Что это такое, в двух словах: лимфоциты брыжеек (соединительно-тканые перемычки между петлями кишечника), реагируя на антиген, отправляются в пейеровы бляшки и там запускают процесс, вовлекающий слизистые ЖКТ и приводящий к продукции огромного количества иммуноглобулинов, например IgA. Аллергики и люди с аутоиммунками тут, скорее всего, подняли одну или две брови - сколько умеете, я только вместе вот могу - вверх. IgA часто выпадают из нормы в случае аутоиммунок и аллергий, запрос в гугле "IgA allergies" выдаст прорву статей по теме. И Пейеровы бляшки в этом деле замешаны, все верно.
Есть еще одна очень интересная история, с ними связана. Эта история - голый землекоп:
Эта животина сейчас находится под прицелом огромного числа ученых, потому что у нее не бывает рака. Вы сейчас правильно прочитали, эта хрень живет под тридцать лет и считается условно бессмертным животным: у них не наблюдается онкологий и старения и не совсем понятно, как и почему они умирают. Цитируя одного моего лектора, "мы не знаем, почему они умирают, не считая очевидных случаев. Возможно, в какой-то момент своей жизни голый землекоп просто решает, что все, ему хватило этой жизни, и отправляется на тот свет".
Как они связаны с Пейеровыми бляшками? У землекопов их нет. Вообще.
На этом все, следующую часть постараюсь выложить по расписанию!
==============
FAQ:
1. Я ученый, иммунолог, работаю с раком;
2. Я НЕ врач;
3. Я с удовольствием отвечу на ваши вопросы и скину ссылки на статьи и книги, из которых беру информацию;
4. Я не буду смотреть на ваши результаты анализов (и все в таком роде), так как не имею квалификации медика, а потому и права давать медицинские советы. Обращайтесь к профильным врачам, не бойтесь медиков и не жалейте ресурсов на свое здоровье.