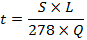Нитраты в воде и методы удаления
Нитраты в воде и методы удаления.
Нитраты — это соли азотной кислоты, хорошо растворимые в воде. В воде эти соли легко распадаются на ионы (заряженные частицы) и существуют в "свободной" форме: в виде нитрат-ионов NO3—. Заряд у нитрат-ионов отрицательный, поэтому они называются анионы (ионы с отрицательным зарядом).
Источники появления нитратов в воде
Нитраты своему широкому появлению обязаны селитре, которая активно задействована при возделывании сельскохозяйственных культур в качестве удобрения. Дешевизна химиката и эффективное влияние на рост и созревание растений зачастую приводят к его передозировке. Как результат – селитра вместе с осадками проникает в грунтовые воды, после чего вода попадает в систему питьевого водоснабжения.
Существуют и другие причины, из-за которых в водоносных горизонтах находится вода с нитратами с превышенным уровнем допустимых норм. Источником заражения выступают:
- недопустимо близкое соседство скважины с частным туалетом, септиком, баней или выгребной ямой;
- применение бытовой химии, после чего отработанный раствор сливают попадает в грунт без очистки;
- обустройство питьевой скважины неподалёку от массовых захоронений, кладбищ;
- завышенная концентрация удобрений для роста огородных культур;
- городские коммунальные отходы, промышленный мусор.
Нитраты входят в 3 класс опасности, по нормам СанПин предел в 45 мг/дм3.
Содержание в воде нитратов может колебаться в зависимости от сезона.
Ещё большую опасность для здоровья человека представляют производные нитратов – нитриты. Нитриты относится ко 2 классу опасности, уровень содержания примесей по требованиям СанПин не должно превышать 3 мг/дм3 соответственно.
Нитраты и нитраты могут накапливаться в организме. Поэтому, с целью обезопасить собственное здоровье, при употреблении воды из скважины лучше придерживаться минимальных значений.
Влияние нитратов на организм человека.
Находясь в организме, нитраты взаимодействуют с гемоглобином. В результате химической реакции гемоглобин в крови человека замещается метгемоглобином. Новое соединение не способно насытить клетки тела необходимым кислородом, что вызывает ряд негативных последствий.
Кислородное голодание сопровождается рядом неприятных симптомов: развивается анемия; человека сопровождает постоянное чувство усталости; длительное воздействие нитратов в дозах, значительно превосходящих нормы, провоцирует обмороки и в крайних случаях заканчивается летальным исходом.
Кроме этого, регулярное употребление воды с содержанием нитратов выше установленных значений, может спровоцировать: развитие злокачественных образований; появление аллергических реакций; всевозможные раздражения на поверхности кожи и слизистых оболочках; оказывать угнетающее действие на функционирование щитовидной железы; нарушить работу нервной системы; проблемы с ЖКТ.
Методы очистки воды
На сегодняшний день широко применяется три метода:
1.- удаление нитратов из воды анионообменными смолами:
2.- удаление нитратов из воды обратным осмосом.
3.- фильтрование воды через цеолит.
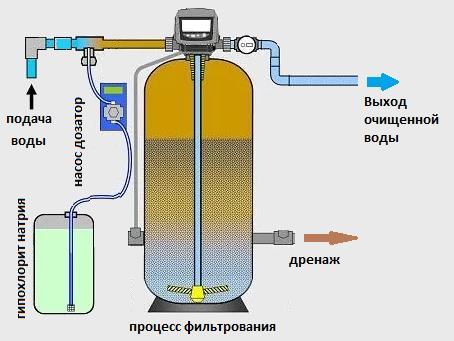
Применение анионообменных смол
Поскольку у частицы есть заряд, то здесь её можно поймать, так как отрицательный заряд притягивается к положительному. Для этого разработаны специальные вещества — нитрат селективные (избирающие нитраты) анионообменные смолы, то есть смолы, которые производят обмен нитрат-анионами.
Анионообменная смола — это длинная органическая молекула, на которую "подвешены" активные центры с положительным зарядом, защищённым слабо держащимся ионом с отрицательным зарядом.
Сильноосновные аниониты (в хлористой форме) селективны последовательно к:
сульфатам→ нитратам → хлоридам → бикарбонатам.
На активных центрах анионообменной смолы происходит обмен одних анионов например хлорид-ионы (Cl —), которые держатся за смолу слабо на нитрат-ионы, которые легко замещают слабые хлорид-ионы. Итак, вода проходит через смолу, нитраты заменяют хлориды, задерживаются на смоле. Хлориды попадают в воду вместо нитратов. Что происходит, когда заканчиваются свободные активные центры с хлоридами - Нитраты перестают задерживаться.
При использовании данной загрузки необходимо тщательно контролировать объем воды, который проходит через фильтр с анионитами. Это связано с тем, что со временем в процессе фильтрации накопленные нитраты начинают вытесняться. В итоге концентрация нитратов повышается до уровня исходной воды. То есть, если превысить расчётный объем воды, возможен не только проскок нитратов, но и сброс их из фильтра в воду. Необходимо всегда производить точный расчёт обменной ёмкости, так как от этого зависит качество потребляемой воды и работа всей установки. Регенерацию проводят до того, как начнётся проскок нитратов в фильтрат.
Если жёсткость поступающей на установку воды выше 2 мг экв/л, ее необходимо предварительно умягчать, так как сильноосновные аниониты не удаляют ионы кальция и магния.
В противном случае при регенерации анионита в его массе будут скапливаться труднорастворимые соединения, что повлечёт за собой снижение ёмкости анионита.
Очерёдность фильтров при этом очень важна! Сначала снижаем жёсткость, потом удаляем нитраты.
Применение нитратселективных анионитов
Желательно использовать такую смолу даже при большом количестве сульфатов в воде, так как она избирательна, прежде всего по отношению к нитратам.
Селективность данных анионитов: нитраты→сульфаты→хлориды→бикарбонаты.
Объёмная ёмкость данной загрузки ниже стандартной смолы. Нитратселективная также как стандартная смола может вызвать сброс нитратов, если позволить выйти за ее расчётный запас обменной емкости, селективная к нитратам смола может вызвать сброс сульфатов, а позже и нитратов, если вовремя не произвести ее регенерацию.
Вывод: тип анионита для очистки воды от нитратов выбирают на основании информации о содержании в исходной воде нитратов и сульфатов:
▫ если содержание сульфатов не превышает содержание нитратов, целесообразно использовать стандартные высокоосновные аниониты;
▫ если концентрация сульфатов превышает концентрацию нитратов, более целесообразно применять нитратселективные аниониты.
Определение содержания нитратов и расчеты времени работы сменных картриджей или анионообменной смолы осложняется тем, что их концентрация может меняться, необходимо вовремя отследить увеличение, чтобы продлить ресурс фильтрующей загрузки. Важен постоянный регулярный контроль и соответствующая корректировка работы установки.
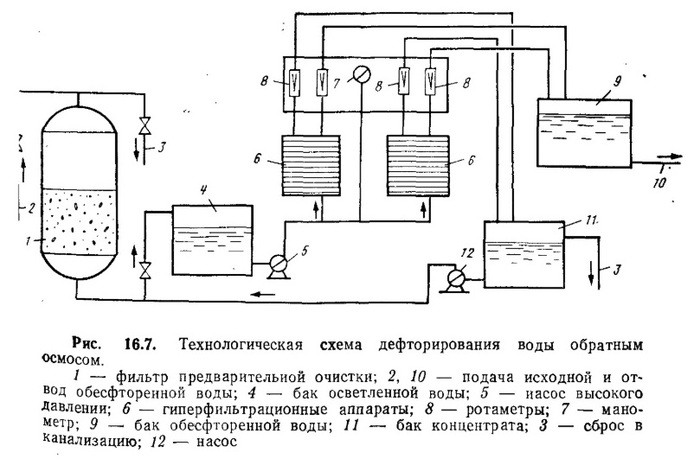
Применение обратного осмоса
Обратный осмос считается одним из наиболее эффективных способов очистки воды не только от нитратных, но и других соединений, которые загрязняют воду.
фильтрование воды через цеолит
Следующий вариант очистки воды от нитратов предполагает использование в качестве загрузки природных минеральных сорбентов (шунгита) или молекулярных сит (цеолитов).
Цеолиты – синтетические или природные адсорбенты с регулярной структурой пор, представляющие собой алюмосиликаты натрия, калия либо иных элементов. В промежутках кристаллического каркаса расположены гидратированные положительные ионы щелочных и щелочно-земельных металлов, компенсирующих заряд каркаса, и молекулы воды.
Общая химическая формула цеолитов: Ме2/n[(Аl203) x (Si02)y].Н20,
где Me – катион щелочного металла; n – его валентность.
В качестве катионов природные цеолиты чаще всего включают натрий, калий, кальций, реже – магний, барий, стронций. Кристаллическая структура цеолитов образована тетраэдрами Si04 и Аl04.
Поскольку цеолит обладает способностью поглощать или пропускать через кристаллический каркас молекулы других химических соединений, он играет роль своего рода молекулярного сита. Также цеолиты относят к ионообменникам катионного типа, то есть они могут очищать воду от тяжёлых металлов. И если сравнивать с синтетическими смолами, то этот способ лучше избавляет жидкость от ионов цезия, свинца, кадмия, стронция.
При очистке воды от нитратов, например, из скважины, природные цеолиты используются в виде порошков. Отработавший цеолит подвергают неоднократной регенерации при помощи исходный воды либо солевого раствора – выбор зависит от целевого использования.
Ниже показана степень эффективности очистки цеолитом от загрязнений.
Эффективность водоочистки цеолитом по органическим и неорганическим загрязнителям:
№ Вредные вещества Степень очистки, %
Пестициды 89,6
Нитриты 99,8
Нитраты 92,5
Хлор (хлорид-ион) 91,2
Но не стоит обольщаться, что только при помощи одного цеолита удастся справиться со всеми названными загрязнениями. Причина кроется в том, что структура этого минерала обладает различными пустотами, которые соответствуют разным веществам. Например, цеолит, справляющийся с нефтепродуктами, будет бесполезен при очистке воды от нитратов только из-за различной геометрии веществ.