Измеряя пустоту, или предшественники Гидрометцентра
«Природа не терпит пустоты». Эти слова Аристотеля сегодня воспринимаются как афоризм, а вот в Средние века их понимали достаточно буквально. Использовали это правило для объяснения некоторых физических явлений. Например, подъем воды в насосах. Но в 1595 году Галилео Галилей вместе с учениками, наблюдая за работой колодцев, убедились, что насосы не поднимают воду больше, чем на 10 метров. В своей книге «Беседы» он так описал этот факт: «Заметив первый раз такой случай, я подумал, что насос испорчен, и позвал мастера для починки; последний заявил, однако, что все было исправно, но что вода опустилась до той глубины, с которой она не может быть поднята насосом вверх, при этом он прибавил, что ни насосами, ни другими машинами, поднимающими воду всасыванием, невозможно поднять воду и на волос выше восемнадцати локтей; будут ли насосы широкими или узкими – предельная высота остается той же самой».
Галилей не смог дать научного объяснения этому ограничению и отшутился: «Очевидно, природа боится пустоты до высоты 18 локтей» (десяти метров). А вот его ученики, Эванджелиста Торричелли и Винченцо Вивиани, продолжили ломать голову над решением этой задачи.
Вокруг них образовался своего рода кружок образованных и любознательных итальянцев, поставивший своей целью утверждение экспериментального метода в познании мира (начало этой работе положил еще Галилей). Со временем кружок вырос в Флорентийскую академию опыта, которая достойна отдельного рассказа. Но вернемся к вопросу десятиметрового предела работы насосов.
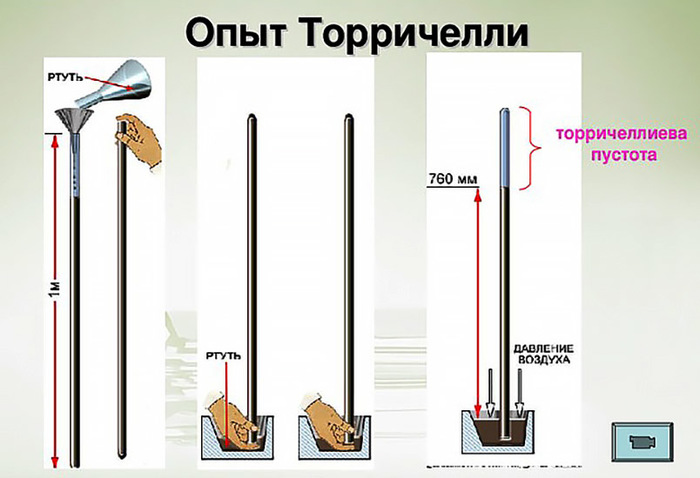
Торричелли решил проверить, до какой высоты будет бояться пустоты ртуть. Он взял метровую стеклянную трубку и заполнил ее ртутью. Потом закрыл один конец пальцем, а второй опустил в сосуд с этим же веществом. Ртуть стала опускаться и остановилась на высоте 760 мм. Потом этот опыт самостоятельно воспроизвел Вивиани.
Проведя опыт несколько раз ученые увидели, что этот уровень подвержен незначительным изменениям. Тогда Торричелли высказал революционную идею для своего времени: воздух давит на поверхность ртути в сосуде и это давление определяет ее уровень в трубке. А то, что это давление может меняться заставляет уровень колебаться.
В 1644 году Торричелли писал: «Мы погружены на дно безбрежного моря воздушной стихии, которая, как известно из неоспоримых опытов, имеет вес. Причем он наибольший вблизи поверхности Земли». Так поэтично итальянец описал атмосферное давление.
Заслуги Торричелли были отмечены и в научной терминологии. Образующееся пустое пространство в трубке так и назвали «торричеливая пустота», а еще есть такая единица измерения давления – торр, которую еще называют миллиметр ртутного столба. Но не все согласились с Торричелли, продолжая утверждать, что дело все-таки не в атмосферном давлении, а в том самом страхе природы перед пустотой.
Доказать правоту итальянца пробовал известный французский математик, физик и поэт Блез Паскаль. Сначала, с помощью ряда опытов, он доказал, что пространство в трубке над ртутью не заполнено ни её парами, ни разреженным воздухом, ни некоей «тонкой материей». «Можно считать это пространство действительно пустым», – заключил он и значит, вопреки Аристотелю, пустота может существовать в природе.
Дальше надо было доказать, что на ртутный столбик влияет именно давление воздуха. Для этого Паскаль отправил своего зятя с прибором Торричелли в горы. Тот провел измерения на разной высоте и установил: разница в высоте столбика ртути на вершине и у подножия горы составила 3 дюйма 1 1/2 линии. Паскаль продолжил изучать это явление и в итоге сформировал идею гидравлического пресса и сделал ряд важный открытий в области гидростатики. Благодарные потомки назвали его именем единицу измерения давления и напряжения (в механике) в системе СИ. Но многие современники Паскаля заявили: «Не убедил!», и продолжили отстаивать правоту Аристотеля.
Точку в этом споре поставил немецкий физик и инженер Отто фон Герике, поставивший в 1654 году знаменитый Магдебургский эксперимент, в ходе которого доказал наличие давления воздуха; установил его (воздуха) упругость и весомость, а заодно - способность поддерживать горение, проводить звук. Уже этого было достаточно, чтобы войти в историю, но немец не остановился и через три года построил первый барометр. И с его помощью стал наблюдать за погодой. В итоге, в 1660 году привел жителей Магдебурга в крайнее смущение, предсказав бурю за два часа до ее начала.
Барометр фон Герике, правда, совсем не походил на современные: он состоял из медной трубки длинной в 20 магдебургских локтей (11 метров), заполненной водой вместо ртути. На этом отличия от конструкции Торричели, собственно, и заканчивались. Трубка крепилась к наружной стене трехэтажного дома Герике. Эта конструкция выглядела достаточно убедительно, чтобы завершить, наконец, споры со сторонниками аристотелевской точки зрения.
Убедительно, но неудобно. Иметь дома прибор, предсказывающий бурю, или даже – дождь хотели бы многие. Но не таких габаритов. Спрос рождает предложение, и вскоре мастера стали изготавливать компактные, можно сказать, комнатные версии «трубки Торричелли». Конечно, поначалу счет шел на единицы и покупала их преимущественно просвещенная публика.
В числе тех, кто увлекся опытами с измерением атмосферного давления был английский физик Роберт Бойль. Он усовершенствовал прибор и в 1665 году дал ему новое название – барометр. Эту работу продолжил помощник, Роберт Гук, который начал создавать барометры в форме колеса или банджо. А заодно разработал для них шкалу, где низкое давление соответствовало дождю или шторму, а высокое – хорошей и сухой погоде. Он вообще был очень изобретательным ученым: придумал спиральную пружину для регулирования хода часов, первую в мире систему оптического телеграфа и много других полезных вещей.
В последующие пару столетий выпускали разные барометры, и с вертикальной трубкой, и с круглой шкалой. Но высота корпуса у них была одинакова, равная высоте того самого ртутного столба (порядка 75 см).
Исключением из этого «тренда» стал прибор для измерения давления, придуманный знаменитым ученым Готфридом Лейбницем в 1698 году. В нем вообще не было жидкости, почему изобретатель назвал его анероид (греч. a — частица отрицания + nērós — «вода»). Он показывает давление, действующее на гофрированную тонкостенную металлическую коробку, внутри которой создано разрежение. При повышении давления коробка слегка сжимается, а при понижении – слегка расширяется. Этих колебаний достаточно, чтобы показать результат на шкале анероида, где обычно делались надписи «дождь», «переменно», «ясно» и проч.
Этот прибор за свои малые размеры пришелся по душе путешественникам. Вероятно, был он (вместе с классическим барометром) и на борту британского экспедиционного судна «Бигль», когда на нем совершал свое знаменитое путешествие Чарльз Дарвин. Во всяком случае – у капитана корабля Роберта Фицроя, который очень интересовался закономерностями погодных изменений. Для него это была не первая успешная экспедиция (и не последняя), что благотворно сказалось на карьере моряка. В последующие годы, он успел побывать депутатом парламента, губернатором Новой Зеландии. А затем, в 1854 году, уже в чине адмирала, он стал основоположником метеорологической службы Великобритании.
Адмирал Фицрой разработал свой вариант барометра (носящий его имя) с бумажной шкалой и указаниями, как с его помощью предсказывать погоду. Силами ведомства Фицроя была создана сеть метеорологических станций: девятнадцать в Англии, одна в Копенгагене, одна в Голландии, две во Франции (Брест и Байен) и ещё одна в Лиссабоне. Станции были соединены с центром службы погоды недавно изобретённым телеграфом Морзе. Сведения о погоде, собранные с этих станций, анализировались в центре службы погоды и на основании этого анализа давались рекомендации. Изучение погоды перестало быть делом одиночек, на смену шла система.
Вскоре Фицрой написал первый учебник по метеорологии, который в 1865 году был переведен на русский язык под названием «Практическая метеорология контр-адмирала Фицроя». «Мы живём в воздушном океане, все изменения погоды зависят от солнечного излучения. Нужно помнить, что состояние воздушного океана скорее говорит о будущей погоде, чем о погоде в настоящий момент», - писал он во введении.
Предсказание погоды из прерогативы шаманов, жрецов и тому подобной публики стало обычным делом. В 1873 г. в Вене состоялся первый международный метеорологический конгресс, на котором был выработан ряд стандартов для синоптиков разных стран.
Наша страна в этом отношении не отставала, во второй половине XIX века был создан ряд ведомственных метеорологических сетей из десятков станций и дождемерных пунктов.
В 1913 г. по представлению академика М. А. Рыкачёва, директора Главной физической обсерватории (ГФО), был подготовлен закон, касающийся Гидрометеослужбы, позволявший существенно увеличить её финансирование и возможности. Законом предусматривалось создание 150 постоянных и 50 опорных новых станций. Центральным метеорологическим учреждением России стала собственно ГФО.
Эта система стала еще более мощной в годы Первой мировой войны, но была практически уничтожена последовавшей за ней Гражданской. Восстановить ее в дореволюционных масштабах удалось лишь к 1930-м годам. Ну а дальше начинается совсем другая история.