История обыкновенной батарейки
Эта музыка будет вечной
если я заменю батарейки
Слово «батарея», происходящее от французского слова «batterie», настолько давно вошло в русский язык, что точный словарный перевод по степени очевидности вызывает в памяти бессмертные строчки из Чехова: - «Волга впадает в Каспийское море, лошади кушают овес и сено». Вот сами посудите, это строчка из русско-французского разговорника:
фр. batterie (сущ.) - батарея.
Только серьезно задавшись целью выяснить этимологию этого слова, через некоторое время можно добраться до объяснения, что batterie - это battre «бить» - соединение нескольких однотипных приборов, устройств в единую систему или установку для эффективного совместного действия. Название происходит от артиллерийской батареи, как исторически первого типа батарей. Впоследствии название стало употребляться для обозначения соединения однотипных предметов вообще.
Кстати, отсюда вытекает то, что в быту мы в общем-то неправильно называем батареями пальчиковые элементы питания, потому что они – сюрприз – одиночные гальванические элементы.
Итак, наш пост про гальванические элементы, иначе именуемые батарейками.
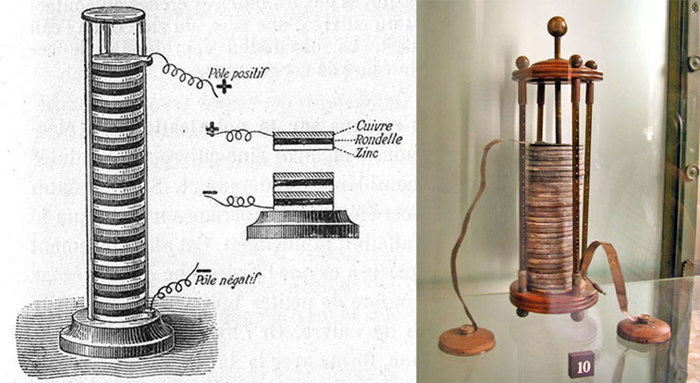
Быстренько пробежимся по истории. Хотя в последнее время археологи стали утверждать, что что-то похожее на химические источники тока появились в Мессопотамии за 100 лет до н.э. (так называемая Багдадская батарейка), но это все на уровне гипотезы, а официальное рождение батареи относят к 1800г, когда итальянский физик Алессандро Вольта, основываясь на опытах итальянского врача и анатома Луиджи Гальвани, сделал устройство, получившее впоследствии название «вольтов столб». Сложив стопку высотой полметра из пластинок цинка, меди и войлока, смоченного раствором серной кислоты, Вольта, приложив руки к концам стопки, получил весьма чувствительный удар током. Так началась электрическая эра.
Изобретение Алессандро Вольта произвело фурор в обществе, Вольта осыпали почестями и наградами, его именем назвали единицу электрического напряжения. Свою долю славы получил и Луиджи Гальвани - в честь его электрохимический элемент, изобретенный Вольта, называется гальваническим (несколько парадоксально, конечно).
Для легкости понимания давайте вспомним немного сведений из школьной программы про гальванический элемент. Я, естественно, не помнил, поэтому пришлось читать. Прочел, осмыслил длинную нудную фразу и пересказываю более простыми словами: гальванический элемент – это источник электрического тока, основанный на химической реакции двух металлов (или их оксидов для удешевления/простоты использования), один из металлов, именуемый анодом, всегда более активный, чем второй, называемый катодом, эти металлы помещены в токопроводящую среду, именуемую электролитом, при соединении этих металлов проводником образуется электрическая цепь и начинает вырабатываться ток, который бежит от анода (-) к катоду (+).
(Перечитав) Ну, тоже длинно, но хоть более-менее понятно.
Гальванические элементы делятся на два типа – первичные и вторичные. Первичные напрямую преобразуют химическую энергию, содержащуюся в реагентах гальванического элемента, в электрическую энергию. Этот процесс идет до полного расхода реагентов, после чего выработка электричества прекращается. Проще говоря, это одноразовые элементы. Все батарейки являются первичными гальваническими элементами.
Вторичные гальванические элементы – элементы, в которых электрическая энергия от внешнего источника тока превращается в химическую энергию и накапливается, а затем, при необходимости, химическая энергия снова превращается в электрическую. Эти вторичные элементы называются аккумуляторами. Про аккумуляторы мы опустим, эта обширная тема достойна отдельной большой статьи.
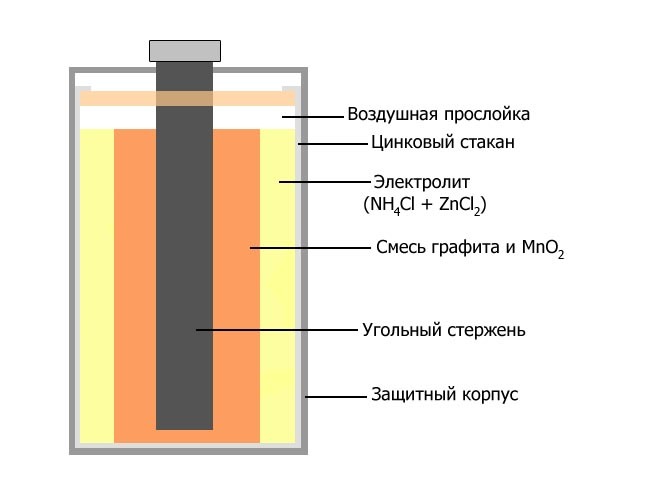
Одним из первых гальванических элементов, которым можно было пользоваться вне лабораторий, был изобретен Жоржем Лекланше в 1866 году. Конструкция имени Лекланше проста - цинковый анод, катод из диоксида марганца с углем, размещенные в электролите из хлорида аммония, т.е. соли аммония. В течении некоторого времени элемент Лекланше претерпел изменения: цинковый анод стал делаться в виде цинкового стаканчика, в стаканчике размещен катод из смеси диоксида марганца и графита, в центре катода находится угольный стержень, являющийся токосъемником (в некоторых источниках именно он неправильно называется катодом), катод окружен электролитом из хлорида аммония с добавкой хлорида цинка, только не в жидком виде, как у Лекланше, а в загущенном, в виде геля, из-за добавления крахмала и муки. Это необходимо для того, чтобы электролит не мог вытечь или высохнуть при хранении и эксплуатации элемента. Элементы с загущенным электролитом получили название «сухие батареи».
А вот сейчас, между прочим, вы прочли описание классической конструкции солевого гальванического элемента, по такой технологии он производится уже 150 лет без особого изменения. Получается как-то не очень хорошо с темпами развития науки в смежных областях – в отличие от бурного, взрывного роста возможностей электроники, за 60 лет уменьшившее компьютер MARK-1 весом 5 тонн и площадью 60 кв.м до микросхемы весом в доли грамма и площадью с булавочную головку, причем с намного большими возможностями, и этот хайтек питает энергией древняя двухсотлетняя технология. Печально. А что еще грустно, фирмы, выпускающие элементы питания, не испытывают никаких иллюзий в появлении прорывных, революционных технологий производства портативных источников тока и откровенно говорят, что в ближайшем и даже не очень ближайшем будущем нас ожидает только постепенное улучшение характеристик батарей. Понемногу, по проценту - по полпроцента в год.
Разумеется, какие-то всплески на плавном растущем графике улучшения характеристик были. И одним из всплесков было появление щелочных батарей.
Щелочная, она же алкалайновая (алкалиновая) батарея.
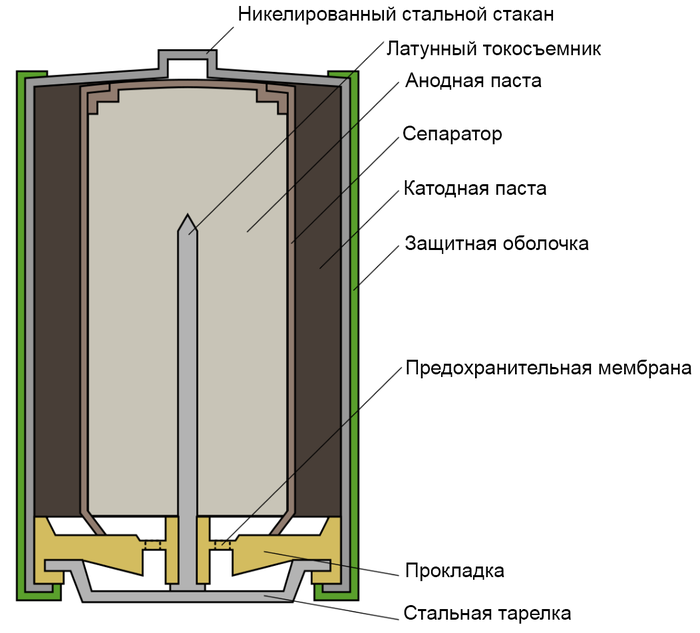
Впервые щелочные батарейки выпустила компания Eveready (ныне Energizer) в 1959г. Принцип ее работы практически идентичен принципу работы солевой батареи – анод из цинка, катод из диоксида марганца, единственное отличие в составе электролита – он не из соли аммония, как в солевой, а из раствора щёлочи, обычно гидроксида калия. И конструкция элемента отличается – она, так сказать, вывернута наизнанку по сравнению с конструкцией солевого элемента. У солевого элемента анод в виде цинкового стаканчика, заполненный катодом в виде диоксида марганца, разделенным электролитом из соли аммония, а у щелочной батареи анод в виде пасты из цинкового порошка в смеси с электролитом находится внутри катода из смеси диоксида марганца с графитом. Анод и катод разделены тонким сепаратором, пропитанным электролитом, и все это располагается в стальном корпусе. Получается, что если у солевого элемента корпус (-), а центральный токоотвод (+), то у щелочного элемента все наоборот, корпус (+), а центральный токоотвод (-).
Такая конструкция, разумеется, сделана не просто так. Выше упоминалось, что первичные гальванические элементы преобразуют химическую энергию, содержащуюся в реагентах элемента. В солевых элементах при химической реакции расходуются все реагенты, составляющие этот элемент - анод, катод, электролит. А в щелочном элементе при химической реакции расходуется только анод и катод, электролит не расходуется. Поэтому электролита там совсем мало, и освободившееся место электролита заполнено увеличенным количеством анода и катода, что значительно увеличивает электроемкость щелочного элемента. И здесь мы плавно переходим к рассмотрению преимуществ и недостатков солевых и щелочных источников питания.
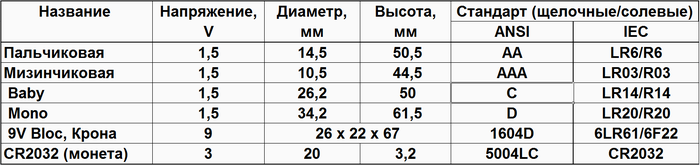
Форм-фактор распространенных гальванических элементов
Преимущества и недостатки солевых и щелочных элементов.
У солевых сейчас осталось только одно преимущество - цена. Технология производства проста и вылизана до идеала уже давным-давно, стоимость реагентов и материалов низка, поэтому себестоимость очень маленькая. Но на этом преимущества кончаются и начинаются недостатки, а именно:
Маленькая емкость. В среднем емкость солевого элемента в 3-5 меньше, чем у щелочного. К тому же это при малой и средней нагрузке, при высокой нагрузке (мощные фонари, фотоаппараты и видеокамеры) разница в емкости еще больше увеличивается и достигает 10. Т.е., к примеру, солевая батарейка питает маломощный прибор, скажем, 10 дней, а щелочная 10*3=30 дней; такая же солевая батарейка обеспечит энергий фотоаппарат со вспышкой в течение 10 минут, а такая же щелочная 10*10=100 минут.
Маленький срок хранения. У солевого элемента – 2 года, у щелочного – 7-10 лет. Срок хранения солевой батареи можно увеличить, если держать ее в холодильнике, при низкой температуре химические реакции, при которой происходит саморазряд, замедляются. Для щелочных элементов температура хранения некритична.
Узкий температурный диапазон эксплуатации. Солевые батареи вообще не могут работать при отрицательных температурах, а щелочная при -20 °С отдает такую же емкость, как солевая в режиме беспрерывного разряда при комнатной температуре.
В последние несколько лет в продаже появились новый тип элементов - литиевый. Принцип действия все так же похож на принцип солевого и щелочного элемента, но анод изготовлен из лития или его соединения. Из химии известно, что литий имеет наивысший отрицательный потенциал по отношению к остальным металлам, соответственно, он имеет наибольшее номинальное напряжение при минимальных размерах. И другие параметры тоже превосходные –очень большое время хранения (до 15 лет), исключительно малые токи саморазряда и высокая степень герметичности, хранение и работа в широком диапазоне отрицательных и положительных температур. Но цена, цена...
Некоторые советы от опытных пользователей касательно батареек.
Не надо стремиться покупать элементы известных фирм, которые на слуху благодаря навязчивой рекламе. Ведь рекламный бюджет надо отбивать, и расходы на рекламу включаются в цену товара. Да, высокотехнологичная батарейка может оказаться самой долгоиграющей, но ее цена взлетает в небеса; две же обычные батарейки по емкости спокойно перекрывают одну супербатарейку, и к тому же стоимость двух обычных оказывается дешевле, чем одной именитой. На одном сайте был проведен большой тест батареек различных фирм, там посчитали комплексный параметр цена/емкость, и в результате тестов лидером отказалась безымянная батарейка, продающаяся в гипермаркете Ашан, ее ватт мощности оказался самым дешевым, оставив далеко позади именитые фирмы. А известная история с батарейками фирмы «Космос», появившиеся в продаже несколько лет назад, покупатели, которые купили эти батарейки, с удивлением и даже некоторым шоком отмечали, что эти батарейки ничуть не хуже, а зачастую и существенно лучше грандов, при цене на порядок ниже.
Севшие солевые батарейки можно восстановить. Делается это двумя способами - обстукиванием корпуса батарейки и зарядкой (да, солевые перезаряжаются) током специальной формы. Обстукивание – самый простой способ восстановления. Суть – под ударной нагрузкой с цинкового анода стряхиваются продукты реакции, налипшие на анод и препятствующие дальнейшей реакции. Стучать надо без особого фанатизма, иначе рискуешь повредить корпус, и электролит вытечет. Перезаряжать – сложнее, здесь требуется «умная» зарядка, которая стоит дорого и не везде продается, и тоже существует риск повреждения элементов.
За пределами поста осталось много интересных элементов (воздушно-цинковые, ртутные, серебряные и т.д.), описание их категорически не влезает в отведенный объем. Но все это перепевы классического гальванического элемента, изобретенного почти 200 лет назад. Выше упоминалось, что фирмы, производящие источники тока, особых прорывов не ожидают. Но интересно же заглянуть за горизонт? И ученые уже предлагают совсем иные принципы работы источников питания для все увеличивающихся в размере и количеству носимых нами гаджетов. Перечислю некоторые научные проекты: преобразование тепла человека в электричество с помощью стеклоткани, канализирование света с помощью фотоэлектрических органических ячеек, преобразование лактатов из человеческого пота в электричество с помощью «биотатуировки». Интересно, что же из этого выстрелит?


Наука | Научпоп
9.1K поста82.5K подписчиков
Правила сообщества
Основные условия публикации
- Посты должны иметь отношение к науке, актуальным открытиям или жизни научного сообщества и содержать ссылки на авторитетный источник.
- Посты должны по возможности избегать кликбейта и броских фраз, вводящих в заблуждение.
- Научные статьи должны сопровождаться описанием исследования, доступным на популярном уровне. Слишком профессиональный материал может быть отклонён.
- Видеоматериалы должны иметь описание.
- Названия должны отражать суть исследования.
- Если пост содержит материал, оригинал которого написан или снят на иностранном языке, русская версия должна содержать все основные положения.
- Посты-ответы также должны самостоятельно (без привязки к оригинальному посту) удовлетворять всем вышеперечисленным условиям.
Не принимаются к публикации
- Точные или урезанные копии журнальных и газетных статей. Посты о последних достижениях науки должны содержать ваш разъясняющий комментарий или представлять обзоры нескольких статей.
- Юмористические посты, представляющие также точные и урезанные копии из популярных источников, цитаты сборников. Научный юмор приветствуется, но должен публиковаться большими порциями, а не набивать рейтинг единичными цитатами огромного сборника.
- Посты с вопросами околонаучного, но базового уровня, просьбы о помощи в решении задач и проведении исследований отправляются в общую ленту. По возможности модерация сообщества даст свой ответ.
Наказывается баном
- Оскорбления, выраженные лично пользователю или категории пользователей.
- Попытки использовать сообщество для рекламы.
- Фальсификация фактов.
- Многократные попытки публикации материалов, не удовлетворяющих правилам.
- Троллинг, флейм.
- Нарушение правил сайта в целом.
Окончательное решение по соответствию поста или комментария правилам принимается модерацией сообщества. Просьбы о разбане и жалобы на модерацию принимает администратор сообщества. Жалобы на администратора принимает и общество Пикабу.