Сколько надо соляной кислоты, чтобы растворить кузов ВАЗ-2104?
Пост носит исключительно юмористический характер и расчеты в нем приблизительные. Ни в коем случае не стоит его считать руководством к действию и видеть в нем серьезное исследование
Пришла мне в голову безумная фантазия. Предположим я волею судьбы стал обратно юношей и дедушка подарил мне свой древний автомобиль. В реальной жизни мне никто не дарил автомобиль, и дед, будучи одноногим ветераном ВОВ, автомобиль не имел. Но я фантазирую.
Подарили мне ВАЗ 2104. Вы спросите: "А почему именно его?". А потому что древняя четверка была моим первым автомобилем, а это как первая женщина в жизни - с ней связаны как самые лучшие воспоминания начинающего автомобилиста, так и самые ужасные, потому что этот пепелац имел свойство ломаться минимум раз в неделю.
Примерно такой был, даже цвет пожарный. Течет по олдскулам слеза.
Итак, автомобиль у меня есть, а водить я толком не умею. Ехал с такими же малолетними дебилами и сбил человека. Испугался, скрылся с места ДТП. Можно сдаться полиции, но я нехороший человек и в тюрьму не хочу. Поэтому надо избавиться от улик. Разбираю автомобиль, часть сжигаю, часть продаю (тот же двигатель), но остается самое палево - разбитый кузов. Его надо срочно утилизировать. Воспользуемся нетрадиционным методом - растворю его в кислоте. Почему так - а так изящнее, и кислоты у меня на работе хоть бассейн наливай. Возьму самую ходовую - соляную. Поэтому поиграем в безумного ученого и проведем такой же эксперимент.
В принципе, если вы знаете азы химии и базовые законы стехиометрии, то легко можете подсчитать, сколько понадобится соляной кислоты для этого черного дела. Если учесть, что салон состоит из железа (грубо буду считать так, но он состоит из стали), то для растворения 1,06 тонны железа (максимально возможная масса салона) понадобится 1,385 тонн чистого хлороводорода. Но это газ, а нам нужен его водный раствор, та самая соляная кислота, максимальная концентрация каковой достигает 36%. Стоит также учесть, что практический выход продукта реакции всегда ниже теоретического. Поэтому не будем забивать себе голову теорией, теория, мой друг, суха, но зеленеет жизни древо, как говорили немецкие классики. Поэтому будем проводить эксперимент
Для этого возьму кусок ржавой насосно-компрессорной трубы марки 30ХМА. Предположим, что вся машина сделана из этой стали
Теперь берем набор юного садиста
И зачищаем его
Чистим долго, он должен блестеть как яички у очень ленивого кота, которому нечего делать, до чистого металла.
Примерно так. Глянец нам не нужен, главное, чтобы металл был чистым, без окалины и ржавчины.
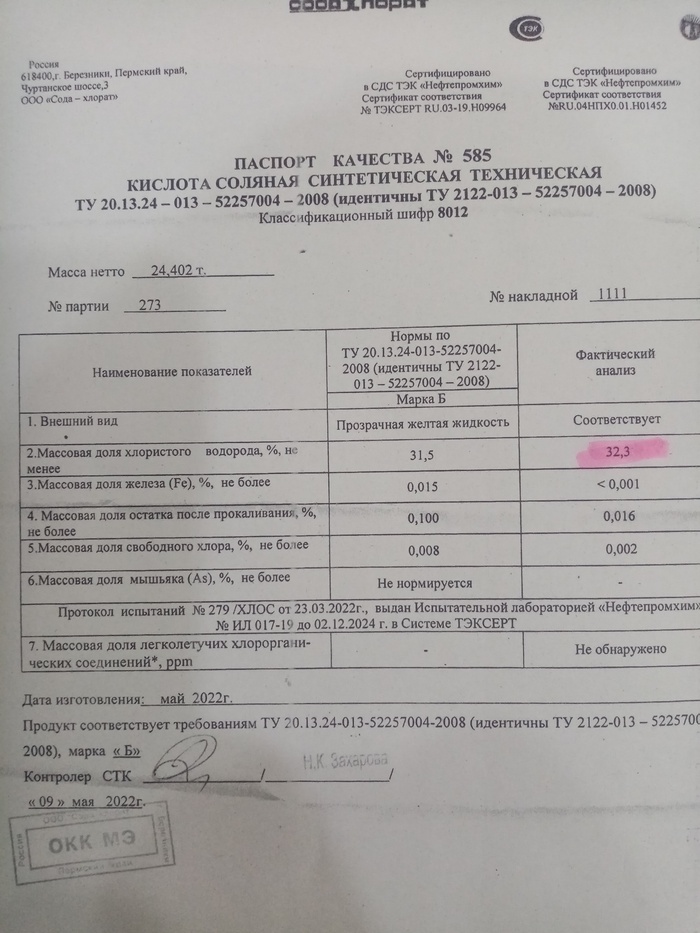
Теперь возьмем соляную кислоту.
В паспорте качества концентрация указана. Но я играю в mad scientist, мы не доверяем заключениям и проводим свою с помощью старого доброго кислотно-щелочного титрования. Наливаем в колбу 40 мм дистиллированной воды
И капаем туда несколько камель спиртового раствора фенолфталеина
Затем берем пипетатор и набираем 0,5 мл кислоты
Объем абсолютно неважен, важна масса. Можно взять хоть миллилтр, да хоть десять, все это просто приведет к перерасходу титранта. Взвешиваем массу кислоты на аналитических весах
И титруем 1Н (1М) раствором гидроксида натрия до появления малиновой окраски
Смотрим объем, затраченный на титрование
После чего делаем расчет
Ну не совсем совпало, хотя очень близко. Виной мои кривые руки и погрешность. Пусть концентрация кислоты будет как в лабораторном заключении - 32,3%.
Теперь беру кусок трубы, который так долго зачищал
И взвешиваю на аналитических весах
И подвешиваю на нитке так, чтобы он не касался ни стенок, ни дна
Начинается активная реакция, водород так и прет
И забываю его на сутки (в реальности их оказалось двое). Чтобы дело пошло быстрее, баночку ставлю в водяную баню при температуре 50 градусов. Старина Вант-Гофф врать не будет, как и Сванте Аррениус (смотрим правило Вант-Гоффа и уравнение Аррениуса). Поверхность периодически промывалась водой, а кислота перемешивалась стеклянной палочкой
Через двое суток наш образец представляет вот такое зрелище. Кислота потемнела, в жидкой фазе черная взвесь, на дне осадок. Реакция прекратилась. Возможно, что произошла пассивация металла. Промоем металл и опустим еще раз в кислоту
Ничего не меняется, реакция не идет. А теперь опустим в свежую
Реакция пошла вновь. Из чего делаю вывод, что кислота отработала свое. Хотя хлороводорода там еще много. Вытаскиваю металл, промываю и высушиваю
Взвешиваю
Образец похудел на 5,5988 грамма. Маловато, я ожидал большего.
Итого, у нас 1 литр данного образца кислоты способен растворить 27,994 грамма. Поэтому чтобы растворить 1060 килограмм стали, нам нужно целых 37,86 м3 кислоты. Если учесть, что 1 м3 технической соляной кислоты при закупке у нас стоит 12 тысяч рублей, для утилизации кузова потребуется 454.320 рублей. Сумма неплоха, но если учесть, что покупаешь несколько лет свободы - то не так уж и велика. Вывод: не совершайте ДТП, не придется разоряться.
Теперь остался еще один вопрос - куда деть стекло. А все туда же - концы в воду, точнее в кислоту. Но это уже будет вопрос следующего эксперимента
PS. Боже мой, какой ерундой я занимаюсь
Дополнение:
Итак. Решил я уточнить ваши расчеты и нашёл ПРЕЙСКУРАНТ № 27-07-36 "ОПТОВЫЕ ЦЕНЫ НА ДЕТАЛИ И УЗЛЫ К АВТОМОБИЛЬНОЙ ТЕХНИКЕ И АВТОПОГРУЗЧИКАМ" от 1989 года. В нём есть деталь 2104-5000010 "Кузов в сборе обитый" весит 480 кг. Для растворения потребуется 17.15 м3. А ещё есть деталь 2104-5000014 "Кузов в сборе окрашенный без обивки" массой 282 кг. Для него нужно будет всего 10.07 м3 раствора кислоты.















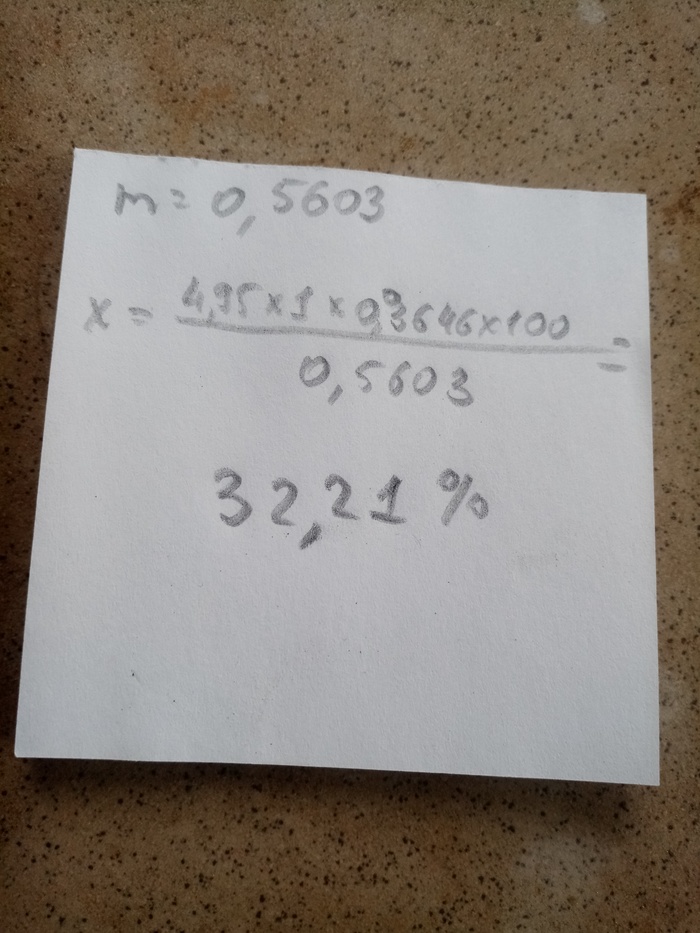









Лига упоротых расчетов
370 постов6.5K подписчика
Правила сообщества
Лига занимается странными веселыми подсчетами на основании уже имеющихся в общем информационном доступе знаний. Расчеты - ради лулзов и хорошего настроения. Не нудите сами и не занудничайте в адрес других, играть в Шелдона Купера хорошо до определенного предела.