Молекулярная биология. Работа РНК-полимеразы. Часть 4
Продолжение постов о молекулярной генетике. (Эта часть получилась большой и менее красочной, я бы даже сказала, как задача со звездочкой)
Существует несколько моделей работы РНК-полимераз. Тут я хочу рассказать о двух моделях, которые наилучшим образом подтверждают экспериментальные исследования. Следует сказать, что мы переходим к рассмотрению следующей стадии транскрипции - элонгации, "осмысленному" движению РНК-полимеразы по ДНК и синтезу мРНК.
Что вообще требуется для работы РНК-полимеразы:
1) обязательным условием является наличие ионов Mg (2+), входящих в состав каталитического центра РНК-полимеразы.
2) рибонуклеозид-трифосфаты (АТФ, ЦТФ, УТФ, ГТФ)
3) и конечно, наличие самой ДНК.
Скорость движения РНК-полимераз измеряется в количестве присоединенных нукледотидов в секунду, так для полимеразы бактериофагов способны элонгировать in vitro растущую цепь РНК со скоростью 200–400 нт/с. Бактериальные РНК-полимеразы транскрибируют ДНК с промежуточной скоростью – 50–100 нт/с, эукариотические РНК-полимеразы элонгируют цепи РНК in vivo со скоростью ~20–30 нт/с. (тут прослеживается некоторая корреляция с размерами и количеством СЕ, ходящих в состав РНК-полимераз)
Основные черты структуры тройного комплекса, осуществляющего элонгацию цепей РНК, консервативны у всех ДНК-зависимых РНК-полимераз. В каждом элонгирующем комплексе имеются каталитический центр, одноцепочечная область ДНК-матрицы, а также несколько сайтов связывания ДНК и РНК. Для реализации принципа комплементарности при построении растущей цепи РНК участок матричной ДНК, входящий в состав комплекса, находится в расплавленном состоянии, и одна из его цепей служит матрицей при транскрипции. Этот участок ДНК, называемый транскрипционным пузырьком, или транскрипционной сферой, контактирует с каталитическим центром РНК-полимеразы. По обеим сторонам транскрипционного пузырька имеются участки ДНК, которые при перемещении фермента вдоль матрицы подвергаются плавлению (расплетанию) и повторному отжигу, в результате которого восстанавливается исходная структура ДНК. Считается, что этот процесс не является каталитическим, протекает самопроизвольно и связан с особенностями структуры РНК-полимеразы как таковой.
1. Модель прерывистого "червеобразного" движения
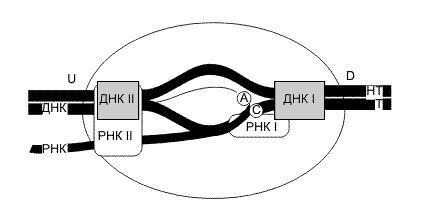
В 1992 г. М. Чамберлин с сотрудниками разработали модель элонгации РНК, в которой постулировалось, что процессы транслокации РНК-полимеразы вдоль ДНК и присоединение нуклеотидов к растущей цепи РНК в активном центре фермента разделены во времени. То есть простым языком можно сказать, что РНК-полимераза стоит из 2х частей, соединенных сжимаемой "пружиной". Существует 2 сайта связывания полимеразы ДНК: Сайт 1 в передней части по отношению к направлению транскрипции, а сайт 2 в передней.
В соответствии с предложенной моделью, молекула РНК- полимеразы перемещается вдоль ДНК наподобие гусеницы: когда один из сайтов связывания ДНК фиксирован, другой может двигаться вперед.
В данной модели гибрид РНК/ДНК не вносит вклад в стабильность транскрипционного комплекса, а растущая цепь РНК удерживается благодаря наличию двух сайтов связывания РНК-полимеразы с РНК: участок прочного связывания (1) (5' конец) и слабого связывания (2) (3' конец).
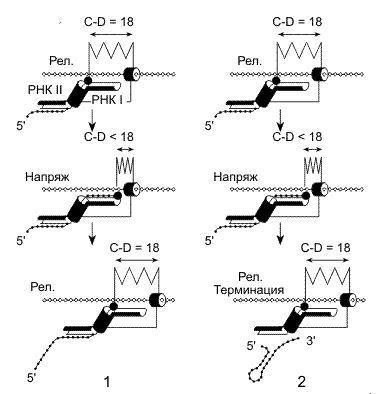
Согласно предложенной модели элонгация цепей РНК представляется в виде циклического процесса.В начале цикла каталитический центр молекулы РНК-полимеразы располагается у задней границы РНК-связывающего сайта 1 в соответствии с положением 3'-ОН-конца РНК.Последовательно присоединяя нуклеотиды к растущей цепи РНК, каталитический участок перемещается относительно РНК-связывающего сайта I и в конце концов заполняет этот сайт десятью нуклеотидами вновь синтезированного участка РНК. Во время этой фазы элонгации ДНК-связывающий сайт 2 остается фиксированным на ДНК, тогда как ДНК-связывающий сайт 1 перемещается вперед синхронно с каталитическим участком на десять нуклеотидов. В конце фазы добавления нуклеотидов ДНК- и РНК-связывающие сайты 2 фиксируются на своих лигандах, а ДНК-связывающий сайт 1 переносится вперед на десять нуклеотидов в новое фиксированное положение. Это перемещение освобождает РНК-связывающий сайт 1, делая его готовым к повторению цикла транслокации.
На рисунке показаны ДНК, синтезируемая РНК, а диагональными линиями - нарастающее напряжение белкового остова РНК-полимеразы.
При дальнейших исследованиях оказалось, что перемещение тройного комплекса вдоль транскрибируемой ДНК не всегда скачкообразно.
Большую часть транскрибируемых ДНК молекулы РНК-полимеразы проходят монотонно, регулярно присоединяя к растущим цепям РНК нуклеотид за нуклеотидом. Прерывистая, скачкообразная элонгация РНК имеет место лишь на участках матричной ДНК, в которых происходит задержка транскрипции или ее прекращение. Задержками могут быть последовательности-палиндромы, образующие шпильку в РНК , а так же последовательности, богатые урацилом.
2. Современное представление элонгирующего комплекса.
Дальнейшие исследования уточнили геометрию тройного комплекса и структуру каталитического центра. В ходе обширных биохимических и генетических исследований локализован активный центр РНК-полнмеразы, а также участки связывания нуклеиновых кислот, необходимых для стабильности элонгационного комплекса.
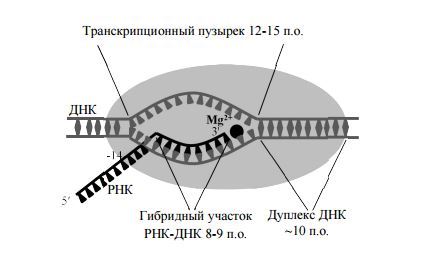
Выяснилось, что три остатка аспарагиновой кислоты в консервативном у всех многосубъединичных РНК-полимераз мотиве NADFDGD самой большой субъединицы (бэта') хелатируют каталитический нон Mg (2+). Субъединицы бэта’ и бэта формируют три сайта связывания: 1) сайт связывания дуплекса ДНК из 10 пар оснований (п.о.) перед активным центром. 2) сайт связывания гибридного участка РНК-ДНК длиной 8—9 п.о., образующегося в "транскрипционном пузырьке" из 12—15 п.о. расплавленной ДНК. и 3) сайт связывания одноцепочечного участка РНК. удаленного на 8—14 нуклеотидов от З'-конца РНК.
Выяснилось, что в элонгационном комплексе передний (по ходу движения РНК-полимеразы) дуплекс ДНК располагается в основном канале между субъединицами бэта' и бэта. Прямые контакты РНК-полимеразы с участком ДНК из ~10 п.о. образуют функциональный сайт связывания ДНК. Подвижный домен бэта', названный “зажимом” (clamp), удерживает ДНК в
канале. Каталитический центр РНК-полимеразы находится рядом с точной расплетания ДНК. Полипептидная петля на бэта СЕ препятствует прохождению двунитеой ДНК в активный центр, и, по-видимому, играет важдую роль в плавлении ДНК, тут цепь ДНК изгибается под углом примерно 90 градусов, освобождая место для формирования гетородуплекса ДНК-РНК. Сам дуплекс находится в канале, образованном бэта и бэта' СЕ. После синтеза 9 нуклеотидов цепь РНК отделяется от ДНК, параллельно с этим восстанавливается дуплекс ДНК, способствующий вытеснению РНК.
В ходе матричного синтеза РНК-полимераза катализирует нуклеофильную атаку 3'- гидроксила растущей цепи РНК на альфа-фосфат поступающего НТФ. в результате чего происходит включение очередного нуклеотида в цепь РНК и высвобождение пирофосфата. Активный центр фермента содержит участок связывания З'-конца РНК (i-сайт) участок связывания поступающего НТФ (i+1-сайт). За образованием фосфодиэфирной связи следует транслокация вновь образованного З’-конца РНК из i+1-сайта в i-сайт. при этом i+1-сайт освобождается для поступления нового НТФ (посттранслокационное состояние). Вместе с этим происходит разъединение пары оснований в переднем дуплексе ДНК. образование пары оснований в заднем дуплексе и разъединение последней пары оснований в гибриде РНК-ДНК.
В данном представлении становится возможным движение фермента в обратную сторону.
Осцилляции РНК-полимеразы назад и вперед по гибриду РНК-ДНК:
• Приводят к освобождению 3-конца РНК из гибрида
• Освобожденный нуклеотид может быть отщеплен
• Так преодолеваются «трудные» участки транскрипции – сигналы паузы и сигналы остановки, исправляются ошибочно встроенные нуклеотиды
Этот пост получился тяжелым, простите, но, надеюсь, это улучшит ваше понимание вопросов.
Спасибо за внимание.
подробнее в статье: С. А. ПРОШКИН, Г. В. ШПАКОВСКИЙ ЯДЕРНЫЕ РНК ПОЛИМЕРАЗЫ I, II И III: СТРУКТУРА И ФУНКЦИИ // Успехи биологической химии, т.45, 2005, с.269-306


Наука | Научпоп
7.7K поста78.5K подписчика
Правила сообщества
Основные условия публикации
- Посты должны иметь отношение к науке, актуальным открытиям или жизни научного сообщества и содержать ссылки на авторитетный источник.
- Посты должны по возможности избегать кликбейта и броских фраз, вводящих в заблуждение.
- Научные статьи должны сопровождаться описанием исследования, доступным на популярном уровне. Слишком профессиональный материал может быть отклонён.
- Видеоматериалы должны иметь описание.
- Названия должны отражать суть исследования.
- Если пост содержит материал, оригинал которого написан или снят на иностранном языке, русская версия должна содержать все основные положения.
Не принимаются к публикации
- Точные или урезанные копии журнальных и газетных статей. Посты о последних достижениях науки должны содержать ваш разъясняющий комментарий или представлять обзоры нескольких статей.
- Юмористические посты, представляющие также точные и урезанные копии из популярных источников, цитаты сборников. Научный юмор приветствуется, но должен публиковаться большими порциями, а не набивать рейтинг единичными цитатами огромного сборника.
- Посты с вопросами околонаучного, но базового уровня, просьбы о помощи в решении задач и проведении исследований отправляются в общую ленту. По возможности модерация сообщества даст свой ответ.
Наказывается баном
- Оскорбления, выраженные лично пользователю или категории пользователей.
- Попытки использовать сообщество для рекламы.
- Фальсификация фактов.
- Многократные попытки публикации материалов, не удовлетворяющих правилам.
- Троллинг, флейм.
- Нарушение правил сайта в целом.
Окончательное решение по соответствию поста или комментария правилам принимается модерацией сообщества. Просьбы о разбане и жалобы на модерацию принимает администратор сообщества. Жалобы на администратора принимает и общество Пикабу.