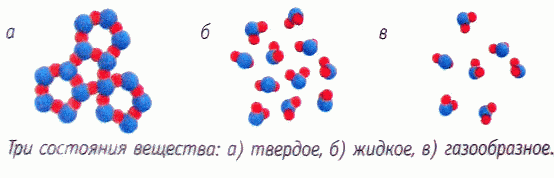Физика фазовых переходов
В честь окончания года, а так же моего маленького праздника
Я решил наконец написать пост, который обещал 11 дней назад.
Так вот: жидкие кристаллы. А, нет. Я хотел было написать сразу о них, но необходима предварительная подготовка. Она заняла целый пост, так что жидкие кристаллы подождут еще чуть-чуть.
Где-то в 7 классе вас научили, что есть
А кому-то повезло иметь физика, который еще и добавил: а еще есть плазма.
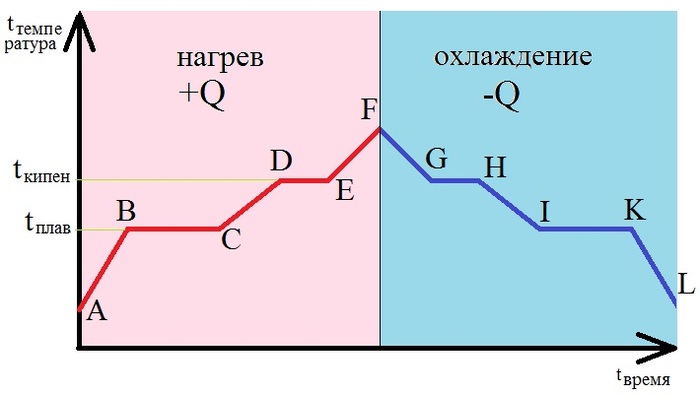
И вам сказали: если передать теплоту твердому телу, оно нагреется, потом расплавится, потом нагреется образовавшаяся жидкость, она испарится, и вы получите газ.
И такая картина всех устраивала примерно до 11 класса. Потом вам сказали, что вас обманули (не все, думаю, это слышали, ибо к 11 классу дай бог четверть еще воспринимает что-то на физике). Вам показали сухой лед: твердое тело, которое переходит сразу из твердого состояния в газообразное, минуя жидкость.
Как это возможно?
Давайте сначала обсудим простую воду. На вопрос: при какой температуре кипит вода? Вопрошающий скорее всего получит недоуменный взгляд и ответ: 100 градусов Цельсия. Но при этом все почему-то уверены, что в горах она кипит при температуре меньшей, чем 100 градусов. Чем отличаются горы от равнин? Правильно - высотой, а значит и атмосферным давлением. То есть температура кипения воды уменьшается с давлением. А что, если сделать давление тогда совсем маленьким?
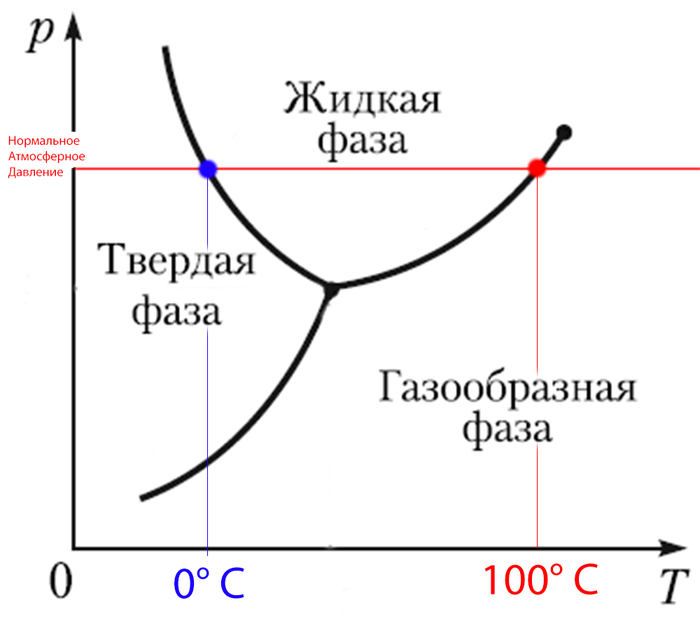
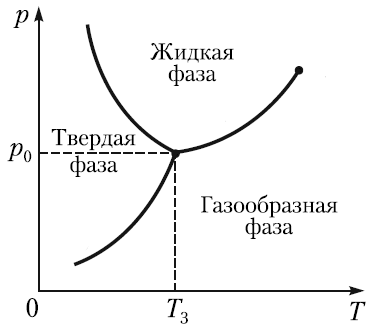
Давайте посмотрим на эту диаграмму
Это называется фазовая диаграмма, на ней изображена зависимость давления от температуры для вещества. Как легко понять, каждой паре давление-температура соответствует свое агрегатное состояние. Для воды при атмосферном давлении мы находимся на красной линии.
Как вы видите, при температуре больше 100 градусов мы получаем газ, меньше 0 - твердое вещество, посередине - жидкость. Начнем уменьшать давление. Первая аномалия, с которой мы столкнемся - тройная точка воды.
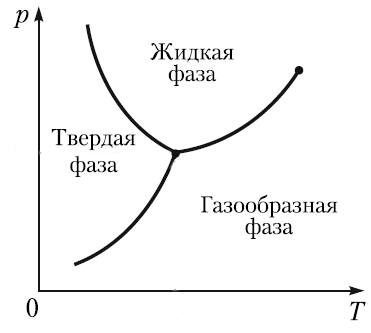
В этом месте встречаются разу 3 фазы. Тройная точка воды находится при температуре 273,16 К (0,01 °C) и давлении 611,657 Па (0,006 атмосферы). Вот так это выглядит (увы, не на примере воды, но вода делает ровно так же)
Опустив давление еще ниже, мы попадем в область, в которой газ переходит в твердое состояние минуя жидкое. Как я уже говорил, для разных веществ это давление разное, и если для воды такое давление составляет тысячные атмосферного, то для сухого льда (CO2) это давление составляет 5,2 атмосферы, то есть при 1 честной атмосфере мы находимся ниже тройной точки, жидкой фазы у сухого льда нет.
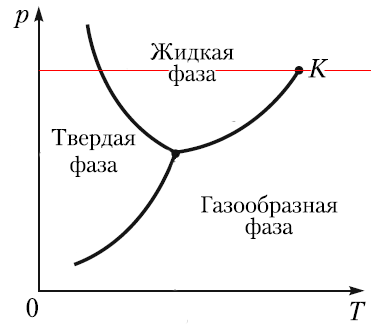
Так, это мы сходили ниже атмосферного давления, а что будет выше него? Мы наткнемся на новую особенность, называемую критической точкой.
Начиная с нее, жидкая и газообразная фаза неразличимы.
Что, думаете этой общей фразой я и обйдусь? Неа. Хотя объяснение тривиальное.
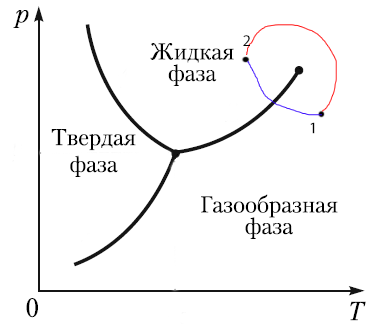
Что происходит на самих черных линиях на фазовой диаграмме? Там одновременно сосуществуют 2 состояния одного вещества (ну для воды: вода и лед, вода и пар). И их визуально легко различить. С точки зрения физики это легко заметить оптически: вещества далеко от фазового перехода оптически прозрачны(ну, в каком-нибудь диапазоне, хоть бы и рентгеновском), в момент перехода становятся непрозрачны, а после перехода снова прозрачны. Думаю, все видели, как мутнеет лед, когда он тает. Вот это почти из этой оперы. Вот так можно определить, что переход произошел. Резкое падение пропускания излучения. И вот до критической точки мы его видим, а после - нет.
То есть двигаясь по синей линии, мы в какой-то момент увидим резкое падение интенсивности пропускаемого света, а по красной - нет.
Конечно, это далеко не полная картина фазовых переходов. Еще есть переходы между различными фазами внутри твердого тела, есть метасостояния, о которых я еще поговорю в следующий раз, можно о плазме ещё поговорить будет.
Но на сегодня все, всем спасибо за внимание.