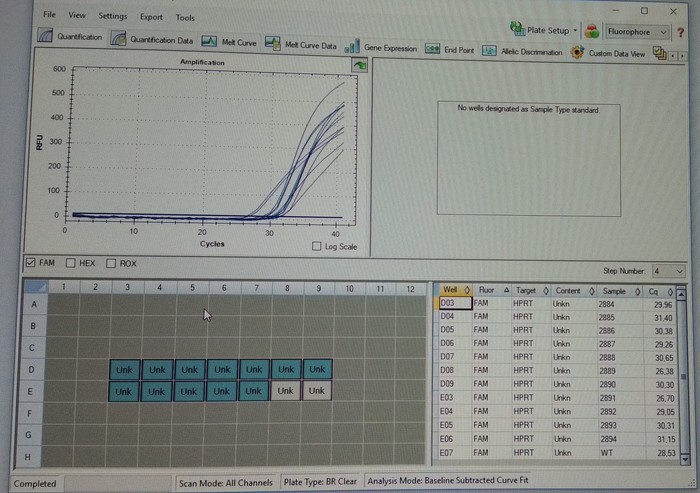
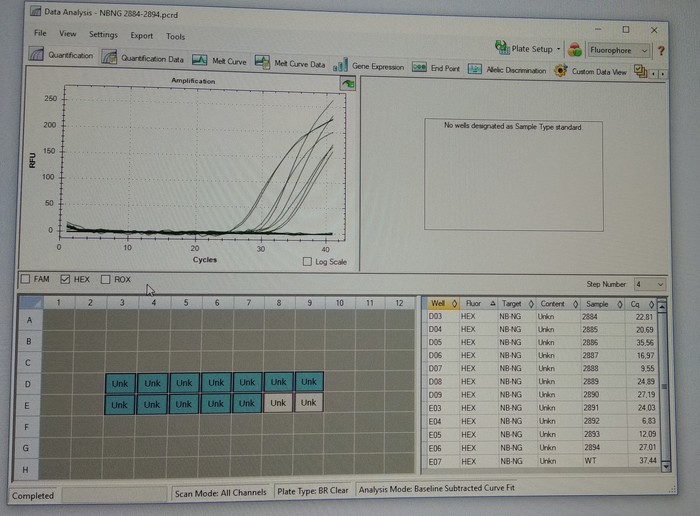
qPCR - полимеразная цепная реакция в реальном времени эффективный метод определения экспрессии генов, на основе амплификации исходного объёма мРНК. Для выбора генного сектора амплификации требуется пара олигонуклеотидных праймеров 3'-Front и 5’-Reverse, которые помечают участок амплификации. Этот материал расскажет как без особого опыта и знаний создать дизайн праймеров и заказать их синтез.
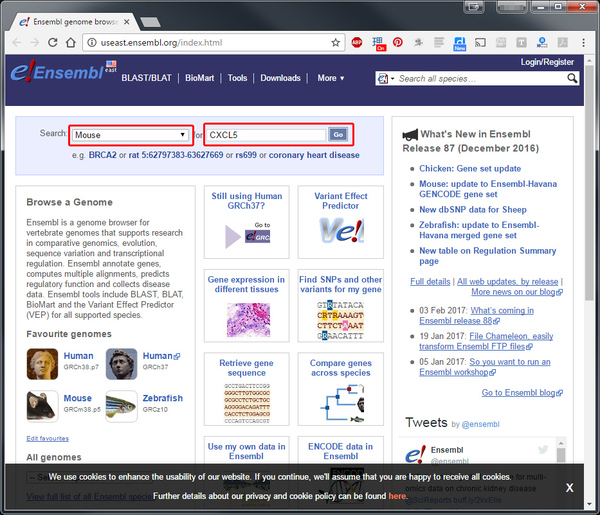
http://useast.ensembl.org/index.html
Для начала нужно определить индекс транскрипта для выбранного гена. В этом примере мы рассмотрим ген кодирующий протеин CXCL5 так же нужно выбрать биологический вид, с которым мы работаем, зависит, откуда вы извлекли вашу РНК, в данном примере это мышь CL57BL6. Теперь нажмите "Go" для поиска.
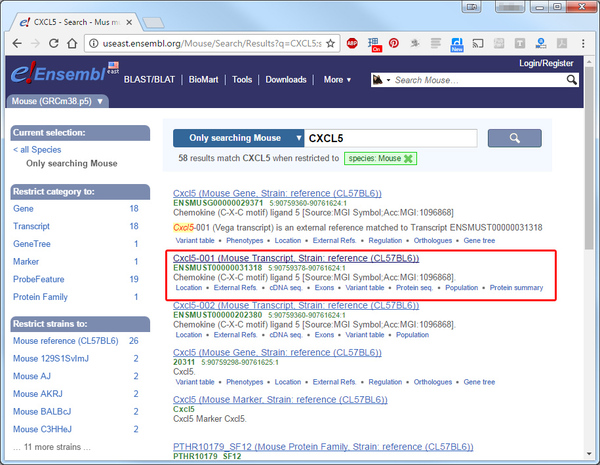
И из полученного списка важно выбрать не сам ген, он обычно идёт первым в поиске, а именно транскрипт.
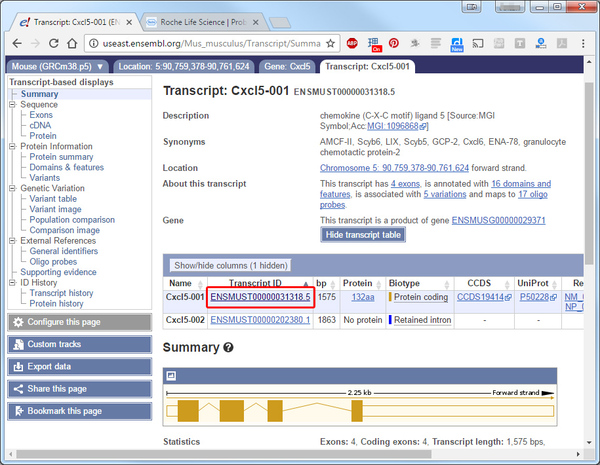
Теперь нажимите на транскрипт в полученном списке нужно скопировать Transcript ID в абсолютном большинстве проектов нас интересует протеин кодирующий Protein coding, не содержащий интрона в этом примере Transcript ID следующий: ENSMUST00000031318.5
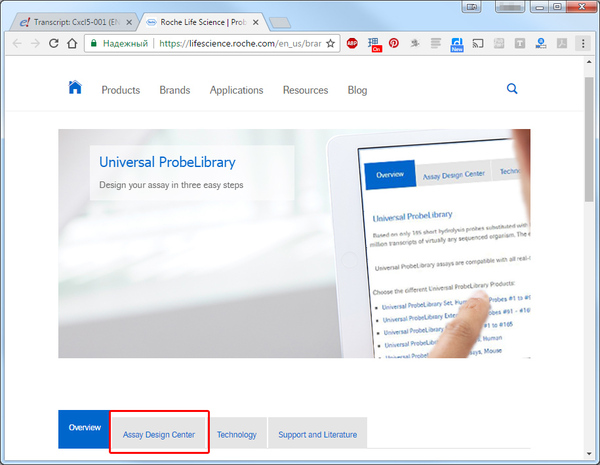
https://lifescience.roche.com/en_us/brands/universal-probe-library.html
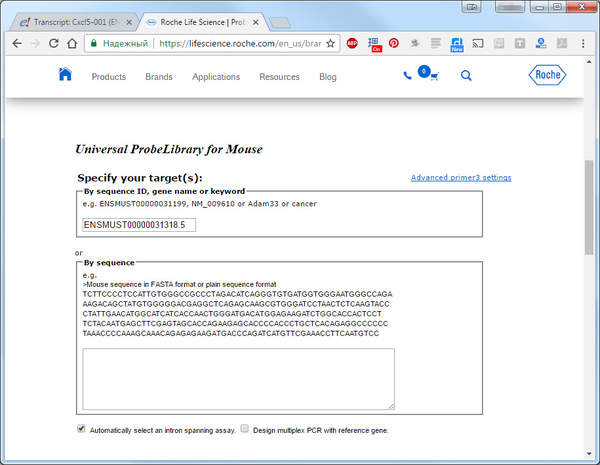
Дальше нам на основании полученного Transcript ID нужно определить нуклеотидную последовательность сделать это можно здесь на сайте Roche LifeScience в онлайн системе Universal Probe Library.
Нажмите Assay Design Center и начните с выбора целевого организма. Опять же в данном случае это мышь Mus musculus (Mouse). Теперь впишите в строку Specify your target(s) Transcript ID полученный выше и нажмите Enter или копку Design.
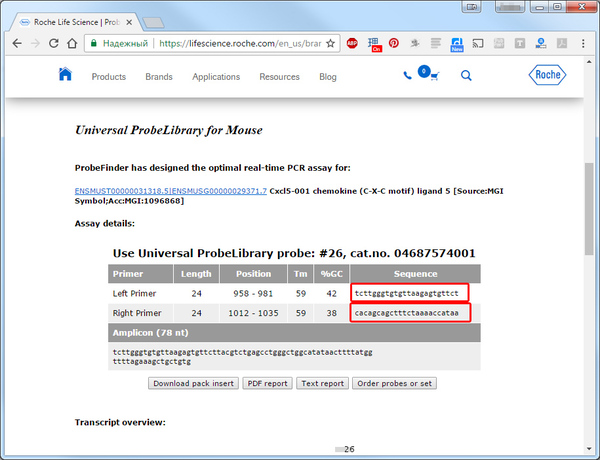
Собственно вот и результат:
CXCL5 3’ tcttgggtgtgttaagagtgttct
CXCL5 5’ cacagcagctttctaaaaccataa
В системе Universal Probe Library прямой праймер 3’ называется left primer, а обратный 5’ right primer, но не суть. Собственно это готовая последовательность qPCR праймеров для синтеза. Чуть ниже сиквенса можно посмотреть карту транскрипта относительно всего гена.
Если вы получили предупреждение об отсутствии интронной сепарации в дизайне праймера, обязательно проведите цикл обработки ваших РНК образцов ДНКазами, для полной фрагментации остаточной ДНК, так как без интронного разделения праймеры могут амплифицировать как cDNA так и обычную ДНК, что может сильно повлиять на конечный результат. Обрабатывать выделенный образец РНК, ДНКазами нужно сразу после извлечения и, разумеется, до синтеза cDNA иначе ДНКазы разберут и её.
Собственно с первым этапом определения Transcript ID можно было бы особенно не заморачиваться, а сразу ввести интересующий нас ген в Universal Probe Library, но тут можно допустить ошибку. Дело в том, что Universal Probe Library предлагает самые разные варианты транскриптов с куда меньшим объёмом сопровождающей информации, закажешь по ошибке не кодирующий или просто не тот конструкт, а потом будешь гадать, почему амплификация не происходит и вместо результатов, qPCR показывает шум. Мелкая ошибка или невнимательность, которая может стоить месяцев работы впустую.
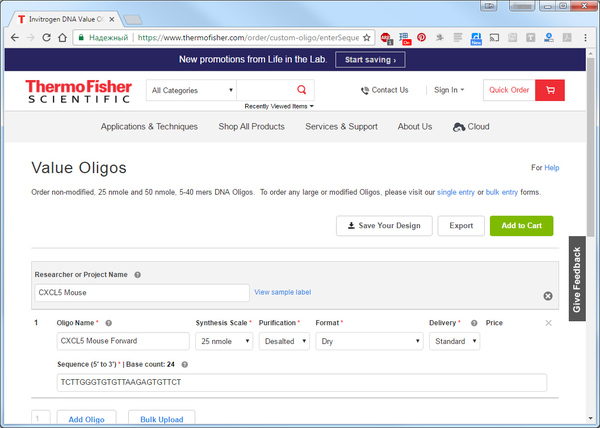
Итак, осталось заказать нуклеотидную последовательность. Фирм которые предоставляют такие услуги множество, выбор часто зависит от того с кем у вашей лаборатории заключён контракт на обслуживание или если на кампусе есть олигонуклеоитидный сиквенсер. Я обычно заказываю через сайт Thermofisher
https://www.thermofisher.com/order/custom-oligo/enterSequences
Всё что нужно это указать название вашего гена, использовать можно только буквы и цифры. Затем нужно вписать название олигонуклеатидной цепи и указать нуклеатидную последовательность. Затем нужно нажать Add Oligo и повторить процесс для обратного праймера. Осталось нажать Add to cart и перейти к оплате. Цена за одну последовательность 5$ при условии, что используется объём в 25 nmole, стандартный режим очистки и доставка в лиофилизированном виде, хотите уже готовый к использованию праймер можно доплатить ещё около 5 долларов и получить готовое разведение, но RNAse free water стоит дешево и лучше разводить праймеры самому. К тому же лиофилизат, хранится намного дольше.
Разумеется, это полностью автоматический режим синтеза праймеров для qPCR, при желании и понимании того как работает процесс амплификации вы можете выбрать другой фрагмент создать свой собственный праймер с интронной сепарацией, протестировать несколько вариантов праймеров с вашим qPCR оборудованием, и так далее для этого существует масса программного обеспечения например https://www.ncbi.nlm.nih.gov/tools/primer-blast/, но это тема другого большого поста. Этот гайд больше для тех, кому нужно готовое решение для немедленного практического применения. Определение правильного сиквенса можно опустить и сразу перейти к заказу последовательности, если вы копируете праймеры из уже опубликованной статьи, однако и тут могут быть подводные камни, не всему что опубликовано в научных журналах можно безоговорочно доверять.
Удачных амплификаций и чистых результатов.