Российские химики разработали соединения, запускающие самоуничтожение раковых клеток
Химиотерапевтические препараты, применяемые для лечения раковых заболеваний, токсичны. Они губительны не только для больных, но также и для здоровых клеток.
Фото: https://наука.рф
Исследователи из ИОФХ им. А.Е. Арбузова и НОЦ Инфохимии разработали новые соединения, которые действуют на раковые клетки точечно, запуская их саморазрушение, и не затрагивают здоровые.
Ученые синтезировали девять молекулярных структур, из них отобрали три наилучшие соединения, выявленные в ходе сравнения при воздействии на клетки рака шейки матки.
По информации Involta.media, при этом клеткам печени и эритроцитам удалось сохранить жизнеспособность.
Данные исследования опубликованы в журнале Bioorganic Chemistry.
Немного ветеринарной лаборатории
Так-с, судя плюсованию пары комментов - народу вкатил прекрасный микромир, за которым можно понаблюдать в микроскоп, поэтому ваш покорный слуга, по совместительству врач-лаборант для , решил запилить небольшой (ага, совсем небольшой) пост про свою работу, заодно кто-то может не только услышит, но и увидит, да кто эти ваши эритроциты такие, что они вообще делают и нафига нужны.
Коротко про работу (что делаю именно я) - крашу стекла кровью, пялю в микроскоп, слушаю музыку, ругаюсь с анализаторами и катаюсь на стуле по своему маленькому плану обливиона между этими самыми анализаторами и микроскопом. Попутно можно посмотреть мочу на наличие различных кристаллов, клеток и микрофлоры.
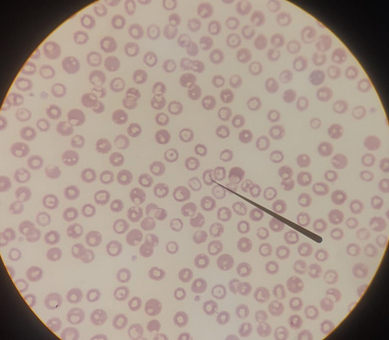
Ладно, приступим, первой пойдет кровь, а с ней и самые известные клетки - эритроциты, красные клетки крови. Розовые кружочки, напоминающие бублик - это они и есть. Кровь собачья, у кошек эритроциты будут поменьше, более равномерно прокрашены. По форме они в виде двояковогнутой линзы, но проще представить себе детскую ватрушку, где область для приземления попца расположена ровно по центру продольного сечения, и как не переворачивай - не ясно, где верх, а где низ, а значит можно плюхнуться с любой стороны. А нафига оно такой формы? Все просто - площадь полезная больше по сравнению с диском, а в мелких сосудах еще можно и сложиться как-нибудь интересно. Зачем площадь? Чтобы прицепить кислорода, да побольше, с этим справляется гемоглобин, который его умеет цеплять. А чтобы гемоглобином затариться побольше, нужно выкинуть что-нибудь ненужное. Например ядро. Которое в процессе развития в костном мозге они благополучно выбрасывают за ненадобностью.
Глазастые, думаю, могут заметить, что некоторые эритроциты имеют небольшую неокрашенную дырку, а некоторые - лишь узенький окрашенный обруч. Песель был не очень здоров, и не всем эритроцитам достался гемоглобин, его содержание в клетках снижено. Ну и плюсом они располагаются часто под некоторым углом и тонкая часть перекрывается бортиком.
Если по какой-то причине возникла проблема с эритроцитами (разрушаются в кровотоке, не созревают вообще или гемоглобин не синтезируется), то это состояние называют анемией, и вариантов анемий - довольно много. Например гемолитическая (разрушение), апластическая (клетки не создаются), железодефицитная (гемоглобин не делается, ибо нет железа). И еще уйма других.
А еще эритроциты могут менять размер, форму, иметь внутриклеточных паразитов, и еще дофига всего.
Ладно, поехали дальше, белые клетки крови, лейкоциты.
Часть иммунной системы, крайне не любят всяких непонятных залетных, имеют полные права на насилие в организме. Гораздо меньше, чем эритроцитов, тусуются по всему организму. Несколько видов, и все выполняют свои задачи. При этом есть еще и подвиды, которые выполняют более узкие задачи. Базово в крови выделяются гранулоциты (нейтрофилы, эозинофилы и базофилы) и агранулоциты (моноциты и лимфоциты). Что характерно, у песелей и котелей лапки базофилы встречаются довольно редко.
Нейтрофилы - основная популяция, обычно занимается неспецифическим ответом, их много, стукают больно, им не особо важно, кого стукать.
Эозинофилы с базофилами - токсичные ребятки, в прямом смысле, могут толпой устроить химическую атаку какому-нибудь паразиту, так же обычно активные участники аллергических реакций.
Моноциты - обычно в крови они транзитом, пока не доберутся до тканей (например альвеол), где превращаются в макрофагов. Жрут всё, жрут всех. Иногда даже своих. И крайне здоровые.
Лимфоциты - этих кадров много подвидов, отвечают за специфический иммунный ответ. С новой угрозой сперва толком ничего сделать не могут, сперва им нужно понять, куда воевать, но когда раскачаются и обучатся - тогда колесо репрессий иммунной системы начинает набирать обороты и на этот самый маховик наматывает всех, кому не повезло оказаться в списках. Кстати, вакцинация имеет смысл именно такой - показать отличительные признаки того, кого на этот маховик наматывать.
Среди лимфоцитов следует отдельно выделить NK-лимфоциты (в норме их немного), которые имеют своеобразную систему "свой-чужой", и если организм признает клетку "чужой", например при заражении вирусом, либо она не дает ответ "свой" (например, онкология) - разбираться они не будут, как и дожидаться, пока возникнет специфический ответ.
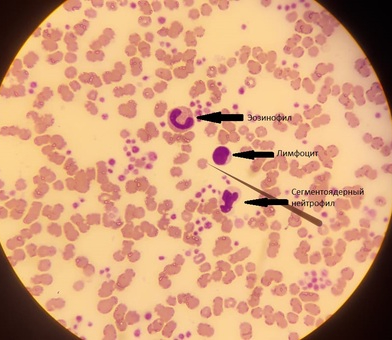
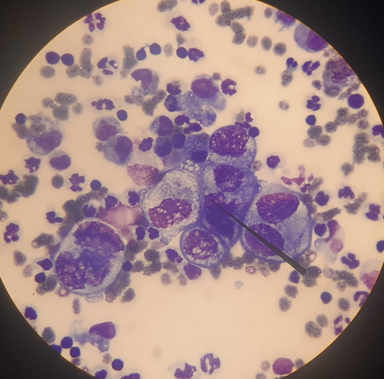
На фото - троица лейкоцитов в окружении эритроцитов и тромбоцитов. Тут, кстати, кровь кошки.
Но не все же может быть так хорошо?) Думаю, во время ковида многие услышали про такую штуку, как цитокиновый шторм. Если очень образно, то лимфоциты начинают раскручивать маховик репрессий, от этого получают удовлетворение, другие клетки решают их не тормозить и чем выше обороты - тем сильнее они продолжают раскручивать, и под раздачу попадают уже вообще все подряд. Но это в основном у человеков, насчет животных не уверен, есть ли подобная реакция.
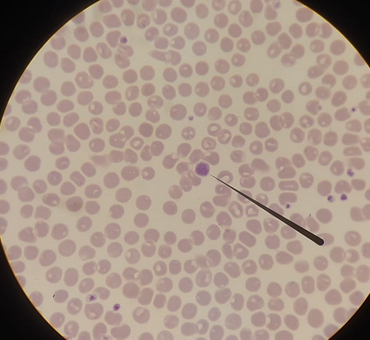
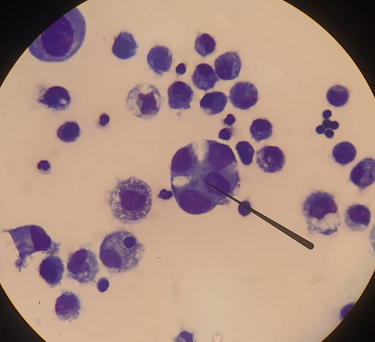
Так-с, кто там из троицы остались? А, точно, тромбоциты. Эти клетки... Эй! Положи микроскоп! Ну ладно, ладно, это не клетки, не душни. Тромбоциты по сути не клетки, а лишь куски клетки, которая зовется мегакариоцитом. От нее отваливаются кусочки, которые и представляют из себя тромбоциты. Суть этих клеток - плавать в кровотоке, и как только появляется какой-либо из активаторов свертывания - активироваться, становясь чем-то похожими на Братскую Луну с ее щупальцами из Dead Space, и благодаря этому замечательно прилепляться к поверхностям, попутно цепляя другие тромбоциты. Когда их накапливается довольно много, они наматывают на себя попутно и все остальные клетки, которым не повезло оказаться в толпе тромбоцитов. И вот эта вся куча мала должна застрять в идеале в дырке, которой быть не должно. На фото с лейкоцитами можно увидеть, что некоторые (мелкие, меньше эритроцита, фиолетовые шарики) уже друг с другом сцепились. У кошек они вообще активируются очень легко и практически мгновенно. Кстати, у этого пациента их много, в норме их в 2-3 раза меньше. А на фото ниже - макротромбоцит, размер сопоставим с эритроцит (т.е. особо крупный, но ему все равно до мегакариоцита как до Луны на тракторе)
Из приколов, которые они могут сотворить - тромбозы (привет тромбоэмболия легочной артерии и неиллюзорный шанс сыграть в ящик), либо если их нет - можно благополучно истечь кровью.
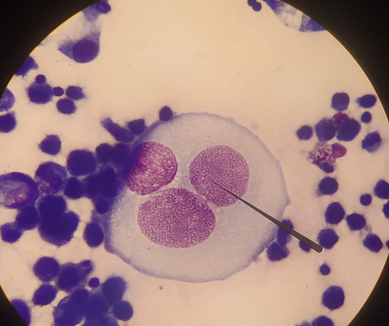
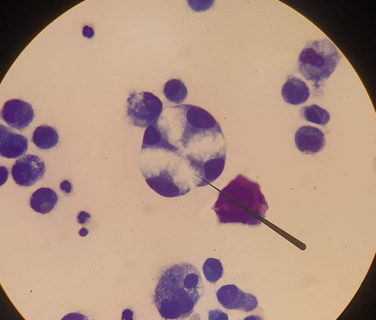
Ну, и небольшой бонус. Немного фоточек выпотных жидкостей, один точно кот, а второй не помню. Но у этих выпотов есть нюанс. Они неопластические. Про онкологию большинство в курсе, а вот как оно может выглядеть на клеточном уровне (диагнозы не скажу уже, диагнозы по итогу не установили, все закончилось эвтаназией)
Надеюсь, получилось достаточно просто, без углублений в глубины наших глубин, понятия не имею, буду ли еще пилить посты, поэтому подписываться особого смысла нет.
Телеги не будет, тег моё, ибо все делал я, фотографировал я, писал я, только материал для исследования чужой, за это спасибо песелям и котелям.
P.S. - черная прямая хреновина на всех фото - указка. Ею просто можно указать на нужную вещь.
Как подготовить машину к долгой поездке
Взять с собой побольше вкусняшек, запасное колесо и знак аварийной остановки. А что сделать еще — посмотрите в нашем чек-листе. Бонусом — маршруты для отдыха, которые можно проехать даже в плохую погоду.
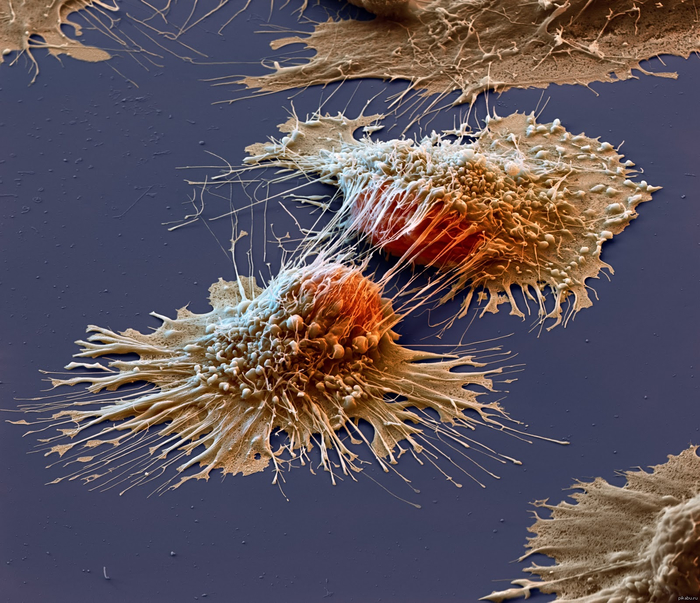
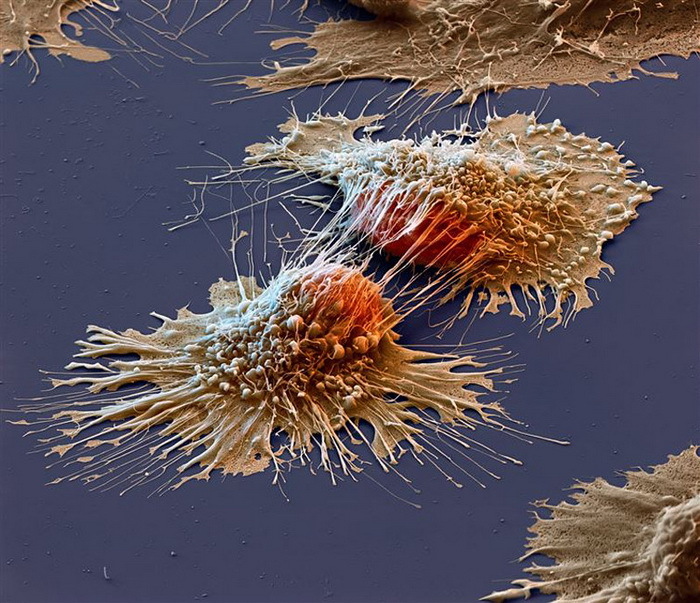
Вот так происходит деление раковых клеток...
Основная проблема заключается в том, что они очень быстро растут и теряют способность к запрограммированному самоуничтожению, которое должно ждать каждую клетку..
ОДУВАНЧИК — МОЩНЫЙ НЕЙТРАЛИЗАТОР РАКОВЫХ КЛЕТОК
Одуванчик может успешно бороться с раковыми клетками, используя губительные вещества, которые находятся в корне растения.
Теперь поговорим поподробнее
Рак является одной из основных причин смерти в мире. Еще большее беспокойство вызывает тот факт, что обнаруживаются все новые и новые виды опухолей. Современная медицина постоянно развивается, особенно в последние десятилетия, и для борьбы с этим заболеванием было создано множество методов лечения. Тем не менее, рак все еще побеждает многих людей. Болезнь устойчива к многочисленным способам лечения.
Хотя химиотерапия является одним из наиболее часто используемых методов борьбы с раком, стоит помнить об альтернативных методах лечения, которые являются довольно многообещающими. Эти методы не должны использоваться в качестве полной замены стандартных средств лечения, но их можно применять в качестве дополнения.
Помните, что лечение не работает одинаково для каждого пациента, и его эффективность значительно зависит от степени развития рака.
Чай от рака из одуванчиков
Одним из альтернативных методов лечения такого серьезного заболевания, как рак, является использование одуванчика. Корни этого растения очень популярны во всем мире из-за многих преимуществ для здоровья.
В древние времена одуванчик использовался для приготовления сиропов и настоев, чтобы бороться с различными проблемами со здоровьем. В настоящее время, однако, известно, что количество ценных свойств, которые он предлагает, определенно больше.
В борьбе с онкологией корень одуванчика влияет только на раковые клетки, оставляя здоровые нетронутым, чего нельзя сказать о химиотерапии.
Считается, что одуванчик борется с раком в 100 раз эффективнее, чем химиотерапия. Чай из одуванчика расщепляет раковые клетки в течение 48 часов после употребления.
Одуванчик содержит витамин В6, тиамин, рибофлавин, витамин С, железо, кальций, калий, фолиевую кислоту и магний. Порция напитка также содержит до 535% необходимой суточной дозы витамина К и около 110% рекомендуемой суточной дозы витамина А.
История из жизни
Один 72-летний пациент прошел интенсивное и агрессивное химиотерапевтическое лечение, которое длилось три года, но рак отказался сдаваться. После этого врачи посоветовали ему вернуться домой, чтобы он смог провести свои последние дни с семьей. В надежде на лучшее будущее, дедушка решил использовать альтернативную медицину.
В поисках чего-то, что могло бы побороть его болезнь, он начал пить чай из одуванчиков. Через четыре месяца тяжесть заболевания уменьшилась, а еще через некоторое время пациент пережил полное выздоровление.
Вот такие чудеса друзья!
Источник статьи https://www.me-d.ru/publ/medicinskoe_oborudovanie/poleznye_sovety/oduvanchik_moshhnyj_nejtralizator_rakovykh_kletok/45-1-0-364
https://doctor.rambler.ru/news/44832979-v-100-raz-effektivne...
https://aif.ru/health/life/oduvanchik_ot_raka_onkologi_schit...
https://www.pravda.ru/news/health/1455784-oduvanchik/
https://vrachonkolog.msk.ru/dzen/lechenie-kornem-oduvanchika...
https://onco.rehab/publikacii/stati/poleznye-materialy/koren...
Как предотвратить метастазы при раке
Команда биологов обнаружила клетки, которые не дают «спящим» в организме раковым клеткам «просыпаться» и образовывать метастазы.
Микрограф рака щитовидной железы / ©Wikipedia
Метастазы могут развиваться в организме даже спустя годы после явно успешного лечения. Они происходят из раковых клеток, которые мигрировали из исходной опухоли в другие органы, и могут бездействовать там в течение длительного периода времени. Теперь ученые обнаружили, как эти клетки просыпаются и образуют метастазы. Выводы опубликованы в журнале Nature.
Команда из Базельского университета и Университетской больницы Базеля (Швейцария) использовала мышей и образцы тканей человека. Ученые исследовали раковые клетки, которые первоначально мигрировали из опухоли молочной железы в печень. Там они некоторое время оставались «спящими», а затем «просыпались», образуя метастазы.
Результаты показали, что ключевую роль в таком переходе играют два типа клеток. Один из них — клетки-киллеры, иммунные клетки, которые убивают аномальные или инфицированные клетки, а также могут замедлять их пролиферацию. По-видимому, они контролируют раковые клетки, выделяя интерферон гамма, который удерживает их в спячке.
Другой тип клеток — клетки Ито — подавляет иммунные клетки и побуждает раковые «проснуться». Причины могут быть разными: например, хроническое воспаление в организме или персистирующая инфекция, объяснили авторы исследования.
Результаты работы определили несколько возможных методов профилактики метастазов. Среди них — иммунотерапия на основе интерлейкина-15, который увеличивает количество естественных киллеров в ткани, и интерфероновая гамма-терапия, поддерживающая раковые клетки в состоянии покоя. А также ингибиторы механизма, посредством которого клетки Ито парализуют киллеры. Соответствующие методы лечения уже существуют, но их нужно тестировать.
«Так называемый период спячки у раковых клеток — важное терапевтическое окно, в котором количество раковых клеток и их гетерогенность еще поддаются контролю. Поэтому понимание клеточных и молекулярных механизмов, определяющих эту самую спячку, имеет решающее значение для предотвращения рецидива рака», — рассказал профессор Мохаммед Бентирес-Альдж, руководитель исследования.
На следующем этапе ученые намерены доказать, что стимуляция естественных клеток-киллеров предотвращает метастазирование у людей. Помимо этого, они изучают способы избежать метастазов не только в печени, но и в других органах.
Белок-регулятор вызывает мутации и в стволовых, и в раковых клетках
Российские ученые выяснили, что белки C/EBP, которые участвуют в работе стволовых клеток и влияют на метаболизм и продолжительность жизни человека, еще и вызывают появление мутаций в регуляторных районах генов. Это может нарушать деление клеток, менять их «жизненный путь» и приводить к серьезным заболеваниям, включая рак.
Ученые установили, что белок-регулятор вызывает мутации и в стволовых, и в раковых клетках / ©Getty images
Результаты работы опубликованы в журнале Cell Reports. Исследование поддержано грантами Российского научного фонда (РНФ). Генетическая информация живых существ, включая человека, закодирована в геноме — наборе молекул ДНК, состоящих из двух цепей. Каждую из них образуют структурные единицы — нуклеотиды четырех типов, — которые можно сравнить с буквами в составе слов.
Буквы, стоящие напротив друг друга в двух цепях молекулы ДНК, подчиняются строгим правилам «спаривания»: напротив «А» стоит «Т», напротив «Г» — «Ц». По разным причинам в ДНК могут случайно происходить замены нуклеотидов, что вызывает нарушение правильного спаривания. Для исправления таких ошибок в клетке есть специальная система.
Если она не справляется с работой, испорченные участки при делении передаются одной из дочерних клеток и становятся мутациями. Мутации в активных районах генома опасны: они могут ошибочно активировать или блокировать работу генов, нарушать деление и менять «судьбу» клеток. Ученые из Института белка РАН (Пущино) с коллегами из НИИ Физико-химической биологии имени А. Н. Белозерского, Института общей генетики имени Н. И. Вавилова и Института молекулярной биологии имени В. А. Энгельгардта (Москва) исследовали частоту возникновения мутаций в разных участках ДНК стволовых клеток взрослого человека.
Такие клетки называются соматическими стволовыми клетками, организм использует их, чтобы поддерживать структуру и обеспечивать регенерацию тканей и органов. Мутации, которые возникают в стволовых клетках, передаются их дочерним при делении и могут приводить к злокачественным новообразованиям. Поэтому для стволовых клеток важно находить в геноме и ошибки, и склонные к ним «хрупкие» участки.
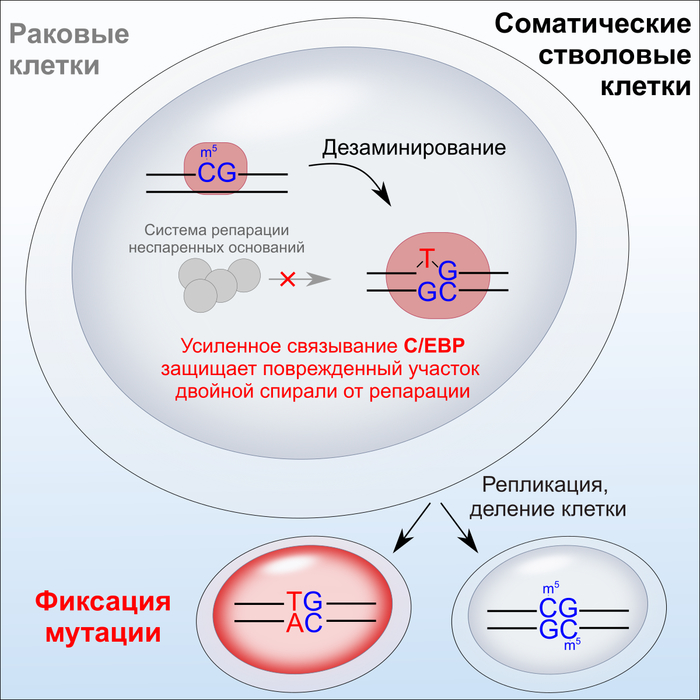
Художественная визуализация механизма появления мутаций / ©Татьяна Руссита
С помощью компьютерных методов исследователи проанализировали информацию о расположении мутаций в ДНК соматических стволовых клеток. Оказалось, что неожиданно часто мутируют места присоединения белков семейства C/EBP. Эти белки — важные регуляторы, которые нужны в различных типах клеток и участвуют во многих процессах — от определения будущей функции клеток до старения организма. Чтобы выяснить причину этих нарушений, ученые построили молекулярную модель взаимодействия одного из C/EBP-белков — C/EBPβ — с ДНК.
Модель предсказала, а эксперимент подтвердил, что белок значительно более прочно связывается с «поврежденными» участками, несущими замену единственного нуклеотида — «Ц» на «Т» — в одной из цепей. Это небольшое изменение приводит к появлению дополнительной водородной связи между белком и ДНК и поэтому к более прочному связыванию. В таком состоянии ДНК оказывается недоступна для системы, которая могла бы исправить неправильную «букву». В результате ошибка в последовательности сохраняется, и при делении клеток мутация передается одной из двух дочерних клеток.
«Интересно, что в дочерних клетках с мутировавшей последовательностью, которую исходно упустила система исправления ошибок, белок C/EBPβ будет связываться достаточно неохотно. Вероятно, что такое нарушение участков связывания C/EBP — еще один неучтенный фактор, затрудняющий адекватную работу стволовых клеток при старении организма или провоцирующий их трансформацию в раковые», — рассказывает Ирина Елисеева, кандидат биологических наук, руководитель гранта РНФ, старший научный сотрудник ИБ РАН.
«Важно, что точечный мутагенез участков посадки белков C/EBP не ограничивается стволовыми клетками: этот же эффект мы обнаружили и в раковых. Мы предполагаем, что усиленное связывание C/EBP с поврежденным участком ДНК может создать для конкретной раковой клетки короткое “окно возможностей” — от момента замены нуклеотида до ближайшего клеточного деления — в которое она временно приобретает новые свойства, например, дополнительно активирует какой-то ген и избегает действия противоопухолевой терапии.
В целом, понимание хрупкости участков посадки C/EBP позволяет по-новому взглянуть на конкретные районы генома, где таких участков много, и мотивирует особенно тщательно их анализировать в районах, управляющих работой онкогенов или онкопротекторов», — предполагает первый автор работы, сотрудница НИИ Физико-химической биологии имени А. Н. Белозерского, кандидат биологических наук Анна Ершова.
Раковые клетки выдерживают химиотерапию без лишних мутаций
Некоторые злокачественные клетки ухитряются выжить после терапии с помощью антиоксидантной защиты.
Химиотерапия не всегда избавляет от рака полностью. Нередко после лечения опухоль возникает снова, и причиной тому – отдельные клетки, которые оказались устойчивы к лекарствам. Их бывает не так много, и большинство из них, хотя и сумели пережить «химическую атаку», делиться уже не могут.
Тем не менее, некоторые устойчивые (или персистирующие) клетки ухитряются снова войти в клеточный цикл – или, проще говоря, начинают делиться, формируя новую опухоль. Можно предположить, что у таких клеток в своё время возникли особые мутации, которые позволили им выжить. Однако в последнее время появляется всё больше данных о том, что механизмы устойчивости могут быть не только генетическими, но и внегенетическими – то есть клетки ухитряются выжить без мутаций, без изменений в генетическом тексте.
Одну из таких работ недавно опубликовали в Nature сотрудники Института Броуда при Массачусетском технологическом институте. Они экспериментировали с клетками рака лёгких, которые стали злокачественными из-за мутации в гене эпидермального фактора роста (EGFR).
Если блокировать белок EGFR веществом под названием озимертиниб, клетки перестанут делиться и начнут умирать. Но если большинство разных клеточных линий (а все линии относились к раку лёгких с мутацией в EGFR) погибали от лекарства, то в 8% появлялись устойчивые клетки, а в 13% из этих восьми устойчивые клетки были ещё и способны к делению. Иными словами, устойчивые клетки появляются довольно рано и из особых клеточных линий (или, грубо говоря, групп) внутри опухоли.
Такие клетки на некоторое время избавляли от лекарства, а потом снова обрабатывали их ядовитой лечебной молекулой. Как оказалось, они снова стали чувствительными к лечению. Если бы своей устойчивостью к лекарству они были обязаны мутации, то мутация наверняка бы сработала снова – клетки стали бы устойчивы раз и навсегда. Отсюда исследователи сделали вывод, что механизм устойчивости к терапии не связан с изменениями в ДНК.
Понять, что это за механизм, удалось с помощью изощрённых методов, позволяющих проанализировать активность генов в отдельно взятой клетке. Выяснилось, что у устойчивых клеток резко усиливалась антиоксидантная защита. При обработке озимертинибом в клетках становится много реактивных форм кислорода – кислородных радикалов, агрессивных окислителей, которые портят клеточные биомолекулы. И чем активнее антиоксидантные системы, тем больше у клетки шансов выжить, и не просто выжить, но и продолжать делиться: у устойчивых клеток, которые перестали делиться, защитные системы работали слабее, чем у тех, кто не просто выдержал атаку лекарством, но и смог потом продолжать размножаться.
Одним из главных антиоксидантных генов оказался NRF2 – если в той или иной линии раковых клеток активность NRF2 искусственным образом повышали, то устойчивых клеток появлялось больше. Кроме того, у устойчивых клеток было больше окисленных жирных кислот. (Вероятно, клетки борются с окислительным стрессом, гася его с помощью жирных кислот и тем самым защищая от повреждения, например, ДНК). Можно предположить, что лекарства, подавляющие активность NRF2 или препятствующие окислению жирных кислот, помогут справиться с устойчивыми к химиотерапии раковыми клетками, причём раковыми клетками из разных опухолей.
Хотя разные вида рака могут возникать из-за разных мутаций, и лекарства против них используют тоже разные, авторам работы удалось показать, что устойчивость к терапии у клеток меланомы, рака груди и колоректального рака зависит от активности NRF2 и степени окисления жирных кислот. Похожие результаты получились не только в экспериментах на клеточных культурах, но и в опытах с мышами, у которых в лёгких формировалась опухоль с мутацией в гене EGFR, аналогичная человеческой.
Ещё раз напомним, что усиление антиоксидантной защиты происходило без специальных мутаций. Гены способны работать сильнее или слабее без изменений в ДНК, которая их кодирует, и вот у некоторых раковых клеток защитные гены работали активнее в силу каких-то случайных факторов.
Несколько лет назад сотрудники Института Броуда публиковали похожую работу о том, что немутационная лекарственная устойчивость среди злокачественных клеток распространена весьма широко. А ещё годом раньше мы рассказывали об экспериментах исследователей института INSERM, которые пришли к выводу, что и для метастазирования раковым клеткам особых мутаций не нужно. С другой стороны, всё это не повод преуменьшать значение мутаций: их у раковых клеток много, и когда их начинают лечить, они стараются мутировать ещё сильнее, чтобы избежать гибели от лекарств.
Автор: Кирилл Стасевич